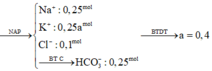cho 188g K2O vào 1 lít dung dịch KOH có D là 1,083g/ml thì được dung dịch A.tìm C% của dung dịch A

Những câu hỏi liên quan
1. Hòa tan 3,1 gam Na2O vào nước được 2 lít dung dịch a. tính nhiệt độ mol trên lít của dung dịch a. 2. Dung dịch KOH 2M (D=1.43g/ml). Tính C%phần trăm của dung dịch Koh
Câu 1 :
a) n Na2O = 3,1/62 = 0,05(mol)
$Na_2O + H_2O \to 2NaOH$
Theo PTHH : n NaOH = 2n Na2O = 0,1(mol)
=> CM NaOH = 0,1/2 = 0,05M
Câu 2 :
Coi n KOH = 1(mol)
=> V dd KOH = 1/2 = 0,5(lít) = 500(ml)
=> mdd KOH = D.V = 500.1,43 = 715(gam)
=> C% KOH = 1.56/715 .100% = 7,83%
Đúng 1
Bình luận (0)
1. Ta có : \(n_{Na_2O}=\dfrac{m}{M}=0,05mol\)
\(PTHH:Na_2O+H_2O\rightarrow2NaOH\)
Theo PTHH: \(n_{NaOH}=2n_{Na_2O}=0,1mol\)
\(\Rightarrow C_{MNaOH}=\dfrac{n}{V}=0,05M\)
2. - Gọi số lít KOH là a lít
\(\Rightarrow m_{dd}=D.V=1430a\left(g\right)\)
Mà \(n_{KOH}=C_M.V=2amol\)
\(\Rightarrow m_{KOH}=n.M=112a\left(g\right)\)
\(\Rightarrow C\%=\dfrac{m}{m_{dd}}.100\%=\dfrac{112a}{1430a}.100\%=~7,83\%\)
Đúng 0
Bình luận (0)
: Tính nồng độ mol của dung dịch thu được khi:
a/ Cho 4 gam NaOH vào nước được 200 ml dung dịch NaOH.
b/ Cho 2,82 gam K2O vào nước được 250 ml dung dịch KOH.
a) \(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(C_M=\dfrac{0,1}{0,2}=0,5M\)
b) \(n_{K_2O}=\dfrac{2,82}{94}=0,03\left(mol\right)\)
PTHH: K2O + H2O --> 2KOH
0,03------------->0,06
=> \(C_M=\dfrac{0,06}{0,25}=0,24M\)
Đúng 6
Bình luận (0)
\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\\ C_M=\dfrac{0,1}{0,2}.=0,5M\)
\(n_{K_2O}=\dfrac{2,82}{94}=0,03\left(mol\right)\\ C_M=\dfrac{0,03}{0,25}=0,12M\)
Đúng 3
Bình luận (0)
Hấp thụ hoàn toàn V lít CO2 vào 250 ml dung dịch hỗn hợp NaOH 0,4M và KOH aM thì thu được dung dịch X. Cho từ từ 250 ml dung dịch H2SO4 0,5M vào X thu được dung dịch Y và 1,68 lít khí (đktc). Cho Ba(OH)2 dư vào Y thấy xuất hiện 34,05 gam kết tủa trắng. Giá trị của a là A. 0,7M B. 0,6M C. 0,9M. D. 0,5M.
Đọc tiếp
Hấp thụ hoàn toàn V lít CO2 vào 250 ml dung dịch hỗn hợp NaOH 0,4M và KOH aM thì thu được dung dịch X. Cho từ từ 250 ml dung dịch H2SO4 0,5M vào X thu được dung dịch Y và 1,68 lít khí (đktc). Cho Ba(OH)2 dư vào Y thấy xuất hiện 34,05 gam kết tủa trắng. Giá trị của a là
A. 0,7M
B. 0,6M
C. 0,9M.
D. 0,5M.
Hấp thụ hoàn toàn 3,92 lít CO2 (đktc) bằng 250 ml dung dịch hỗn hợp Na2CO3 0,5M và KOH aM thu được dung dịch X. Nhỏ từ từ đến hết 200 ml dung dịch HCl 0,5M vào dung dịch X thì thấy có 1,12 lít khí (đktc) thoát ra. Giá trị của a là
A. 0,4.
B. 1,5.
C. 1,4.
D. 1,2.
Hấp thụ hoàn toàn 3,92 lít CO2 (đktc) bằng 250 ml dung dịch hỗn hợp Na2CO3 0,5M và KOH aM thu được dung dịch X. Nhỏ từ từ đến hết 200 ml dung dịch HCl 0,5M vào dung dịch X thì thấy có 1,12 lít khí (đktc) thoát ra. Giá trị của a là A. 0,4. B. 1,5. C. 1,4. D. 1,2.
Đọc tiếp
Hấp thụ hoàn toàn 3,92 lít CO2 (đktc) bằng 250 ml dung dịch hỗn hợp Na2CO3 0,5M và KOH aM thu được dung dịch X. Nhỏ từ từ đến hết 200 ml dung dịch HCl 0,5M vào dung dịch X thì thấy có 1,12 lít khí (đktc) thoát ra. Giá trị của a là
A. 0,4.
B. 1,5.
C. 1,4.
D. 1,2.
Đáp án A.
Dung dịch cuối cùng thu được gồm Na+ (0,25 mol), K+ (0,25a mol), HCO3– và Cl– (0,1 mol).
![]()
![]()
Đúng 0
Bình luận (0)
hòa tan 35,25 gam K2O vào nước được 0,75 lít dung dịch A
a)tính nồng độ mol của dung dịch A
b)Dẫn từ từ 8,4 lít khí CO2 dktc vào dung dịch A Hãy tính khối lượng muối thu được sau phản ứng
c)Nếu Trung Hòa vừa đủ dung dịch A thì cần bao nhiêu ml dung dịch H2SO4 60% (D = 1,5 g / ml)
a) PTHH: \(K_2O+H_2O\rightarrow2KOH\)
Ta có: \(n_{KOH}=2n_{K_2O}=2\cdot\dfrac{35,25}{94}=0,75\left(mol\right)\)
\(\Rightarrow C_{M_{KOH}}=\dfrac{0,75}{0,75}=1\left(M\right)\)
b) Ta có: \(\left\{{}\begin{matrix}n_{KOH}=0,75\left(mol\right)\\n_{CO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo muối trung hòa
PTHH: \(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
Theo PTHH: \(n_{K_2CO_3}=0,375\left(mol\right)\) \(\Rightarrow m_{K_2CO_3}=0,375\cdot138=51,75\left(g\right)\)
c) PTHH: \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
Theo PTHH: \(n_{H_2SO_4}=0,375\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,375\cdot98}{60\%}=61,25\left(g\right)\) \(\Rightarrow V_{ddH_2SO_4}=\dfrac{61,25}{1,5}\approx40,83\left(ml\right)\)
Đúng 2
Bình luận (1)
So mol cua kali oxit
nK2O = \(\dfrac{m_{K2O}}{M_{K2O}}=\dfrac{35,25}{94}=0,375\) (mol)
Pt : K2O + H2O \(\rightarrow\) 2KOH \(|\)
1 1 2
0,375
a) So mol cua dung dich kali hidroxit
nKOH = \(\dfrac{0,375.2}{1}=0,75\) (mol)
Nong do mol cua dung dich kali hidroxit
CMKOH = \(\dfrac{n}{v}=\dfrac{0,75}{0,75}=1\) (M)
b) So mol cua khi cacbon dioxit
nCO2 = \(\dfrac{V_{CO2}}{22,4}=\dfrac{8,4}{22,4}=0,375\) (mol)
Pt : CO2 + 2KOH \(\rightarrow\) K2CO3 + H2O\(|\)
1 2 1 1
0,375 0,75
Lap ti so so sanh : \(\dfrac{0,375}{1}=\dfrac{0,75}{2}\)
So mol cua muoi kali cacbonat
nK2CO3 = \(\dfrac{0,375.1}{1}=0,375\) (mol)
Khoi luong cua muoi kali cacbonat
mK2CO3 = nK2CO3 . MK2CO3
= 0,375 . 138
= 51,75 (g)
c) 2KOH + H2SO4 \(\rightarrow\) K2SO4 + 2H2O\(|\)
2 1 1 2
0,75
So mol cua axit sunfuric
nH2SO4 = \(\dfrac{0,75.1}{2}=0,375\) (mol)
Khoi luong cua axit sunfuric
mH2SO4 = nH2SO4 . MH2SO4
= 0,375 . 98
= 36,75 (g)
Khoi luong cua dung dich axit sunfuric C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{36,75.100}{60}=61,25\) 0/0
The tich cua dung dich axit sunfuric can dung
D = \(\dfrac{m}{V}\Rightarrow V=\dfrac{m}{D}=\dfrac{61,25}{1,5}=40,8\left(ml\right)\)
Chuc ban hoc tot
Đúng 0
Bình luận (4)
Hấp thụ hoàn toàn 1,12 lít khí CO2 (đktc) vào 200 ml dung dịch KOH 1M, thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là A. 80ml. B. 60 ml C. 40 ml D. 100ml.
Đọc tiếp
Hấp thụ hoàn toàn 1,12 lít khí CO2 (đktc) vào 200 ml dung dịch KOH 1M, thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
A. 80ml.
B. 60 ml
C. 40 ml
D. 100ml.
Hấp thụ hoàn toàn 1,12 lít CO2 (đktc) vào 150 ml dung dịch KOH 1M, thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là A. 80. B. 40. C. 60. D. 100.
Đọc tiếp
Hấp thụ hoàn toàn 1,12 lít CO2 (đktc) vào 150 ml dung dịch KOH 1M, thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
A. 80.
B. 40.
C. 60.
D. 100.
Hấp thụ hoàn toàn 1,12 lít khí
C
O
2
(đktc) vào 200 ml dung dịch KOH 1M thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là A. 80 B. 60 C. 40 D. 100
Đọc tiếp
Hấp thụ hoàn toàn 1,12 lít khí C O 2 (đktc) vào 200 ml dung dịch KOH 1M thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
A. 80
B. 60
C. 40
D. 100