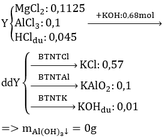
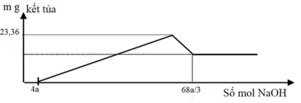
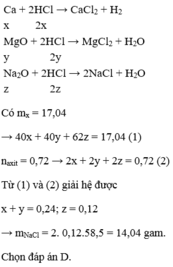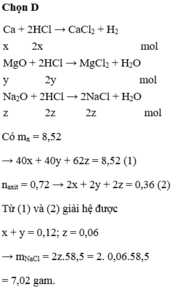hỗn hợp X có MgO và CaO, hỗn hợp Y có MgO va Al2O3 khối lượng X = khối lượng Y = 9,6gam . Số gam MgO trong X = 1,125 lần số gam MgO trong Y. Cho X,Y đều tac dụng với 100 ml dd HCl 19,87 % ( D=1,047) thì được dd X' va Y' khi cho X' tac dụng hết với Na2CO3 thì có 1,904 dm3 khí CO2 thoat ra (đktc)
a, Tính % khối lượng cac chat trong X và nồng độ % của các chất trong X'
b, Hỏi Y có tan hết không nếu cho 300ml KOH 2M vao dd thì tách ra bao nhiêu gam kết tủa