Clo có 2 đồng vị bền \(\overline{A}\)Cl = 35,45. Đồng vị 1: A1 = 37; 17p chiếm 25%. Viết KHNT của 2 đồng vị?

Những câu hỏi liên quan
Clo có nguyên tử khối trung bình là 35,45. Hỏi có bao nhiêu nguyên tử của đồng vị Cl 17 35 trong 100 ml dung dịch HCl 0,1M?
Biết: Clo chỉ có hai đồng vị Cl 17 35 và Cl 17 37 ; số Avogadro N = 6,02.10^23
Trong tự nhiên nguyên tố Cl có 2 đồng vị A1 Cl và A2 Cl chiếm 75 phần trăm.Nguyên tử khối trung bình của Nguyên tố Clo là 35,5.Biết rằng A1 - A2 bằng 2.Xác định 2 đồng vị của Clo
Theo đề : \(A_1-A_2=2\left(1\right)\)
\(\overline{M}_{Cl}=\dfrac{A_1.\left(100-75\right)+A_2.75}{100}=35,5\)
\(\Leftrightarrow25A_1+75A_2=3550\left(2\right)\)
Từ(1),(2)\(\Rightarrow\left\{{}\begin{matrix}A_1=37\\A_2=35\end{matrix}\right.\)
Vậy 2 đồng vị của Clo là : 37Cl và 35Cl
Chúc bạn học tốt
Đúng 3
Bình luận (0)
Clo có 2 đồng vị bền \(^{35}_{17}Cl\) (chiếm 75%) , \(^{37}_{17}Cl\) (chiếm 25%). Hãy tìm số nguyên tử đồng vị \(^{37}_{17}Cl\) có trong 2,22 gam CaCl2
ta có :
Atb=\(\frac{35\cdot75+37\cdot25}{100}\)
=35,5
số mol CaCl2 là :
nCaCl2=\(\frac{2,22}{40+35,5\cdot2}\)
=0,02mol
số mol Cl trong CaCl2 la: nCaCl2 = 0,02*2=0,04mol
số nguyên tử 37Cl trong 2,22g CaCl2 là :
0,04*2*6,02*1023*25%=1,2*1022nguyên tử
Đúng 0
Bình luận (0)
Nguyên tử khối trung bình của Clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35 Cl và 37 Cl. Tính phần trăm về khối lượng của 37 Cl chứa trong HClO4 (với Hidro đồng vị là 1 H, oxi đồng vị là 16 O)
\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Đúng 3
Bình luận (1)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
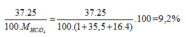
Đúng 1
Bình luận (2)
Trong tự nhiên, clo có 2 đồng vị bền là 35 Cl và 37 Cl. Biết nguyên tử khối trung bình của clo là 35,5.Thành phần % về khối lượng của đồng vị 35 Cl trong hợp chất HClO a là 31,065%. Tìm giá trị của a
biết nguyên tử khối của H:1, O:16.
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
Đúng 0
Bình luận (0)
Clo có hai đồng vị bền : 3517Cl và 3717Cl . Nguyên tử khối trung bình của clo là 35 , 5 . Tính thành phần phần trăm số nguyên tử của mỗi đồng vị .
HELP ME !!!!!!
30. Nguyên tố Clo trong tự nhiên gồm 2 đồng vị bền là 1735Cl và 3717Cl, biết rằng 7,108 gam khí Clo chiếm thể tích 2,24 lít (đktc). Xác định thành phần % về số mol của các đồng vị 1735Cl và 1737Cl lần lượt là?
Nguyên tố Clo trong tự nhiên gồm 2 đồng vị bền 1735Cl và 1737Cl, biết rằng 7,108 gam khí Clo chiếm thể tích 2,24 lít(đktc). Xác địng thành phần phần trăm về số mol của các đồng vị 1735Cl và 1737Cl lần lượt là?
Nguyên tử Clo trong tự nhiên có 2 đồng vị \(^{35}_{17}Cl\) và \(^{37}_{14}Cl\) . Biết \(\overline{A}=35,5\)
a) Tính % của từng đồng vị
b) Tính % của \(^{35}Cl\) trong KClO4
a) Gọi x là thành phần phần trăm của \(_{17}^{35}Cl\)
Ta có: \(\overline{A}=\frac{35x+37\left(100-x\right)}{100}=35,5\leftrightarrow x=75\)
Vậy trong tự nhiên đồng vị \(_{17}^{35}Cl\) chiếm 75% và \(_{17}^{37}Cl\) chiếm 25%
b) Ta có \(\%Cl=\frac{35,5\cdot100}{39+35,5+16\cdot4}=\frac{7100}{277}\sim25,63\%\)
\(\Rightarrow\%^{35}Cl=\frac{25,63\cdot75}{100}=\frac{7689}{400}\sim19,22\%\)
Đúng 0
Bình luận (0)



















