Cho a mol kim loại R tan vừa hết trong đ chứa a mol H2SO4 thì thu được 1,56g muối và 1 khí A. Hấp thụ hoàn toàn khí A vào 45ml dd NaOH 0,2M thì thấy tạo thành 0,608g muối. Tìm R

Những câu hỏi liên quan
45. Khử hoàn toàn 7,12 gam oxit kim loại bằng khí hiđro dư, sau khi phản ứng kết thúc thu được 1,602 gam nước. Nếu hòa tan hết lượng oxit trên vào dd HCl thì nhận được 0,089 mol muối clorua.a/Tìm công thức oxit b/Tính khối lượng chất rắn thu được sau khi khửc/Tính thể tích dd HCl 1,2M cần dùng.
Đọc tiếp
45. Khử hoàn toàn 7,12 gam oxit kim loại bằng khí hiđro dư, sau khi phản ứng kết thúc thu được 1,602 gam nước. Nếu hòa tan hết lượng oxit trên vào dd HCl thì nhận được 0,089 mol muối clorua.
a/Tìm công thức oxit b/Tính khối lượng chất rắn thu được sau khi khử
c/Tính thể tích dd HCl 1,2M cần dùng.
hòa tan hết 22.6 gam hỗn hợp gồm Fe và các oxit sắt trong 240 gam dd HNO3 31.5% thu được dd X ( không chứa muối amoni)và hỗn hợp khí T . cho từ từ đến hết 680ml dd NaOH 1.5M vào dung dịch X thu được 32.1 gam kết tủa duy nhất. Mặt khác hòa tan hoàn toàn hết 22.16 gam hỗn hợp trên cần dùng V lít dd chứa HCl 1M và H2SO4 0.5M thu được dd Y chứa 49.09 gam muối và 1.792 lít khí H2. Nồng độ C% của muối sắt có trong dd X là
Đọc tiếp
hòa tan hết 22.6 gam hỗn hợp gồm Fe và các oxit sắt trong 240 gam dd HNO3 31.5% thu được dd X ( không chứa muối amoni)và hỗn hợp khí T . cho từ từ đến hết 680ml dd NaOH 1.5M vào dung dịch X thu được 32.1 gam kết tủa duy nhất. Mặt khác hòa tan hoàn toàn hết 22.16 gam hỗn hợp trên cần dùng V lít dd chứa HCl 1M và H2SO4 0.5M thu được dd Y chứa 49.09 gam muối và 1.792 lít khí H2. Nồng độ C% của muối sắt có trong dd X là
A là hỗn hợp của cacbonat trung hòa của 2 kim loại X( hóa trị i ) và Y hóa trị ii. Hòa tan hoàn toàn 18g hỗn hợp a bằng ddHCl vừa đủ thì thu được 2,24l khí ở đktc và dd B
a)nếu cô cạn dd B thì thu được bao nhiêu gam muối khan
b) Nếu tỉ lệ số mol muối cacbonat của X và muối cacbonat của Y là 2:1, NTK X>Y là 15đvC. Xác định công thức của 2 muối
Hòa tan hoàn toàn 5,95g hỗn hợp muối cacbonat của kim loại hóa trị I và kim loại hóa trị II trong dd HCl thì sinh ra 1,12l khí (đktc). Đem cô cạn dung dịch sau phản ứng thì thu được bao nhiêu (g) muối khan.
Ta có:
\(n_{CO_2}=\frac{1.12}{22.4}=0.05\left(mol\right)\) \(\Rightarrow m_{CO_2}=0.05\times44=2.2\left(g\right)\)
\(X_2CO_3+2HCl\rightarrow2XCl+H_2O+CO_2\)
\(YCO_3+2HCl\rightarrow YCl_2+H_2O+CO_2\)
Ta thấy
\(n_{HCl}=2n_{CO_2}=2\times0.05=0.1\left(mol\right)\)
\(\Rightarrow\) \(m_{HCl}=0.1\times36.5=3.65\left(g\right)\)
\(n_{H_2O}=n_{CO_2}=0.05\left(mol\right)\)
\(\Rightarrow\) \(m_{H_2O}=0.05\times18=0.9\left(g\right)\)
Áp dụng định luật bảo toàn khối lượng ta được:
\(m_{XCl+YCl_2}=\left(5.95+3.65\right)-\left(2.2+0.9\right)=9.6-3.1=6.5\left(g\right)\)
Đúng 0
Bình luận (1)
Nung 12,64 gam hỗn hợp FeCO3 và FexOy trong không khí tới khi phản ứng xảy ra hoàn toàn thu được sản phẩm khí A và 11,2 gam chất rắn. Cho khí A hấp thụ hết vào 200ml dung dịch Ba(OH)2 0,15M thấy có 3,94 gam kết tủa tạo thành.
a) Viết các phương trình hóa học xảy ra.
b) Tìm công thức phân tử FexOy.
a)
4FeCO3 + O2 --> 2Fe2O3 + 4CO2 (1)
4FexOy + (3x-2y)O2 --> 2xFe2O3 (2)
CO2 + Ba(OH)2 → BaCO3 + H2O (3)
2CO2 + Ba(OH)2 → Ba(HCO3)2 (4)
b)
Giả sử Ba(OH)2 dư , chỉ xảy ra (3) không xảy ra pư (4)
nBaCO3 = 0,02 mol = nCO2
=> nFe2O3 (1) = 0,01 mol
Mà \(\Sigma\)nFe2O3 (1) + (2) = \(\dfrac{11,2}{160}\)= 0,07 mol => nFe2O3 (2) = 0,07 -0,01 = 0,06 mol
=> nFexOy = \(\dfrac{0,12}{x}\) mol
mFexOy = 12,64 - mFeCO3 = 12,64 - 0,02.116 = 10,32 gam
=> M FexOy = 86x (g/mol)
Với x = 1,2,3 ... đều không thỏa mãn
=> Ba(OH)2 phản ứng hết, xảy ra cả phản ứng (3) và (4)
nBa(OH)2 = 0,03 mol , nBaCO3 = 0,02 mol
=> nBa(OH)2 (4) = 0,03 - 0,02 = 0,01 mol
=> nCO2 (4) = 0,01.2 = 0,02 mol
=> nCO2 (1) = nCO2 (3) + nCO2 (4) = 0,04 mol
<=> nFe2O3 (1) = 0,02 mol , nFeCO3 = 0,04 mol
=> nFe2O3 (2) = 0,07 - 0,02 = 0,05 mol <=> n FexOy = \(\dfrac{0,1}{x}\) mol
mFexOy = 12,64 - mFeCO3 = 12,64 - 0,04.116 = 8 gam
=> M FexOy = 80x (g/mol)
với x = 2 => mFexOy = 160 (g/mol) <=> Fe2O3
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn m gam FeS2 bằng một lượng O2 vừa đủ, thu được khí X. Hấp thụ hết X vào 1 lít dung dịch chứa Ba(OH)2 0,15M và KOH 0,1M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa. Giá trị của m là: A. 23,2 B. 12,6 C. 18,0 D. 24,0
Đọc tiếp
Đốt cháy hoàn toàn m gam FeS2 bằng một lượng O2 vừa đủ, thu được khí X. Hấp thụ hết X vào 1 lít dung dịch chứa Ba(OH)2 0,15M và KOH 0,1M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa. Giá trị của m là:
A. 23,2
B. 12,6
C. 18,0
D. 24,0
Đáp án C
Pt pư:
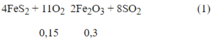
Ta có: nBaC03 = 0,15 mol
nKOH = 0,1 mol ⇒ nBa2+ = 0,15 mol ; nOH- = 0,4 mol
Khi cho SO2 vào dung dịch Y thu được 21,7 (g) BaSO3. Cho Y tác dụng với dung dịch NaOH thấy xuất hiện thêm kết tủa, chứng tỏ trong dung dịch Y có ion HSO3-.
Vì: Ba2+ + HSO3- + OH- " BaSO3 + H2O
Ta có: nBaC03 = 0,1 mol
Ptpứ:
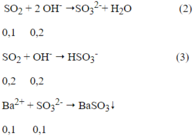
Ta có: nOH- = 0,4 - 0,2 = 0,2 mol
Theo ptpư (2), (3) ta có: n SO2= 0,1 + 0,2 = 0,3 mol
Theo ptpư (1) ta có: n FeS2 = ½ n SO2= 0,15 mol ⇒ m FeS2 = 120.0,15 = 18(g)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là A. 3 : 5. B. 4 : 3. C. 2 : 3 D. 3 : 2.
Đọc tiếp
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là
A. 3 : 5.
B. 4 : 3.
C. 2 : 3
D. 3 : 2.
Chọn B.
Theo đề ta có: n O 2 = 1 , 225 ; n C O 2 = 1 , 05 v à n H 2 O = 1 , 05 => X no, đơn chức, mạch hở (vì n C O 2 = n H 2 O )
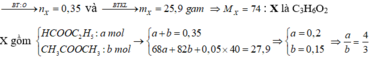
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là A. 3 : 5 B. 4 : 3 C. 2 : 3 D. 3 : 2
Đọc tiếp
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là
A. 3 : 5
B. 4 : 3
C. 2 : 3
D. 3 : 2
Hoà tan hoàn toàn hỗn hợp A gồm Al và kim loại X ( hoá trị a ) trong H2SO4 đặc , nóng đến khi không còn khí thoát ra thu được dung dịch B và khí C . Khí C bị hấp thụ NaOH dư tạo ra 50,4g muối .
Khi thêm vào A một lượng kim loại X bằng 2 lần lượng kim loại X có trong A ( giữ nguyên lượng Al ) rồi hoà tan bằng H2SO4 đăc nóng thì lượng muối trong dung dịch mới tăng thêm 32g so với muối trong dung dịch B nhưng nếu giảm một nửa lượng Al có trong...
Đọc tiếp
Hoà tan hoàn toàn hỗn hợp A gồm Al và kim loại X ( hoá trị a ) trong H2SO4 đặc , nóng đến khi không còn khí thoát ra thu được dung dịch B và khí C . Khí C bị hấp thụ NaOH dư tạo ra 50,4g muối .
Khi thêm vào A một lượng kim loại X bằng 2 lần lượng kim loại X có trong A ( giữ nguyên lượng Al ) rồi hoà tan bằng H2SO4 đăc nóng thì lượng muối trong dung dịch mới tăng thêm 32g so với muối trong dung dịch B nhưng nếu giảm một nửa lượng Al có trong A ( giữ nguyên lượng X ) thì khi hoà tan ta thu được là 5,6 lít khí (đktc ) khí C .
1, Tính khối lượng nguyên tử X biết rằng số hạt (p,n,e ) trong X là 93 .
2. Tính % về khối lượng các kim loại trong A .
P/s : giải ra r nhưng đăng lên để tìm cách mới để học hỏi .
Ta có: số hạt (p,n,e ) trong X là 93 .
\(\Rightarrow\dfrac{93}{3,2222}\le p\le\dfrac{93}{3}\)
\(\Leftrightarrow\left[{}\begin{matrix}p=29\\p=30\\p=31\end{matrix}\right.\)
=> X có hóa trị II
Hỗn hợp A: \(\left\{{}\begin{matrix}Al:a\left(mol\right)\\X:b\left(mol\right)\end{matrix}\right.\)
\(2Al\left(a\right)+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2\left(1,5a\right)+6H_2O\)
\(X\left(b\right)+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}XSO_4+SO_2\left(b\right)+2H_2O\)
\(SO_2\left(1,5a+b\right)+2NaOH\rightarrow Na_2SO_3\left(1,5a+b\right)+H_2O\)
\(n_{Na_2SO_3}=0,4\left(mol\right)\)
\(\Rightarrow1,5a+b=0,4\left(I\right)\)
Khi thêm vào A một lượng kim loại X bằng 2 lần lượng kim loại X có trong A ( giữ nguyên lượng Al )
rồi hoà tan bằng H2SO4 đăc nóng thì lượng muối trong dung dịch mới tăng thêm 32g so với muối trong dung dịch B
\(X\left(2b\right)+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}XSO_4\left(2b\right)+SO_2+2H_2O\)
\(\Rightarrow2b\left(X+96\right)=32\left(II\right)\)
Khi giảm một nửa lượng Al có trong A ( giữ nguyên lượng X ) thì khi hoà tan ta thu được là 5,6 lít khí (đktc ) khí C .
\(2Al\left(0,5a\right)+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2\left(0,75a\right)+6H_2O\)
\(X\left(b\right)+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}XSO_4+SO_2\left(b\right)+2H_2O\)
\(n_{SO_2}=0,25\left(mol\right)\)
\(\Rightarrow0,75a+b=0,25\left(III\right)\)
Từ \(\left(I\right)\&\left(III\right)\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
Thay vào \(\left(II\right)\Rightarrow X=64\left(Cu\right)\)
Suy ra % về khối lượng các kim loại trong A .
Đúng 0
Bình luận (0)
Nếu đề cho X có hóa trị = bao nhiêu thì quá dễ dàng.
Còn nếu ko cho thì vs bài này mk sẽ xét 3 tường hợp: a = 1;2;3.
Mặc dù hơi dài nhưng sẽ ra.
Đúng 0
Bình luận (2)
Thấy tỉ tỉ với tiểu đệ cứ nói bài dài
dài cái j
quan trọng làm ra không thôi
mấy thánh cứ ngồi chém Minh Thương, Kiệt BD .
Đúng 0
Bình luận (0)
Xem thêm câu trả lời