biết khí A có tỉ lệ khối với X bằng 0,5.Một lít khí X ở (đktc) nặng 1,428 gam.tính khối lượng mol của khí A.

Những câu hỏi liên quan
Biết tỉ khối khí A so với khí B là 0,5; 1 lít khí B (đktc) nặng 2,857 gam. Hãy xác định khối lượng mol của A,B
\(d_{\dfrac{A}{B}}=0,5\Rightarrow\dfrac{A}{B}=\dfrac{1}{2}\Leftrightarrow2A=B\)
\(n_B=\dfrac{1}{22,4}=\dfrac{2,857}{B}\Rightarrow B=2,857.22,4\approx64\left(g\right)\)
=> A= 64/2 = 32(g)
vậy MA= 32(g)
MB= 64(g)
Đúng 2
Bình luận (2)
tính khối lượng mol của khí A. biết khí a có tỉ khối so với khí X bằng 0.5. Biết 1 lít khí X ở điều kiên tiêu chuẩn thì nặng 1,428g
Biết khí A có tỉ khối so với khí X bằng 0,5, biết 1l khí x ở điều kiện tự nhiên thì nặng 1,428g. Xác định khối lượng mol của khí A
Hóa học 8 nha mn
tính mol khí a biết khí a có tỉ khối so với khí x=0.5 biết 11 khí x ở đktc nặng 1.428g vậy khối lượng khí a là bao nhiêu
Để tính mol khí a, ta cần biết khối lượng khí a.
Theo đề bài, khí a có tỉ khối so với khí x là 0.5. Tỉ khối được định nghĩa là khối lượng của một đơn vị khối lượng của khí a so với khối lượng của một đơn vị khối lượng của khí x.
Vì vậy, ta có thể tính được khối lượng của khí a bằng cách nhân khối lượng của khí x với tỉ khối:
Khối lượng khí a = Khối lượng khí x * Tỉ khối
Trong trường hợp này, khối lượng của 11 khí x là 1.428g.
Vậy: Khối lượng khí a = 1.428g * 0.5 = 0.714g
Vậy khối lượng của khí a là 0.714g.
Đúng 2
Bình luận (0)
Bài 1: Cho biết 0,5 mol hợp chất khí A nặng 32g a , Tính khối lượng mol khí A b , Tính thể tích khí (ở đkctc ) của 36*10^23 c , Tính khối lượng của 73,44 lít khí CO2 ( ở đktc )
b . n=36x1023/6x1023=6(mol)
V=6x22,4=134,4 g
Đúng 1
Bình luận (0)
biết A có tỉ khối so với khí X bằng 0,5. mặt khác 1 lít khí X ở đktc nặng 1,428. tính khối lượng mol của khí A
MX=22,4.1,428\(\approx\)32 đvC
MA=0,5MX=0,5.32=16 đvC
Đúng 0
Bình luận (0)
1.Tính số mol của: a. 7,3 gam HCl b. 8,96 lít khí CH4 ở đktc c. 15.1023 phân tử H2O
2.Cho biết 2,24 lít khí A ở đktc có khối lượng là 3 gam
a. Tính khối lượng mol của khí A b. Tính tỉ khối của A so với Oxi
1)
a) \(n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
b) \(n_{CH_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
c) \(n_{H_2O}=\dfrac{15.10^{23}}{6.10^{23}}=2,5\left(mol\right)\)
2)
a) \(n_A=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) => MA = \(\dfrac{3}{0,1}=30\left(g/mol\right)\)
b) \(d_{A/O_2}=\dfrac{30}{32}=0,9375\)
Đúng 0
Bình luận (0)
2 . a, Tính khối lượng của 0,5 Mol MgTính thể tích ( ở đktc ) của 0,25 Mol khí SO2b, Tính khối lượng của hỗn hợp khí gồm 16,8 lít khí N2 và 5,6 lít O2 . Biết các khí đó ở đktc
mMg = 0,5.24 = 12 gam
VSO2 = n.22,4 = 0,25.22,4 = 5,6 lít
nN2 = \(\dfrac{16,8}{22,4}\)= 0,75 mol , nO2 = \(\dfrac{5,6}{22,4}\)= 0,25 mol
=> m(N2 + O2 ) = 0,75.28 + 0,25.32 = 29 gam
Đúng 0
Bình luận (0)
Hỗn hợp X gồm một số amin no đơn chức, mạch hở có tỉ khối so với H2 bằng 425/22. Trộn X với một hidrocacbon Y theo tỉ lệ khối lượng là 17:6 thu được 0,16 mol hỗn hợp khí Z. Đốt cháy hoàn toàn Z thu được 7,28 lít khí ở đktc và 8,73 gam nước. Khối lượng của Y có trong 0,16 mol Z là: A. 1,5 gam B. 1,04 gam C. 4,84 gam D. 2,88 gam
Đọc tiếp
Hỗn hợp X gồm một số amin no đơn chức, mạch hở có tỉ khối so với H2 bằng 425/22. Trộn X với một hidrocacbon Y theo tỉ lệ khối lượng là 17:6 thu được 0,16 mol hỗn hợp khí Z. Đốt cháy hoàn toàn Z thu được 7,28 lít khí ở đktc và 8,73 gam nước. Khối lượng của Y có trong 0,16 mol Z là:
A. 1,5 gam
B. 1,04 gam
C. 4,84 gam
D. 2,88 gam
Chọn đáp án A.
Gọi ![]()
Ta có:
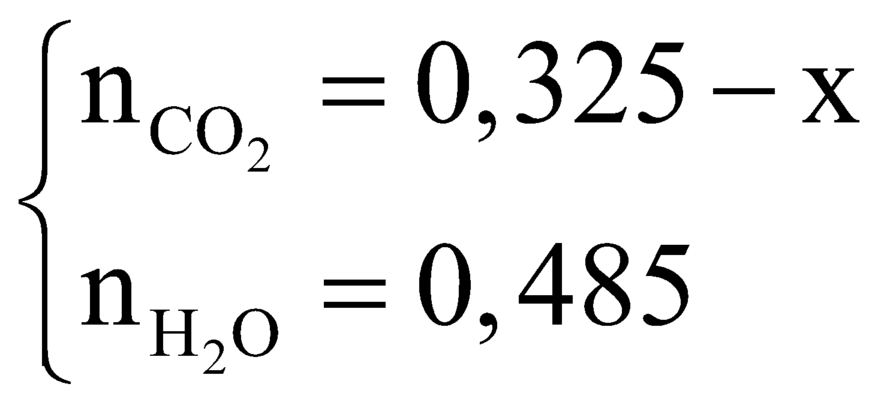
Khối lượng amin trong Z là:
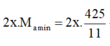
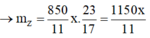
Bảo toàn khối lượng:
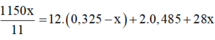
![]()
![]()
Đúng 0
Bình luận (0)





















