2/ Tính pH của các dung dịch sau: a) Dung dịch NaOH 0,01M b) Dung dịch Ba(OH)2 0,005M

Những câu hỏi liên quan
Trộn 250ml dung dịch hỗn hợp gồm H2SO4 0,005M và HCl 0,01M với 200ml dung dịch hỗn hợp gồm NaOH 0,001M và Ba(OH)2 0,0005M thu được dung dịch X. Dung dịch X có pH là:
A. 12,3
B. 1,18
C. 11,87
D. 2,13
Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 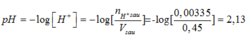
Đúng 0
Bình luận (0)
Tính pH của dung dịch sau:
a, 1 lít dung dịch hỗn hợp NaOH 0,005M; KOH 0,005M và Ba(OH)2 0,005M
NaOH và KOH: \(pOH=2,3\Rightarrow pH=11,7\)
\(Ba\left(OH\right)_2:\) \(\left[OH^-\right]=0,005\cdot2=0,01M\)
\(pOH=2\Rightarrow pH=12\)
Đúng 0
Bình luận (0)
Cho dung dịch X là dung dịch HCl 0,01M . Dung dịch Y là dung dịch Ba(OH)2 0,005M
a/ Tính pH của dung dịch X và pH của dung dịch Y .
b/ Trộn 300 ml dd X với 200 ml dd Y thu được 500 ml dd Z . Tính pH của dd Z .
Tính pH của các dung dịch sau :
a/ 100 ml dung dịch X có hòa tan 2,24 lít khí HCl ( đktc )
b/ Dung dịch HNO3 0,001M
c/ Dung dịch H2SO4 0,0005M
d/ Dung dịch NaOH 0,001M
e/ Dung dịch Ba(OH)2 0,005M
f/ Dung dịch CH3COOH 0,01M ( độ điện li \(\alpha=4,25\%\))
HELP ME !!!!!
Trộn 100ml NaOH 0,01M với 150ml dd Ba(OH)2 0,01M . Tính pH của dung dịch sau khi trộn
$n_{NaOH} = 0,001(mol)$
$n_{Ba(OH)_2} = 0,01.0,15 = 0,0015(mol)$
$NaOH \to Na^+ + OH^-$
$Ba(OH)_2 \to Ba^{2+} + 2OH^-$
Ta có :
$n_{OH^-}= 0,001 + 0,0015.2 = 0,004(mol)$
$V_{dd} = 0,1 + 0,15 = 0,25(mol)$
$[OH^-] = \dfrac{0,004}{0,25} = 0,016M$
$pOH = -log(0,016) = 1,795 \Rightarrow pH = 14 - 1,795 = 12,205$
Đúng 3
Bình luận (1)
\(n_{OH^-}=0,1.0,01+0,15.0,01.2=0,004\left(mol\right)\\ V_{ddsau}=100+150=250\left(ml\right)=0,25\left(l\right)\\ \Rightarrow\left[OH^-\right]=\dfrac{0,004}{0,25}=0,016\left(M\right)\\ pH=14+log\left[0,016\right]\approx12,204\)
Đúng 1
Bình luận (0)
Giúp mình câu này với. Tính pH của các dung dịch sau: a. Dung dịch H2so5 0,01M b. Dung dịch ca(oH)2 0,03M
a) \(\left[H^+\right]=0,01.2=0,02M\)
=> pH = 1,7
b) \(\left[OH^-\right]=0,03.2=0,06M\)
=> pOH= 1,22
=> \(pH=14-1,22=12,78\)
Đúng 2
Bình luận (0)
a) pH= -log[H+]= -log[0,01.2]=1,69
b) pH= 14 - pOH= 14 + log[OH-]= 14+ log[0,03.2]=12,78
Đúng 0
Bình luận (0)
A là dung dịch HCl 0,01M ; B là dung dịch hỗn hợp gồm NaOH 0,01M và Ba(OH)2 0,015M .
a/ Hãy tính pH của dung dịch A và pH của dung dịch B .
b/ Hãy tính pH của dung dịch thu được khi trộn 300ml dung dịch A với 100 ml dung dịch B .
HELP ME !!!!!
Rót từ từ 10ml dung dịch H2SO4 0,01M vào 20ml dung dịch 0,005M. Tính pH của dung dịch a) viết phương trình hóa học của phản ứng đã xảy ra trong thí nghiệm trê b) tính nồng độ mol của các chất sau phản ứng c) Tính pH của dung dịch d) Nhúng quỳ tím vào lọ hóa chất sau phản ứng có hiện tượng gì xảy ra
















