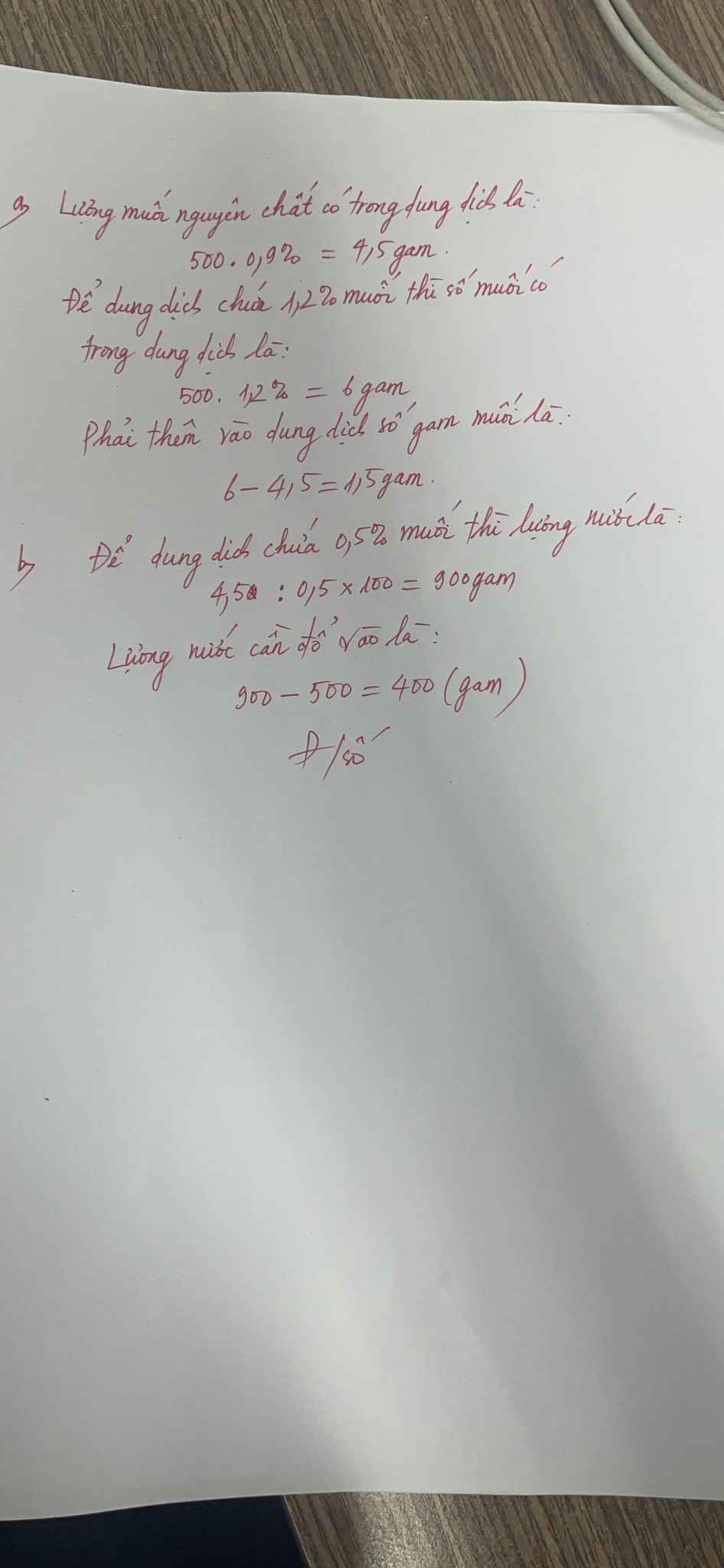Có 1000g dung dịch Nacl 0.3%. Để có nước muối sinh lí 0.9%, em hãy tính xem cần thêm vào bao nhiêu gam muối dung dịch nguyên chất ? ( làm tròn đến chữ số thập phân thứ nhất )

Những câu hỏi liên quan
Bài 6. Một bình đựng 500g dung dịch nước muối 0.9%. Hỏi:
a) Phải cho thêm bao nhiêu gam muối để được dung dịch muối 1.2%?
b) Phải cho thêm bao nhiêu gam nước nguyên chất để được dung dịch nước muối 0.5%?
nước muối sinh lí là dung dịch nacl 0,9% có tính ưu trương, có tác dụng sát trùng, diệt khuẩn, được dùng làm nước xúc miệng tại nhiều gia đình. cần bao nhiêu gam muối ăn để pha chế được 2kg ( khoảng 2 lít) nước muối sinh lý
\(m_{NaCl}=\dfrac{2000.0,9}{100}=18\left(g\right)\)
Đúng 3
Bình luận (0)
Biết rằng trong 500 g dung dịch nước muối chứ 150 g muối nguyên chất. Hỏi cần phải thêm vào dung dịch đó bao nhiêu gam nước để dung dịch đó có nồng độ là \(20\% \)?
Gọi số gam nước cần thêm vào để được dung dịch muối có nồng độ \(20\% \) là \(x\) (gam). Điều kiện \(x > 0\).
Vì ban đầu dung dịch có khối lượng 500 g nên khi thêm \(x\) g nước vào dung dịch thì được dung dịch mới có nồng độ mới là \(x + 500\) g.
Vì nồng độ dung dịch mới là \(20\% \) nên ta có phương trình:
\(\frac{{150}}{{x + 500}}.100 = 20\)
\(\frac{{150}}{{x + 500}} = 20:100\)
\(\frac{{150}}{{x + 500}} = 0,2\)
\(150 = 0,2\left( {x + 500} \right)\)
\(150 = 0,2x + 100\)
\(0,2x = 150 - 100\)
\(0,2x = 50\)
\(x = 50:0,2\)
\(x = 250\) (thảo mãn điều kiện)
Vậy cần thêm 250 gam nước vào dung dịch ban đầu để được dung dịch mới có nồng độ là \(20\% \).
Đúng 1
Bình luận (0)
Trong 800 gam dung dịch nước muối có 40% là muối.Hỏi cần phải thêm vào dung dịch này bao nhiêu gam muối để có được dung dịch nước muối có 60% là muối?
Giúp em/mình với ạ!!
Em/mình cần trước 6h
(Cần lời giải chi tiết)
Em/mình cảm ơn!
Lời giải:
Lượng muối trong dung dịch ban đầu:
$800\times 40:100=320$ (gam)
Giả sử cần thêm vào đó $x$ gam muối để được dung dịch 60%.
Ta có:
$\frac{320+x}{800+x}=\frac{60}{100}=0,6$
$320+x=0,6\times (800+x)=480+0,6\times x$
$x-0,6\times x=480-320$
$0,4\times x=160$
$x=400$ (gam)
Đúng 0
Bình luận (0)
Trong 800 gam dung dịch nước muối có 40% là muối.Hỏi cần phải thêm vào dung dịch này bao nhiêu gam muối để có được dung dịch nước muối có 60% là muối?
Lời giải:
Giả sử cần thêm vào $x$ gam muối để được dung dịch 60% muối
Lượng muối trong 800 gam dung dịch nước là:
$800\times 40:100=320$ (gam)
Ta có: $(320+x):(800+x)=\frac{60}{100}$
$(320+x):(800+x)=0,6$
$320+x=0,6\times (800+x)$
$320+x=480+0,6\times x$
$x=480+0,6\times x-320=160+0,6\times x$
$x-0,6\times x=160$
$x\times 0,4=160$
$x=160:0,4=400$
Vậy cần thêm vào 400 gam muối.
Đúng 1
Bình luận (0)
Một bình đựng 500g dung dịch nước muối 0,9%. Hỏi:
a) Phải cho thêm bao nhiêu gam muối để được dung dịch nước muối 1,2%?
b) Phải cho thêm bao nhiêu gam nước nguyên chất để được dung dịch nước muối 0,5%?
Có ai đó giúp e nhanh với ạ
Hoà tan 100g muối vào 1000g nước ta sẽ thu được một dung dịch nước muối. Như vậy muối chiếm … % trong dung dịch nước muối. (lấy kết quả có 2 chữ số ở phần thập phân)
Khối lượng dung dịch nước muối:
1000 + 100 = 1100 (gam)
Muối chiếm :
100/1100 x 100 = 9,09(%)
Đúng 0
Bình luận (0)
Bài 4. Hòa tan 7,1 gam Na2SO4 ; 7,45 gam KCl ; 2,925 gam NaCl vào nước để được 1 lít dung dịch A.
Tính nồng độ mol/lít của mỗi ion trong dung dịch A.
Cần dùng bao nhiêu mol NaCl và bao nhiêu mol K2SO4 để pha thành 400 ml dung dịch muối có nồng độ ion như trong dung dịch A.
Có thể dùng 2 muối KCl và Na2SO4 để pha thành 400 ml dung dịch muối có nồng độ ion như dung dịch A được không?
Câu 90) hoà tan 5g NaCl vào 120ml nước,ta có dung dịch X. cần phải pha thêm bao nhiêu gam muối trên vào dung dịch X để có dung dịch mới nồng độ 10%:A. 6,83g b. 4,5g c. 9g d. 8,33gcâu 91: người ta dùng quặng boxit (hàm lượng Al2O3 trong quặng là 40%) để sản xuất Al theo phương trình phản ứng sau : 2Al2O3 ---dienphan----- 4Al + 3O2 . Để có được 4 tấn Al nguyên chất cần m quặng là bao nhiêu?( biết %H của quá trình sản xuất là 90%).A. 21 tấn B. 20,8 tấn ...
Đọc tiếp
Câu 90) hoà tan 5g NaCl vào 120ml nước,ta có dung dịch X. cần phải pha thêm bao nhiêu gam muối trên vào dung dịch X để có dung dịch mới nồng độ 10%:
A. 6,83g b. 4,5g c. 9g d. 8,33g
câu 91: người ta dùng quặng boxit (hàm lượng Al2O3 trong quặng là 40%) để sản xuất Al theo phương trình phản ứng sau : 2Al2O3 ---dienphan-----> 4Al + 3O2 . Để có được 4 tấn Al nguyên chất cần m quặng là bao nhiêu?( biết %H của quá trình sản xuất là 90%).
A. 21 tấn B. 20,8 tấn C. 20,975 tấn D. 20,9 tấn
Câu 97) một oxit sắt có thành phần là 7 phần khối lượng sắt kết hợp với 3 phần khối lượng oxi. công thức hoá học đơn giản của oxit sắt là công thức nào sau đây:
A. FeO2 B. Fe3O4 C. FeO D. Fe2O3
\(2Al_2O_3 \xrightarrow{đp} 4Al + 3O_2\\ m_{Al} = 4000(kg)\\ n_{Al} = \dfrac{4000}{27}(kmol)\\ \Rightarrow n_{Al_2O_3\ pư} = \dfrac{1}{2}n_{Al} = \dfrac{2000}{27}(kmol)\\ \Rightarrow m_{Al_2O_3\ đã\ dùng} = (\dfrac{2000}{27}.102) : 90\% = \dfrac{680 000}{81}(kg)\\ \Rightarrow m_{quặng} = \dfrac{680 000}{81} : 40\% = 20987(kg) ≃21(tấn)\)
Đáp án A
Đúng 1
Bình luận (0)
Câu 90 :
$d_{H_2O} = 1(g/ml) \to m_{H_2O} = 1.120 = 120(gam)$
Gọi $m_{NaCl\ cần\ thêm} = a(gam)$
Sau khi thêm :
$m_{dd} = 5 + 120 + a = 125 + a(gam)$
$m_{NaCl} = 5 + a(gam)$
Ta có :
$C\%_{NaCl} = \dfrac{5 + a}{125 + a}.100\% = 10\%$
$\Rightarrow a = 8,33(gam)$
Đáp án D
Đúng 1
Bình luận (0)
Câu 97 :
Gọi CTHH là $Fe_xO_y$
Ta có :
\(\dfrac{56x}{7} = \dfrac{16y}{3}\\ \Rightarrow \dfrac{x}{y} = \dfrac{7.16}{56.3} = \dfrac{2}{3}\)
Với x = 2 ; y = 3 thì thỏa mãn
Vậy oxit là $Fe_2O_3$
Đáp án D
Đúng 1
Bình luận (0)




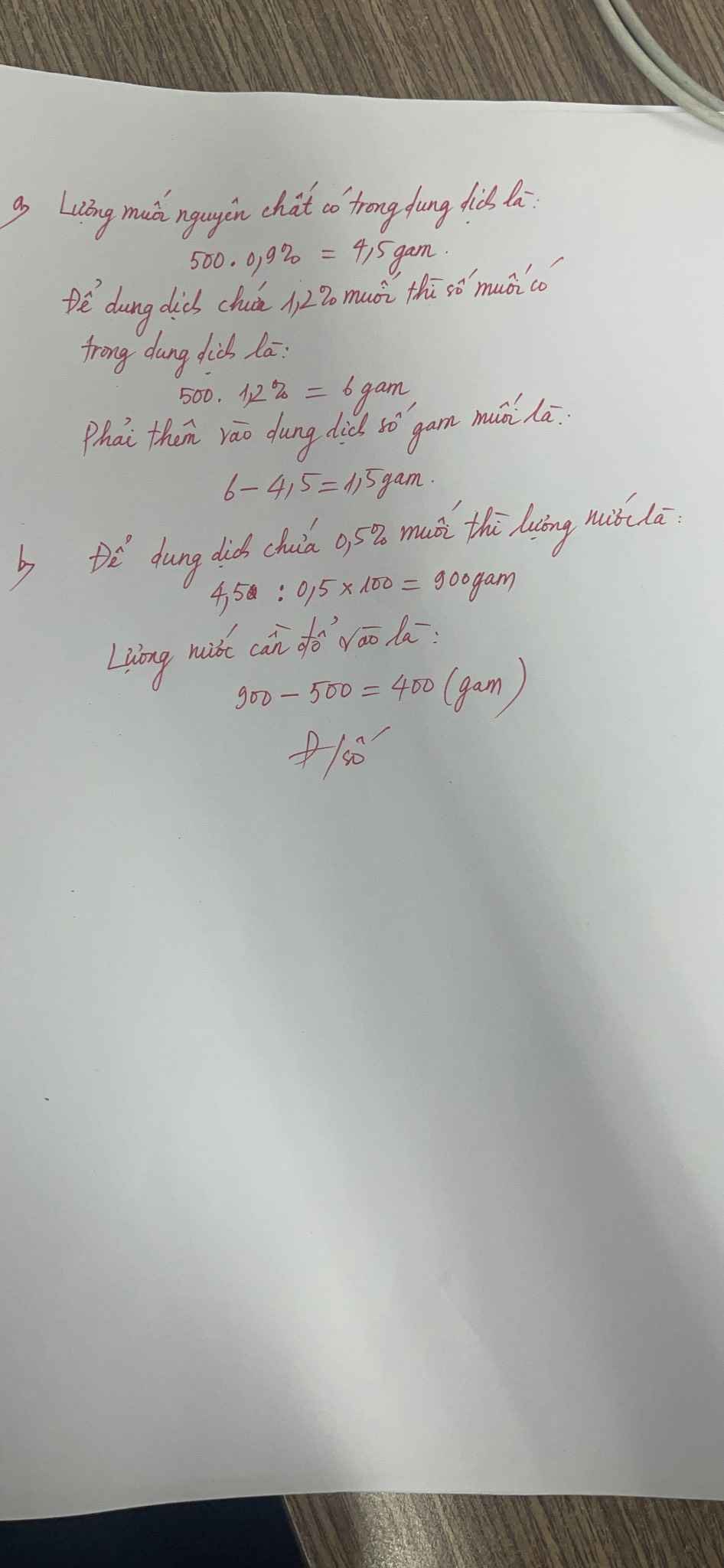 nếu sai thì con mình xin lỗi nhé
nếu sai thì con mình xin lỗi nhé