: Cho 9,1 gam bột kim loại kẽm tác dụng vừa đủ với dung dịch CuSO4 20% có khối lượng riêng là 1,12 g/ml
a) Tính khối lượng kim loại đồng được tạo thành sau phản ứng.
b) Tính thể tích dung dịch CuSO420% đã dùng
12./ Cho 3,92 gam bột sắt vào 200ml dung dịch CuSO4 10% ( D= 1,12 g/ml ) .
a. Tính khối lượng kim loại mới tạo thành
b. Tính nồng độ mol của dung dịch sau phản ứng ( giả sử thể tích dung dịch thay đổi không đáng kể
Ta có: \(n_{Fe}=\dfrac{3,92}{56}=0,07\left(mol\right)\)
\(PTHH:Fe+CuSO_4--->FeSO_4+Cu\downarrow\)
a. Theo PT: \(n_{Cu}=n_{FeSO_4}=n_{Fe}=0,07\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,07.64=4,48\left(g\right)\)
Ta có: \(V_{dd_{FeSO_4}}=V_{dd_{CuSO_4}}=\dfrac{200}{1000}=0,2\left(lít\right)\)
\(\Rightarrow C_{M_{FeSO_4}}=\dfrac{0,07}{0,2}=0,35M\)
Cho 1,12 gam bột Fe và 0,24 gam bột Mg tác dụng với 250 ml dung dịch CuSO 4 , khuấy nhẹ cho đến hết màu xanh, nhận thấy khối lượng kim loại sau phản ứng là 1,76 gam. Nồng độ đung dịch CuSO 4 trước phản ứng là
A. 0,01 M
B. 0,02M
C, 0,03M
D. 0,04M
Đáp án D
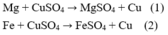
Nhận xét: khi cho bột kim loại vào dung dịch, khối lượng kim loại sau phản ứng sẽ tăng lên.
Ta có khoảng sau:
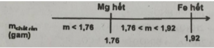

Cho một hỗn hợp gồm có 1,12 gam Fe và 0,48 gam Mg tác dụng với 500 mL dung dịch CuSO4. Phản ứng thực hiện xong, người ta thu được kim loại có khối lượng 2,44 gam. Tính nồng độ mol của dung dịch CuSO4 đã dùng
A. 0,020 M
B. 0,050 M
C. 0,025 M
D. 0,080 M
Cho 2,4 gam kim loại Mg tác dụng vừa đủ với dung dịch H2SO4 4,9%.
a) Tính khối lượng dung dịch H2SO4 đã dùng.
b) Dung dịch thu được sau phản ứng có nồng độ là bao nhiêu?
c) Dẫn lượng khí thu được sau phản ứng qua 20 gam bột đồng (II) oxit ở 400°C thu được 3,2 gam chất rắn màu đỏ. Tính hiệu suất của phản ứng.
a) \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,1---->0,1------->0,1---->0,1
=> \(m_{dd.H_2SO_4}=\dfrac{0,1.98}{4,9\%}=200\left(g\right)\)
b) mdd sau pư = 2,4 + 200 - 0,1.2 = 202,2 (g)
mMgSO4 = 0,1.120 = 12 (g)
\(C\%_{MgSO_4}=\dfrac{12}{202,2}.100\%=5,9\%\)
c)
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,25}{1}>\dfrac{0,1}{1}\) => Hiệu suất tính theo H2
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,05<-----0,05
=> \(H=\dfrac{0,05}{0,1}.100\%=50\%\)
a, \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PTHH: Mg + H2SO4 ---> MgSO4 + H2
0,1--->0,1---------->0,1-------->0,1
\(m_{dd\left(H_2SO_4\right)}=\dfrac{0,1.98}{4,9\%}=200\left(g\right)\)
b, \(m_{dd\left(sau.pư\right)}=2,4+200-0,2.2=202,2\left(g\right)\)
\(\rightarrow C\%_{MgSO_4}=\dfrac{0,1.120}{202,2}.100\%=5,93\%\)
c, \(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
LTL: 0,25 > 0,1 => CuO dư
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
Theo pt: \(n_{H_2}=n_{Cu}=0,05\left(mol\right)\)
=> \(H=\dfrac{0,05}{0,1}.100\%=50\%\)
Cho một hỗn hợp gồm có 1,12 gam Fe và 0,24 gam Mg tác dụng với 250 ml dung dịch CuSO4. Phản ứng thực hiện xong, người ta thu được kim loại có khối lượng là 1,88 gam. Tính nồng độ mol của dung dịch đã dùng.
A. 0,1M
B. 0,12M
C. 0,2M
D. 0,05M
Đáp án A
Phương trình hóa học:
Mg + CuSO4 → MgSO4 + Cu (1)
Fe + CuSO4 → FeSO4 + Cu (2)
Có: nMg = 0,01 mol và nFe = 0,02 mol
Theo (1) và (2), nếu Mg và Fe phản ứng hết thì thu được 0,03 mol Cu.
Khối lượng kim loại thu được sau phản ứng là:
0,03 .64 = 1,92 (gam)
Thực tế chỉ thu được 1,88 gam kim loại. Chứng tỏ kim loại đã cho không phản ứng hết.
Mg có tính khử mạnh hơn Fe nên phản ứng trước.
Lượng Cu sinh ra ở (1) là 0,01 mol tương ứng với khối lượng 0,64 (gam)
Khối lượng Fe dư và Cu sinh ra ở (2) là: 1,88 – 0,64 = 1,24 (gam)
Đặt khối lượng Fe tham gia ở (2) là x, khối lượng sắt dư là (1,12 – 56x) và khối lượng Cu sinh ra ở (2) là 64x.
Ta có: (1,12-56x) + 64x = 1,24 => x = 0,015
Lượng CuSO4 trong 250 ml dung dịch đã phản ứng hết:
0,015 + 0,01 = 0,025(mol)
Nồng độ mol của dung dịch đã dùng là : 0,025/0,25 = 0,1mol/l
Cho 1,68 gam bột sắt và 0,36 gam Mg tác dụng với 375 ml dung dịch CuSO 4 khuấy nhẹ cho đến khi dung dịch mất màu xanh, thấy khối lượng kim loại thu được sau phản ứng là 2,82 gam. Nồng độ mol/l của CuSO4 trong dung dịch trước phản ứng là
A. 0,15M
B. 0,2M
C. 0,1M
D. 0,05M
Bài 4:
4Na + O2 → 2Na2O
nNa = \(\dfrac{4,6}{23}\)= 0,2 mol , nO2 = \(\dfrac{2,24}{22,4}\)= 0,1 mol
\(\dfrac{nNa}{4}\)<\(\dfrac{nO_2}{1}\)=> Sau phản ứng oxi dư , nO2 phản ứng = \(\dfrac{nNa}{4}\)= 0,05 mol
=> nO2 dư = 0,1 - 0,05 = 0,05 mol <=> mO2 dư = 0,05.32= 1,6 gam
a) nNa2O = 1/2 nNa = 0,1 mol
=> mNa2O = 0,1. 62 = 6,2 gam
Bài 1:
Zn + 2HCl → ZnCl2 + H2
a) nZn = \(\dfrac{6,5}{65}\)= 0,1 mol , nHCl = \(\dfrac{3,65}{36,5}\)= 0,1 mol
Ta có \(\dfrac{nZn}{1}\)> \(\dfrac{nHCl}{2}\)=> Zn dư , HCl phản ứng hết
nZnCl2 = \(\dfrac{nHCl}{2}\)= 0,5 mol => mZnCl2 = 0,5. 136 = 68 gam
b) nH2 = \(\dfrac{nHCl}{2}\) = 0,5 mol => V H2 = 0,5.22,4 = 11,2 lít
Bài 2:
Fe + CuSO4 → FeSO4 + Cu
nFe = \(\dfrac{11,2}{56}\)= 0,2 mol , nCuSO4 = \(\dfrac{40}{160}\)= 0,25 mol
Ta thấy nFe < nCuSO4 => Fe phản ứng hết , CuSO4 dư
nCu = nFe = 0,2 mol <=> mCu = 0,2.64 = 12,8 gam
Bài 3:
2H2 + O2 → 2H2O
nH2 = \(\dfrac{2,24}{22,4}\)= 0,1 mol , nO2 = \(\dfrac{4,48}{22,4}\)= 0,2 mol
\(\dfrac{nH_2}{2}\)< \(\dfrac{nO_2}{1}\) => sau phản ứng oxi dư , nO2 phản ứng = \(\dfrac{nH_2}{2}\)= 0,05 mol
nO2 dư = nO2 ban đầu - nO2 phản ứng = 0,2 - 0,05 = 0,15 mol
=>V O2 dư = 0,15.22,4 = 3,36 lít
Mong mọi người giúp em , em đang ôn lại các dạng bài để thi học kì , còn vài ngày nữa thi rồi nên mong mọi người giải đáp giúp em ạ , em cảm ơn nhiều :">
Câu 1 : Cho 10g hỗn hợp 2 kim loại : Al và Cu tác dụng với dung dịch H2SO4 20% thu được 6.72 lít khi H2 ( ĐKTC)
a) Tính khối lượng các chất có trong hỗn hợp
b) Tình khối lượng H2S04 cần dùng
Câu 2 : Cho 20g hỗn hợp 2 muối là NaCl và Na2CO3 tác dụng vừa đủ với 400 Ml dung dịch HCl
a) Tính nồng độ mol của dung dịch HCl
b) Tính phần trâm theo khối lượng của mỗi muối trong hỗn hợp ban đầu
Câu 3 : Một sợi dây Al có khối lượn là 16,2g được nhúng vào dung dịch CuSO4 25%
a) Khối lượng dung dịch CuSO4 25% dùng đẻ làm tan hết sợi Al
b) Khối lượng Cu tạo thành sau phản ứng
Câu 4 : Cho 200g dung dịch BaCl2 10,4% tác dụng vừa đủ với 400g dung dịch Na2SO4
a) Khối lượng kết tủa tạo thành
b) Nồng độ % của chất còn lại trong dung dịch sau khi lọc bỏ kết tủa
Câu 5 : Cho 200 ml dung dihcj AgNO3 ; 2M tác dụng vừa đủ
a) Hiện tượng quan sát được ? PT ?
b) Khối lượng chất rắn sinh ra
c) Nồng độ mol của dung dịch sau phản ứng
Câu 6 : Cho bột săt dư tác dụng với 100g ml dung dịch CuSO4 1M . Sau khi phản ứng kết thúc , lọc được chất rắn A và dung dịch B
a) Cho A tác dụng với dung dịch HCl dư . Tính khối lượng chất rắn còn lại sau phản ứng
b) Khối lượng dung dịch NaOH 20% vừa đủ đẻ kết tủa hoàn toàn dung dịch B
Câu 1:
PTHH: 2Al + 3H2SO4 ===> Al2(SO4)3 + 3H2
a)Vì Cu không phản ứng với H2SO4 loãng nên 6,72 lít khí là sản phẩm của Al tác dụng với H2SO4
=> nH2 = 6,72 / 22,4 = 0,2 (mol)
=> nAl = 0,2 (mol)
=> mAl = 0,2 x 27 = 5,4 gam
=> mCu = 10 - 5,4 = 4,6 gam
b) nH2SO4 = nH2 = 0,3 mol
=> mH2SO4 = 0,3 x 98 = 29,4 gam
=> Khối lượng dung dịch H2SO4 20% cần dùng là:
mdung dịch H2SO4 20% = \(\frac{29,4.100}{20}=147\left(gam\right)\)
nH2 = 6.72 : 22.4 = 0.3 mol
Cu không tác dụng với H2SO4
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
0.2 <- 0.3 <- 0.1 <- 0.3 ( mol )
mAl = 0.2 x 56 = 5.4 (g)
mCu = 10 - 5.4 = 4.6 (g )
mH2SO4 = 0.3 x 98 = 29.4 ( g)
mH2SO4 20% = ( 29.4 x100 ) : 20 = 147 (g)
3, \(n_{Al}=\dfrac{16,2}{27}=0,6\left(mol\right)\)
2Al + 3CuSO4 \(\rightarrow\) Al2(SO4)3 + 3Cu
de: 0,6 \(\rightarrow\) 0,9 \(\rightarrow\) 0,9
\(m_{CuSO_4}=0,9.160=144g\)
a, \(m_{ddCuSO_4}=\dfrac{144.100}{25}=576g\)
b, \(m_{Cu}=0,9.64=57,6g\)
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.

Bảo toàn nguyên tố M: nMSO4 = 0,25mol
Bảo toàn nguyên tố Cu: nCuSO4 dư = 0,1 mol
=> M = 24 (Mg)
b.
