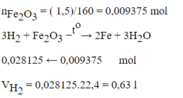dùng 4,48l khí h2(ở đktc) khử hoàn toàn 43,4 g oxit mo hãy tìm ct của oxit đó

Những câu hỏi liên quan
Khử hoàn toàn 24g hh oxit CuO và FexOy bằng H2 thu được 17,6g 2 kim loại cho hoàn toàn bộ 2 kim loại vào ddHCl dư thu được 4,48l khí H2 ở đktc . Xác định CT của oxi sắt
Gọi số mol CuO, FexOy là a, b (mol)
=> 80a + (56x + 16y)b = 24 (1)
PTHH: CuO + H2 --to--> Cu + H2O
a--------------->a
FexOy + yH2 --to--> xFe + yH2O
b----------------->bx
=> 64a + 56bx = 17,6 (2)
PTHH: Fe + 2HCl --> FeCl2 + H2
bx------------------->bx
=> bx = \(\dfrac{4,48}{22,4}=0,2\) (3)
(2)(3) => a = 0,1 (mol)
(1) => 56bx +16by = 16
=> by = 0,3 (mol)
=> \(\dfrac{bx}{by}=\dfrac{0,2}{0,3}\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH: Fe2O3
Đúng 3
Bình luận (5)
Khử 3,48(g) một oxit kim loại M cần dùng 1,334(l) khí H2 ở đktc, toàn bộ lượng kim loại thu được tác dụng vơi dung dịch HCl cho 1,008(l) khí H2 ở đktc. Tìm kim loại M và oxit của nó.
Để khử hoàn toàn 2,32 gam một oxit kim loại, cần dùng 0,896 lít khí H 2 ở đktc. Kim loại đó là
A. Mg.
B. Cu.
C. Fe.
D. Cr.
Để khử hoàn toàn 2,32 gam một oxit kim loại, cần dùng 0,896 lít khí
H
2
ở đktc. Oxit kim loại là A. MgO. B. CuO. C.
F
e
3
O
4
. D.
C
r
2
O
3
.
Đọc tiếp
Để khử hoàn toàn 2,32 gam một oxit kim loại, cần dùng 0,896 lít khí H 2 ở đktc. Oxit kim loại là
A. MgO.
B. CuO.
C. F e 3 O 4 .
D. C r 2 O 3 .
Khử hoàn toàn 1,5 g sắt (III) oxit bằng khí H 2 . Thể tích khí hidro (đktc) cần dùng là
A. 2,34 l
B. 1,2 l
C. 0,63 l
D. 0,21 l
Khử hoàn toàn 3,2 g oxit sắt (FexOy) cần dùng vừa đủ 13,44 lit khí H2 (đktc) . Xác định công thức FexOy
Sửa: \(32g\) oxit sắt
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6(mol)\\ PTHH:Fe_xO_y+yH_2\to xFe+yH_2O\\ \Rightarrow y.n_{Fe_xO_y}=n_{H_2}=0,6(mol)\\ \Rightarrow \dfrac{32y}{56x+16y}=0,6\\ \Rightarrow 32y=33,6x+9,6y\\ \Rightarrow 33,6x=22,4y\\ \Rightarrow \dfrac{x}{y}=\dfrac{22,4}{33,6}=\dfrac{2}{3}\\ \Rightarrow x=2;y=3\)
Vậy CTHH là \(Fe_2O_3\)
Đúng 2
Bình luận (0)
dùng khí h2 vừa đủ để khử hoàn toàn 34,8g một oxit sắt ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được 25,2g sắt, làm lạnh hơi nước thu được sau phản ứng. a. tính thể tích khí H2 đã phản ứng ở đktc b. xác định CTHH của oxit sắt đó c. tính thể tích nước thu đc ở thể lỏng ( giải thích các bước làm )
a) \(n_O=\dfrac{34,8-25,2}{16}=0,6\left(mol\right)\)
=> \(n_{H_2O}=0,6\left(mol\right)\) (bảo toàn O)
=> \(n_{H_2}=0,6\left(mol\right)\) (bảo toàn H)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b) \(n_{Fe}=\dfrac{25,2}{56}=0,45\left(mol\right)\)
nFe : nO = 0,45 : 0,6 = 3 : 4
=> CTHH: Fe3O4
c) \(m_{H_2O}=0,6.18=10,8\left(g\right)\)
Mà \(d_{H_2O}=1\left(g/ml\right)\)
=> \(V_{H_2O}=10,8\left(ml\right)\)
Đúng 2
Bình luận (0)
Khử hoàn toàn 3,48g một oxit của kim loại R cần dùng vừa đủ 1,344 lít khí H2 (đktc). Toàn bộ khối lượng KL thu được tác dụng với dung dịch HCl dư thì thu được 1,008 lít khí H2(đktc)
Tìm R và oxit của R
Ta có : + H2 --> H2O
0,06-----0,06
--> m(R) = 3,48 - 0,06.16 = 2,52 gam
--> \(\frac{2,25n}{M}=\frac{1,008}{22,4}\)(n là hoá trị của R)
--> 28.n = M
--> n = 2 --> M = 56 (Fe)
nFe : nO = 0,045 : 0,06 = 3 : 4 --> oxit là :
Đúng 0
Bình luận (0)
một hỗn hợp z gồm 2 este RCOOR' và R1COOR'' .cứ 0.74g hỗn hợp z phản ứng vừa hết với 7 g dung dịch KOH 8% thu đc hai muối và 2 rượu .trong hỗn hợp hai rượu thì rượu etylic chiếm 1/3 tổng số mol của hai rượụ .tìm công thức cấu tạo và thành phần % theo khối lượng của mỗi este trong hỗn hợp z
Đúng 0
Bình luận (0)
Khử hoàn toàn 11,6g một oxit sắt (FexOy) bằng khí H2 ở to cao thu được 8,4g sắt kim loại. Xác định CTHH của oxit sắt và tính VH2 (đktc) đã dùng
chỉ mik với các bn
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\ n_O=\dfrac{11,6-0,15}{16}=0,2\left(mol\right)\)
CTHH: FexOy
\(\rightarrow x:y=n_{Fe}:n_O=0,15:0,2=3:4\)
CTHH: Fe3O4
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
0,2 0,15
=> VH2 = 0,2.22,4 = 4,48 (l)
Đúng 3
Bình luận (1)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
\(n_{Fe_xO_y}=\dfrac{11,6}{56x+16y}\) mol
\(Fe_xO_y+yH_2\rightarrow\left(t^p\right)xFe+yH_2O\)
\(\dfrac{11,6}{56x+16y}\) \(\dfrac{11,6x}{56x+16y}\) ( mol )
\(\Rightarrow\dfrac{11,6x}{56x+16y}=0,15\)
\(\Leftrightarrow11,6x=8,4x+2,4y\)
\(\Leftrightarrow3,2x=2,4y\)
\(\Leftrightarrow4x=3y\)
\(\Leftrightarrow x=3;y=4\)
\(\Rightarrow CTHH:Fe_3O_4\)
\(\Rightarrow n_{H_2}=0,15.4:3=0,2mol\)
\(V_{H_2}=0,2.22,4=4,48l\)
Đúng 2
Bình luận (1)