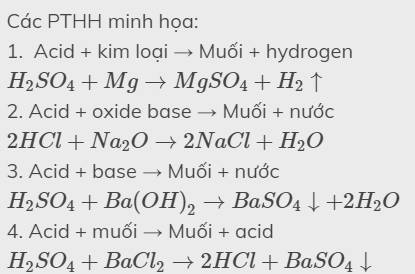Vẽ mũi tên thể hiện mối quan hệ của Acid với các hợp chất khác, Từ đó rút ra nhận xét về mối quan hệ giữa chúng. Viết PTHH minh họa Acid+.......→Muối +hydrogen Acid+.......→Muối + Nước Acid+.......→ Muối + Nước Acid +......→Muối + Acid

Những câu hỏi liên quan
Acid+....... → Muối +hydrogen Acid+....... → Muối + Nước Acid+.......→ Muối + NƯỚC Acid+......→Muối + Acid
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản.
13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối...
Đọc tiếp
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản.
13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối đó.
14. Dung dịch đệm là gì? Cấu trúc của dung dịch đệm? Tính pH của dung dịch đệm? Ứng dụng của dung dịch đệm.
giúp với các bạn?
Mối quan hệ giữa cấu tạo và vai trò của các phân tử sinh học: protein, nucleic acid?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản.
13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối đó
. 14. Dung dịch đệm là gì? Cấu trúc của dung dịch đệm? Tính pH của dung dịch đệm? Ứng dụng của dung dịch đẹm?
Đọc tiếp
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản.
13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối đó
. 14. Dung dịch đệm là gì? Cấu trúc của dung dịch đệm? Tính pH của dung dịch đệm? Ứng dụng của dung dịch đẹm?
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giú...
Đọc tiếp
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giúp với ạ các bạn........
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giả...
Đọc tiếp
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giải giúp mình vơi ạ
Tìm hiểu về các phản ứng tạo muốiBảng 11.1. Phản ứng tạo thành muối, tên gọi và thành phần phân tử của một số muốiQuan sát Bảng 11.1 và thực hiện các yêu cầu:1. Nhận xét về sự khác nhau giữa thành phần phân tử của acid (chất phản ứng) và muối (chất sản phẩm). Đặc điểm chung của các phản ứng ở Bảng 11.1 là gì?2. Nhận xét về cách gọi tên muối.
Đọc tiếp
Tìm hiểu về các phản ứng tạo muối
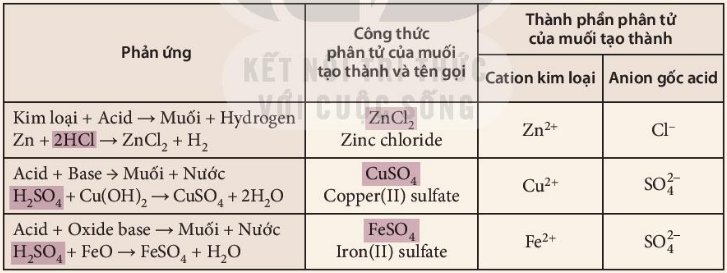
Bảng 11.1. Phản ứng tạo thành muối, tên gọi và thành phần phân tử của một số muối
Quan sát Bảng 11.1 và thực hiện các yêu cầu:
1. Nhận xét về sự khác nhau giữa thành phần phân tử của acid (chất phản ứng) và muối (chất sản phẩm). Đặc điểm chung của các phản ứng ở Bảng 11.1 là gì?
2. Nhận xét về cách gọi tên muối.
1. Điểm khác nhau giữa thành phần phân tử của acid (chất phản ứng) và muối (chất sản phẩm) là phần tử mang điện dương (cation). (Cation kim loại ở muối và cation H+ ở acid)
Điểm chung của các phản ứng ở Bảng 11.1 là đều có sự thay thế ion H+ của acid bằng ion kim loại.
2. Cách gọi tên muối gồm có cation kim loại và anion gốc acid:
Tên kim loại (hoá trị, đối với kim loại có nhiều hoá trị) + tên gốc acid.
Đúng 1
Bình luận (0)
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản.
13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối đó.
14. Dung dịch đệm là gì? Cấu trúc của dung dịch đệm? Tính pH của dung dịch đệm? Ứng dụng của dung dịch đệm
giúp mọi người nhé..................
Đọc tiếp
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản.
13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối đó.
14. Dung dịch đệm là gì? Cấu trúc của dung dịch đệm? Tính pH của dung dịch đệm? Ứng dụng của dung dịch đệm
giúp mọi người nhé..................
Cho 2,7 gam aluminium tác dụng với acid sunfuric acid a a.Viết PTHH b.Tính khối lượng muối tạo thành c.Nếu dùng thể tích khí hydrogen sinh ra để khử 23,2 gam Fe³O⁴ tính khối lượng kim loại thứ được help mình với
Đề sai:
Sửa lại:
Cho 2,7 gam aluminium tác dụng với acid sunfuric acid a a.Viết PTHH b.Tính khối lượng muối tạo thành c.Nếu dùng thể tích khí hydrogen sinh ra để khử 23,2 gam Fe3O4 tính khối lượng kim loại thu được
Đúng 0
Bình luận (0)
a, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,05\left(mol\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\)
Ta có: \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
PT: \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,15}{4}\), ta được Fe3O4 dư.
Theo PT: \(n_{Fe}=\dfrac{3}{4}n_{H_2}=0,1125\left(mol\right)\Rightarrow m_{Fe}=0,1125.56=6,3\left(g\right)\)
Đúng 0
Bình luận (0)