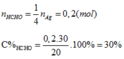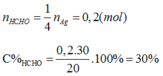Formaldehyde là chất khí không màu, có mùi hắc và gây khó chịu. Dung dịch trong nước chứa khoảng 37% formaldehyde gọi là formalin. Hãy tìm hiểu ứng dụng của formalin sử dụng trong sinh học

Những câu hỏi liên quan
Bài 2: Có những chất sau: CuO, Fe(OH)3, Cu, Al, Al2O3, K2SO3. Hãy chọn một trong những chất trên tác dụng với dung dịch H2SO4 loãng để sinh ra:a. Dung dịch màu xanh lamb. Dung dịch màu vàng nâuc. Khí mùi hắc, nặng hơn không khíd. Khí nhẹ hơn không khí, cháy được trong không khíe. Dung dịch không màuBài 3: Cần bao nhiêu lit dd HCl 1,2M để hòa tan hoàn toàn 4,8 gam đồng (II) oxit
Đọc tiếp
Bài 2: Có những chất sau: CuO, Fe(OH)3, Cu, Al, Al2O3, K2SO3. Hãy chọn một trong những chất trên tác dụng với dung dịch H2SO4 loãng để sinh ra:
a. Dung dịch màu xanh lam
b. Dung dịch màu vàng nâu
c. Khí mùi hắc, nặng hơn không khí
d. Khí nhẹ hơn không khí, cháy được trong không khí
e. Dung dịch không màu
Bài 3: Cần bao nhiêu lit dd HCl 1,2M để hòa tan hoàn toàn 4,8 gam đồng (II) oxit
Bài 2 :
a) Dung dịch màu xanh lam :
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
b) Dung dịch màu vàng nâu :
\(2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)
c) Khí nhẹ hơn không khí , cháy được trong không khí :
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
d) Dung dịch không màu :
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Chúc bạn học tốt
Đúng 3
Bình luận (1)
Bài 3 :
\(n_{CuO}=\dfrac{4,8}{80}=0,06\left(mol\right)\)
Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O|\)
1 2 1 1
0,06 0,12
\(n_{HCl}=\dfrac{0,06.2}{1}=0,12\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0,12}{1,2}=0,1\left(l\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
1. Có những chất sau: CuO, Na2SO3, Al2O3, Mg.
Hãy cho biết chất nào tác dụng được với dd HCl sinh ra:
a. Chất khí cháy được trong không khí và nhẹ hơn không khí
b. Dung dịch có màu xanh lam
c. Chất khí nặng hơn không khí và có mùi hắc d. Dung dịch không màu và nước
d. Dung dịch không màu và nước
Viết PTHH minh họa Can gap
a) \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
b) \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
c) \(Na_2SO_3+2HCl\rightarrow2NaCl+H_2O+SO_2\uparrow\)
d) \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Đúng 1
Bình luận (0)
Cho 20 gam dung dịch formalin tác dụng với AgNO3 dư trong NH3 thu được 86,4 gam Ag . Nồng độ phần trăm của dung dịch formalin là A. 20% B. 30% C. 50% D. 60%
Đọc tiếp
Cho 20 gam dung dịch formalin tác dụng với AgNO3 dư trong NH3 thu được 86,4 gam Ag . Nồng độ phần trăm của dung dịch formalin là
A. 20%
B. 30%
C. 50%
D. 60%
Cho 20 gam dung dịch formalin tác dụng với AgNO3 dư trong NH3 thu được 86,4 gam Ag . Nồng độ phần trăm của dung dịch formalin là
A. 20%
B. 30%
C. 50%
D. 60%
Tìm hiểu và trình bày các ứng dụng của formaldehyde, acetaldehyde và acetone.
Formic aldehyde (HCHO) và acetic aldehyde (CH3CHO) là các aldehyde phân tử khối nhỏ có trạng thái khí ở nhiệt độ thường.
Đúng 0
Bình luận (0)
Câu 36: Chất phản ứng được với dung dịch HCl tạo ra một chất khí có mùi hắc, nặng hơn không khí và làm đục nước vôi trong là: A. Zn.B. Na2SO3.C. FeS.D. Na2CO3. Câu 37: Trong sơ đồ phản ứng sau: . Chất X là A. Cu.B. Cu(NO3)2.C. CuO.D. CuSO4. Câu 38: Có 5 kim loại sau: Ba, Mg, Al, Fe, Ag. Chỉ có nước và dung dịch HCl, có thể nhận biết được mấy kim loại? A. 1.B. 2.C. 3.D. 5. Câu 39: Có bốn ống nghiệm đựng các dung dịch: Ba(NO3)2, KOH, HCl và Na2CO3. Dùng hóa chất gì có thể nhận biết được chúng? A....
Đọc tiếp
Câu 36: Chất phản ứng được với dung dịch HCl tạo ra một chất khí có mùi hắc, nặng hơn không khí và làm đục nước vôi trong là:
A. Zn.
B. Na2SO3.
C. FeS.
D. Na2CO3.
Câu 37: Trong sơ đồ phản ứng sau: . Chất X là
A. Cu.
B. Cu(NO3)2.
C. CuO.
D. CuSO4.
Câu 38: Có 5 kim loại sau: Ba, Mg, Al, Fe, Ag. Chỉ có nước và dung dịch HCl, có thể nhận biết được mấy kim loại?
A. 1.
B. 2.
C. 3.
D. 5.
Câu 39: Có bốn ống nghiệm đựng các dung dịch: Ba(NO3)2, KOH, HCl và Na2CO3. Dùng hóa chất gì có thể nhận biết được chúng?
A. Dùng quỳ tím.
B. Dùng phenolphtalein.
C. Dùng dung dịch BaCl2.
D. Dùng acid H2SO4.
Câu 40: Thuốc thử dùng để nhận biết 3 dung dịch: HCl, HNO3, H2SO4 đựng trong 3 lọ khác nhau đã mất nhãn. Các thuốc thử dùng để nhận biết được chúng là:
A. Dung dịch AgNO3 và giấy quì tím.
B. Dung dịch BaCl2 và dung dịch AgNO3.
C. Dùng quì tím và dung dịch NaOH.
D. Dung dịch BaCl2 và dung dịch phenolphtalein.
Giúp mk vớiii ạ, mk cảm ơn trc
Khí H2S tác dụng với dung dịch chứa K2Cr2O7 và H2SO4 tạo nên kết tủa A. Kết tủa này cháy trong O2 tạo nên một khí có mùi khó chịu. Hòa tan khí này vào nước thu được 100 gam dung dịch axit 8,2%. Khối lượng K2Cr2O7 đã tác dụng với H2S là? A. 8,2 gam B. 9,8 gam C. 22,5 gam D. 29,4 gam
Đọc tiếp
Khí H2S tác dụng với dung dịch chứa K2Cr2O7 và H2SO4 tạo nên kết tủa A. Kết tủa này cháy trong O2 tạo nên một khí có mùi khó chịu. Hòa tan khí này vào nước thu được 100 gam dung dịch axit 8,2%. Khối lượng K2Cr2O7 đã tác dụng với H2S là?
A. 8,2 gam
B. 9,8 gam
C. 22,5 gam
D. 29,4 gam
Khí H2S tác dụng với dung dịch chứa K2Cr2O7 và H2SO4 tạo nên kết tủa. Kết tủa này cháy trong O2 tạo nên một khí có mùi khó chịu. Hòa tan khí này vào nước thu được 100 gam dung dịch axit 8,2%. Khối lượng K2Cr2O7 đã tác dụng với H2S là A. 8,2 gam. B. 9,8 gam. C. 22,5 gam. D. 29,4 gam.
Đọc tiếp
Khí H2S tác dụng với dung dịch chứa K2Cr2O7 và H2SO4 tạo nên kết tủa. Kết tủa này cháy trong O2 tạo nên một khí có mùi khó chịu. Hòa tan khí này vào nước thu được 100 gam dung dịch axit 8,2%. Khối lượng K2Cr2O7 đã tác dụng với H2S là
A. 8,2 gam.
B. 9,8 gam.
C. 22,5 gam.
D. 29,4 gam.
Đáp án B
H 2 S ⇒ S ⇒ S O 2 ⇒ H 2 S O 3 n H 2 S = n H 2 S O 3 = 100 . 0 , 082 82 = 0 , 1 B ả o t o à n e 2 n H 2 S = 6 n K 2 C r 2 O 7 ⇒ n K 2 C r 2 O 7 = 0 , 1 3 ⇒ m K 2 C r 2 O 7 = 0 , 1 3 . 294 = 9 , 8 ( g )
Đúng 0
Bình luận (0)
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2. a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí. b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm. -Thể tích khí sunfurơ sinh ra ở đktc. -Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
Đọc tiếp
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2.
a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí.
b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm.
-Thể tích khí sunfurơ sinh ra ở đktc.
-Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
a) Phương trình hóa học S + O2 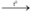 SO2
SO2
b) nS = 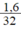 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 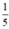 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l
Đúng 1
Bình luận (0)