0,525 mol MgCl2 chứa số nguyên tử Cl là?

Những câu hỏi liên quan
Trong tự nhiên, clo có 2 đồng vị: 35 Cl và 37 Cl . Số nguyên tử 35 Cl có trong 14,244
gam MgCl2 (Mg=24) là \(1.368\cdot10^{23}\). Cho hằng số Avogagro \(N_A=6\cdot10^{23}\). Tính
nguyên tử khối trung bình của clo.
Câu 9: Trong tự nhiên, clo có 2 đồng vị: \(^{35}Cl\) và \(^{37}Cl\) . Số nguyên tử 35Cl có trong 14,244 gam MgCl2 (Mg=24) là \(1,368\cdot10^{23}\). Cho hằng số Avogagro \(N_A=6\cdot10^{23}\). Tính nguyên tử khối trung bình của clo
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng: - Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl. - Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O. - Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O. - Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O. - Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
Đọc tiếp
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng:
- Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl.
- Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O.
- Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O.
- Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O.
- Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
- Hợp chất A:
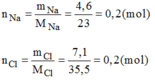
Cứ 0,2 mol hợp chất A có chứa 0,2 mol Na và 0,2 mol Cl.
Suy ra 1 mol hợp chất A có chứa 1 mol Na và 1 mol Cl.
Vậy công thức hóa học đơn giản của A là NaCl.
- Hợp chất B:
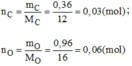
Vậy 0,03mol phân tử B có chứa 0,03 mol phân tử C và 0,06 mol nguyên tử O.
Suy ra 1 mol phân tử B có chứa 1 mol nguyên tử C và 2 mol nguyên tử O.
→Công thức hóa học của B là C O 2
- Hợp chất C:
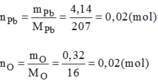
Vậy 0,02 mol phân tử C có chứa 0,02 mol nguyên tử Pb và 0,02 mol nguyên tử O.
Suy ra 1 mol phân tử C có chứa 1 mol nguyên tử Pb và 1 mol nguyên tử O.
→Công thức của phân tử C là: PbO.
- Hợp chất D:
Theo đề bài: 0,04 mol phân tử D có 0,08 mol Fe và 3 mol O.
Vậy 1 mol phân tử D có: 2 mol Fe và 0,12 mol O.
→ Công thức hóa học của D là F e 2 O 3
- Hợp chất E:
Cho biết: 0,02 mol phân tử E có 0,04 mol Na kết hợp 0,02 mol C và 0,06 mol nguyên tử O.
Vậy 1 mol phân tử E co 2 mol Na kết hợp 1 mol C và 3 mol O.
Công thức hóa học của E là N a 2 C O 3 .
Đúng 0
Bình luận (0)
Cho các nguyên tử Mg, Cl, Al, O a, Viết cấu hình e của nguyên tử, ion b, Viết phương trình cho - nhận e tạo thành phân tử MgCl2, Al2O3, MgO, AlCl3
hãy tìm khối lượng của :
a. 3 mol nguyên tử Cl và 1 mol phân tử Cl2
b. 1 mol nguyên tử Ca và 5 mol phân tử CaO
a) 3 mol Cl = 3.35 = 105g
1 mol Cl2 = 35.2 = 70g
b) 1 mol Ca = 40g
5 mol CaO = 5( 40+ 16) = 280g
Đúng 0
Bình luận (0)
a) m3.Cl= 3. MCl=3.35,5=106,5(g)
\(m_{Cl_2}=2.M_{Cl}=2.35,5=71\left(g\right)\)
b) mCa=40(g)
m5.CaO= 5.MCa+5.MO=5.40+5.16=280(g)
Đúng 0
Bình luận (0)
Hòa tan hỗn hợp chứa 0,15 mol Mg và 0,15 mol Al vào dung dịch hỗn hợp chứa 0,15 mol Cu(NO3)2 và 0,525 mol AgNO3. Khỉ phản ứng xong chất rắn thu được có khối lượng là: A. 63,9 B. 66,3 C. 56,7 D. 32,4
Đọc tiếp
Hòa tan hỗn hợp chứa 0,15 mol Mg và 0,15 mol Al vào dung dịch hỗn hợp chứa 0,15 mol Cu(NO3)2 và 0,525 mol AgNO3. Khỉ phản ứng xong chất rắn thu được có khối lượng là:
A. 63,9
B. 66,3
C. 56,7
D. 32,4
Đáp án A
Thứ tự các phản ứng xảy ra:
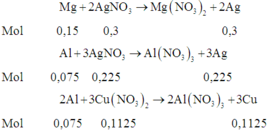
Vậy mchất rắn sau phản ứng = mAg + mCu = 108.0,525 + 64.0,1125 = 63,9 (gam)
Đúng 0
Bình luận (0)
1. 2mol mol nguyên tử sắt (fe) là lượng có chứa bao nhiêu nguyên tử sắt 2. 3 mol phân tử nước (H2O) là lượng có chứa bao nhiêu phân tử nước 3. 3,011.10²³ nguyên tử sắt (Fe) có chứa mấy mol? 4. 18,066.10²³ nguyên tử K có chứa mấy mol?
1)
Số nguyên tử Fe = 2.6,022.1023 = 12,044.1023 (nguyên tử)
2)
Số phân tử H2O = 3.6,022.1023 = 18,066.1023 (nguyên tử)
3)
\(n_{Fe}=\dfrac{3,011.10^{23}}{6,022.10^{23}}=0,5\left(mol\right)\)
4)
\(n_K=\dfrac{18,066.10^{23}}{6,022.10^{23}}=3\left(mol\right)\)
Đúng 1
Bình luận (0)
Một chất hữu cơ Z (chứa các nguyên tố C, H, Cl) trong đó thành phần % theo khối lượng của Cl là: 70,3%, của H: 5,94%. Biết 0,1 mol chẩ này có khối lượng 5,05 g. Xác định công thức phân tử, công thức cấu tạo của Z.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân của nhau cần dùng 0,525 mol O2 và thu được 0,45 mol CO2, 0,45 mol H2O. Nếu cho m gam X tác dụng hết với 0,2 mol NaOH, rồi cô cạn dung dịch tạo thành còn lại 12,9 gam chất rắn khan. Phần trăm khối lượng của este có số nguyên tử cacbon trong gốc axit nhỏ hơn trong X là A. 66,67. B. 50,00. C. 33,33. D. 60,00.
Đọc tiếp
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân của nhau cần dùng 0,525 mol O2 và thu được 0,45 mol CO2, 0,45 mol H2O. Nếu cho m gam X tác dụng hết với 0,2 mol NaOH, rồi cô cạn dung dịch tạo thành còn lại 12,9 gam chất rắn khan. Phần trăm khối lượng của este có số nguyên tử cacbon trong gốc axit nhỏ hơn trong X là
A. 66,67.
B. 50,00.
C. 33,33.
D. 60,00.
Đáp án : A
Bảo toàn O : nO(X) = 2nCO2 + nH2O – 2nO2 = 0,3 mol
=> nX = ½ nO = 0,15 mol
=> nC : nH : nO = 0,45 : 0,9 : 0,3 = 3 : 6 : 2
=> X là C3H6O2 gồm 2 este : x mol CH3COOCH3 và y mol HCOOC2H5
=> nNaOH dư = nNaOH – nX = 0,2 – 0,15 = 0,05 mol
mrắn = mCH3COONa + mHCOONa + mNaOH
=> 82x + 68y = 12,9 – 40.0,05
nX = x + y = 0,15
=> x = 0,05 ; y = 0,1 mol
=> %mHCOOC2H5 = 66,67%
Đúng 0
Bình luận (0)
















