Dựa vào các giá trị năng lượng liên kết, hãy dự đoán ở nhiệt độ thường thì đơn chất nitrogen hay chlorine dễ phản ứng với hydrogen hơn. Cho biết năng lượng liên kết Cl − Cl trong phân tử chlorine là 243 kJ.mol-1.

Những câu hỏi liên quan
Khi phản ứng với H2, các phân tử như F2, N2 cần phải cắt đứt liên kết giữa các nguyên tử. Dựa vào năng lượng liên kết, em hãy dự đoán phản ứng của F2 hay của N2 với H2 sẽ thuận lợi hơn (dễ xảy ra hơn)?
- Giá trị năng lượng liên kết của:
+ F – F trong phân tử F2: 159 kJ mol-1
+ N = N trong phân tử N2: 418 kJ mol-1
⟹ Năng lượng liên kết của F – F < N = N.
⟹ Liên kết của N2 bền hơn F2.
- Vậy phản ứng giữa F2 với H2 thuận lợi hơn (dễ xảy ra hơn) so với phản ứng giữa N2 với H2.
Đúng 0
Bình luận (0)
Dựa vào giá trị độ âm điện của carbon, hydrogen và chlorine, nhận xét về sự phân cực của các liên kết C – C, C – H và C – Cl.
Liên kết | C – C | C – H | C – Cl |
Hiệu độ âm điện | 0 | 0,35 | 0,96 |
Nhận xét: độ phân cực của liên kết tăng dần theo thứ tự: C – C, C – H, C – Cl.
Đúng 0
Bình luận (0)
Năng lượng liên kết của liên kết C – C (trong phân tử ethane) là 368 kJ mol-1 và năng lượng liên kết của liên kết C = C (trong phân tử ethene) là 636 kJ mol-1. Hãy cho biết liên kết nào (σ hay π) dễ bị bẻ gãy hơn khi phân tử tham gia phản ứng.
Liên kết đơn C – C có gồm 1 liên kết σ có năng lượng là 368 kJ mol-1.
Liên kết đôi C = C gồm 1 liên kết σ và liên kết π có năng lượng là 636 kJ mol-1.
=> Năng lượng của liên kết π là: 636 – 368 = 268 (kJ mol-1)
Vì năng lượng của liên kết σ (368 kJ mol-1) lớn hơn năng của liên kết π (268 kJ mol-1) nên khi phân tử tham gia phản ứng, liên kết π dễ bị bẻ gãy hơn.
Đúng 0
Bình luận (0)
Sử dụng bảng giá trị năng lượng liên kết ở Phụ lục 2.
a) Hãy tính tổng năng lượng liên kết trong mỗi phân tử H2S và H2O.
b) Nhiệt độ để bắt đầu phá vỡ liên kết (nhiệt độ phân hủy) trong hai chất trên ứng với một trong hai nhiệt độ sau: 400oC hoặc 1000oC. Em hãy dự đoán nhiệt độ phân hủy của chất nào cao hơn. Vì sao?
a)
- Phân tử H2S:
+ Năng lượng liên kết của S – H là: 368 kJ mol-1.
+ Vì có 2 liên kết S – H
⟹ Tổng năng lượng liên kết trong phân tử H2S là: 368.2 = 736 (kJ mol-1)
- Phân tử H2O:
+ Năng lượng liên kết của O – H là: 464 kJ mol-1.
+ Vì có 2 liên kết O – H
⟹ Tổng năng lượng liên kết trong phân tử H2O là: 464.2 = 928 (kJ mol-1)
b)
- Ta thấy năng lượng liên kết của H2S là 38 kJ mol-1 ; của H2O là 928 kJ mol-1.
⟹ Năng lượng liên kết của H2S < H2O.
⟹ Liên kết của H2O bền hơn H2S.
⟹ Nhiệt độ phân hủy của H2O > H2S.
Đúng 0
Bình luận (0)
đơn chất magnesium và đơn chất chlorine phản ứng với nhau tạo thành hợp chất magnesium chloride ,là hợp chất có cấu trúc tinh thể vẽ sơ đồ mô tả sự hình thành liên kết ion trong hợp chất MgCl2 từ các nguyên tử Mg và Cl . Cho biết số proton trong hạt nhân của Mg là 12 và của Cl là 17
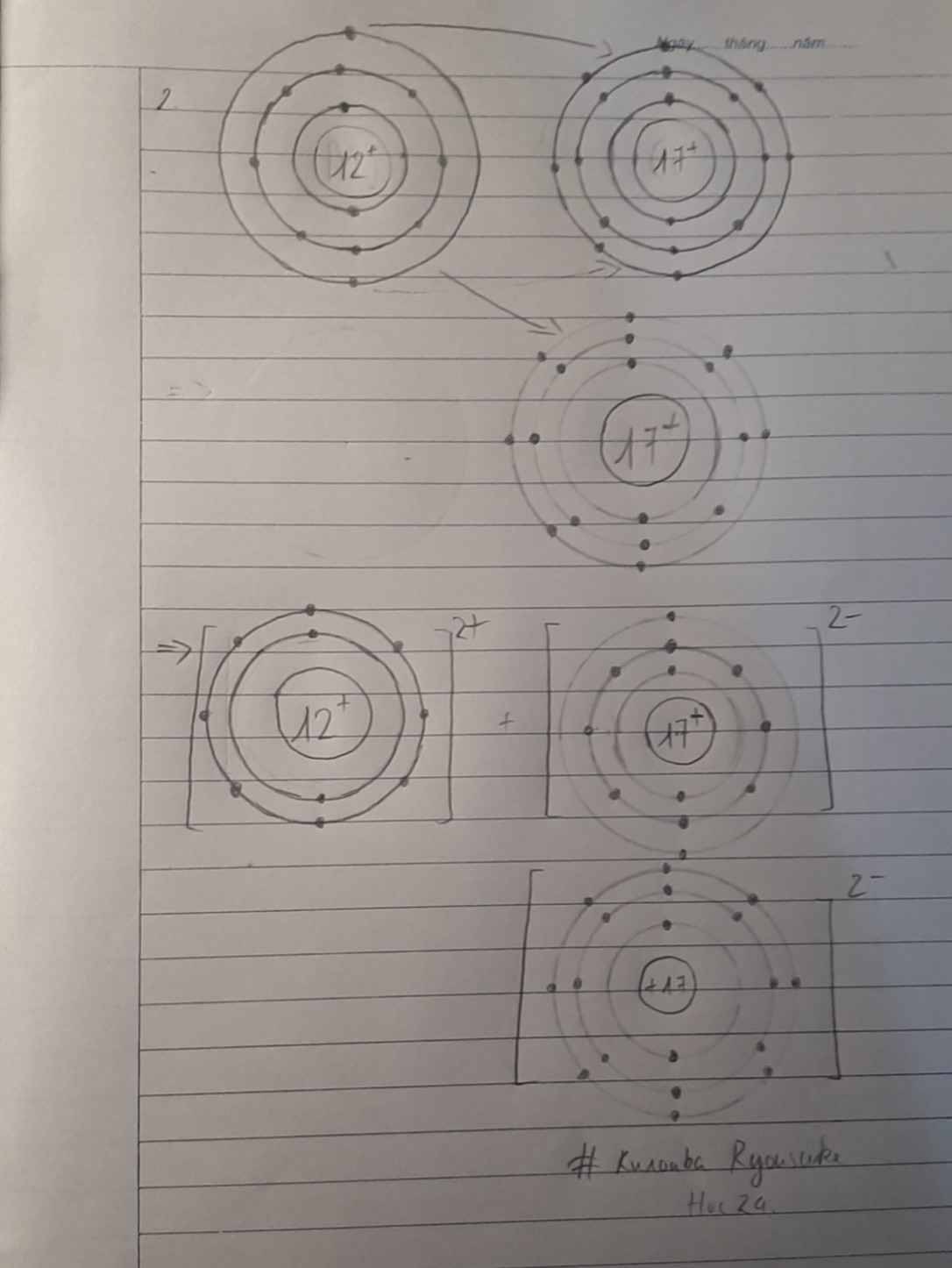
*chỉ vẽ sơ đồ thôi bạn nhỉ?
Đúng 5
Bình luận (7)
Hai nguyên tử Cl liên kết với nhau tạo thành phân tử chlorine
a) Mỗi nguyên tử Cl cần thêm bao nhiêu electron vào lớp ngoài cùng để có lớp vỏ tương tự khí hiếm
b) Hãy vẽ sơ đồ tạo thành liên kết trong phân tử chlorine
Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Từ đây em tự vẽ khi mỗi nguyên tử góp 1e dùng chung
Đúng 0
Bình luận (0)
Dựa vào năng lượng liên kết, tính ${\Delta _r},H_{298}^0$ các phản ứng sau:
a) Các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4, C2H6, H2 ở thể khí.
b) F2(g) + H2O(g) → 2HF(g) + ½ O2(g)
Dự đoán các phản ứng trên là thuận lợi hay không thuận lợi.
a)
- Xét phản ứng đốt cháy 1 mol C2H4
C2H4 (g) + 3O2 (g) → 2CO2 (g)+ 2H2O (g)
∆fH0298 = 1 x Eb (C2H4) + 3 x Eb (O2) - 2 x Eb (CO2) - 2 x Eb (H2O)
∆fH0298 = 1 x EC=C + 4 x EC-H + 3 x EO2 – 2 x 2EC=O – 2 x 2EO-H
∆fH0298 = 1x611 + 4x414 + 3x498 – 2x2x799 – 2x2x464 = -1291kJ
- Xét phản ứng đốt cháy 1 mol C2H6
C2H6 (g) + 7/2 O2 (g) → 2CO2 (g)+ 3H2O (g)
∆fH0298 = 1 x Eb (C2H6) + 7/2 x Eb (O2) - 2 x Eb (CO2) - 3 x Eb (H2O)
∆fH0298 = 1 x EC-C + 6 x EC-H + 7/2 x EO2 – 2 x 2EC=O – 3 x 2EO-H
∆fH0298 = 1x347 + 6x414 + 7/2 x498 – 2x2x799 – 3x2x464 = -1406kJ
- Xét phản ứng đốt cháy 1 mol CO
CO(g) + ½ O2 (g) → CO2(g)
∆fH0298 = 1 x Eb (CO) + 1/2 x Eb (O2) - 1 x Eb (CO2)
∆fH0298 = 1 x ECO + 1/2 x EO2 – 1 x 2EC=O
∆fH0298 = 1 x 1072 + 1/2 x 498– 1x2x799 = -277kJ
b)
F2(g) + H2O(g) → 2HF(g) + ½ O2 (g)
∆fH0298 = 1 x Eb (F2) + 1 x Eb (H2O) - 2 x Eb (HF) – 1/2 x Eb (O2)
∆fH0298 = 1 x EF-F + 1x2EO-H - 2 x EH-F - 1/2 x EO2
∆fH0298 = 1 x 159 + 2x464– 2x565 - 1/2 x 498= -292kJ
Các phản ứng trên đều có giá trị elthanpy âm => Các phản ứng trên đều thuận lợi
Đúng 0
Bình luận (0)
Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử khí chlorine, khí nitrogen
`Cl_2`
Mỗi nguyên tử `Cl` có `7e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ar`, `2` nguyên tử `Cl` đã liên kết với nhau bằng cách mỗi nguyên tử `Cl` góp chung `1e` ở lớp ngoài cùng tạo thành `1` cặp electron dùng chung.
`N_2`
Mỗi nguyên tử `N` có `5e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ne`,`2` nguyên tử `N` đã liên kết với nhau bằng cách mỗi nguyên tử `N` góp chung `3e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.
Đúng 2
Bình luận (0)
Biết năng lượng liên kết của phân tửCl2là 243 kJ mol-1, năng lượng ion hoá thứ nhất của nguyên tử Cl và phân tử Cl2 lần lượt là 1 250 và 1 085 kJ mol-1. Tính năng lượng liên kết của Cl2 + và thảo luận tiểu phân nào (Cl2, Cl2 +) có liên kết dài hơn. Giải thích.
Đọc tiếp
Biết năng lượng liên kết của phân tửCl2là 243 kJ mol-1, năng lượng ion hoá thứ nhất của nguyên tử Cl và phân tử Cl2 lần lượt là 1 250 và 1 085 kJ mol-1. Tính năng lượng liên kết của Cl2 + và thảo luận tiểu phân nào (Cl2, Cl2 +) có liên kết dài hơn. Giải thích.
Ta có hai sơ đồ ứng với quá trình:
\(Cl_2->2Cl->Cl^+,Cl\\ Cl_2->Cl_2^+->Cl^+,Cl\)
Theo nguyên lý I của nhiệt động học:
\(E_{b\left(Cl_2\right)}+IE_{Cl}=IE_{Cl_2}+E_{b\left(Cl_2^+\right)}\\ E_{b\left(Cl_2^+\right)}=243+1250-1085=408kJ\cdot mol^{-1}\\ E_{b\left(Cl_2^+\right)}>E_{b\left(Cl_2\right)}\)
Vì \(Cl_2^+\) có ít hơn một e phản liên kết so với Cl2, bậc liên kết cao hơn (1.5), do đó tiểu phân \(Cl_2\) có liên kết dài hơn.
Đúng 1
Bình luận (0)











