KMnO4--to-->
Câu 1. Lập phương trình hóa học của các phản ứng sau:
a. Al + O2 -->to …
b. … + O2 -->to N2O5
c. … + … -->to Fe3O4
d. KClO3 ->to KCl + …
e. KMnO4 ->to … + MnO2 + …
f. C2H6O + … ->to CO2 + H2O
g. Al + H2SO4 loãng → … + H2
h. Fe + … → FeCl2 + H2
i. Fe3O4 + … ->to Fe + …
k. … + … ->to H2O
Mỗi phản ứng hóa học trên đây thuộc loại phản ứng hóa học nào? (Phản ứng: hóa hợp, phân hủy, phản ứng có xảy ra sự oxi hóa chất, thế)
a) Al + O2 → Al2O3
b) N2 + O2 → N2O5
c) Fe + O2 → Fe3O4
d) KClO3 → KCl + O2
e) KMnO4 → K2MnO4 + MnO2 + O2
f) C2H6O + O2 → CO2 + H2O
g) Al + H2SO4 loãng → Al2(SO4)3 + H2
h) Fe + HCl → FeCl2 + H2
i) Fe3O4 + H2 → Fe + H2O
k) H2 + O2 → H2O
(tất cả các phản ứng trên chưa cân bằng)
Phản ứng hoá hợp: a, b, c, k
Phản ứng phân huỷ: d, e
Phản ứng thế: g, h
Phản ứng có sự oxi hoá chất: a, b, c, f, k
a) 4Al + 3O2 -> (t°) 2Al2O3
b) 2N2 + 5O2 -> (t°) 2N2O5
c) 3Fe + 2O2 -> (t°) Fe3O4
d) 2KClO3 -> (t°, MnO2) 2KCl + 3O2
e) 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
f) C2H6O + 3O2 -> (t°) 2CO2 + 3H2O
g) 2Al + 3H2SO4 (loãng) -> Al2(SO4)3 + 3H2
h) Fe + HCl -> FeCl2 + H2
i) Fe3O4 + 4H2 -> (t°) 3Fe + 4H2O
k) 2H2 + O2 -> (t°) 2H2O
Phản ứng hoá hợp: a, b, c, k
Phản ứng phân huỷ: d, e
Phản ứng thế: g, h
Phản ứng có sự oxi hoá chất: a, b, c, f, k
Cho các thí nghiệm sau:
( 1 ) N H 4 N O 2 → t o
( 2 ) K M n O 4 → t o
( 3 ) N H 3 + O 2 → t o
( 4 ) N H 4 C l → t o
( 5 ) ( N H 4 ) 2 C O 3 → t o
( 6 ) A g N O 3 → t o
Số thí nghiệm tạo ra đơn chất là:
A. 6
B. 5
C. 4
D. 3
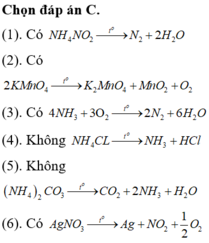
| CHÚ Ý |
| Với phản ứng nhiệt phân NH4NO3 tùy thuộc vào nhiệt độ có thể cho ra khí N2O hoặc N2. |
6. Nhiệt phân hoàn toàn 56,1 gam hỗn hợp gồm 2 muối: KMnO4 và KClO3, sau
khi phản ứng xong thu được 8,96 lít khí O2 ở đktc.
Theo phản ứng: KMnO4 ⎯⎯to→ K2MnO4 + MnO2 + O2 và tính khối lượng
mỗi muối có trong hỗn hợp ban đầu?
Gọi x, y lần lượt là số mol của KMnO4 và KClO3.
Theo đề, ta có: 158x + 122,5y = 56,1 (*)
Ta có: \(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH:
\(2KMnO_4\overset{t^o}{--->}K_2MnO_4+MnO_2+O_2\left(1\right)\)
\(2KClO_3\xrightarrow[MnO_2]{t^o}3KCl+3O_2\left(2\right)\)
Theo PT(1): \(n_{O_2}=\dfrac{1}{2}.n_{KMnO_4}=\dfrac{1}{2}x\left(mol\right)\)
Theo PT(2): \(n_{O_2}=\dfrac{3}{2}.n_{KClO_3}=\dfrac{3}{2}y\left(mol\right)\)
\(\Rightarrow\dfrac{1}{2}x+\dfrac{3}{2}y=0,4\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}158x+122,5y=56,1\\\dfrac{1}{2}x+\dfrac{3}{2}y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{KMnO_4}=158.0,2=31,6\left(g\right)\)
\(m_{KClO_3}=0,2.122,5=24,5\left(g\right)\)
Hoàn thành những phản ứng hoá học sau A. ...+...—to–>MgO B. ...+...—to–>P2O5 C. ...+...—to–>Al2O3 Đ. ...+...—to–>Na2S E. H2O—dp–>...+... F. KClO3–to–>...+... G. ...+...—to–>CuCl2 H. KMnO4—to—>K2MnO4+MnO2+... I. Mg+HCl—>...+... J. Al+H2SO4—>...+... K. H2+...—to–>Cu+... L. CaO+H2O—>... Cho biết mỗi phản ứng hoá học trên thuộc loại phản ứng hoá học nào?
Cho phản ứng sau :
KMnO4 + HCl đặc, nóng;
SO2 + dd KMnO4;
Cl2 + dd NaOH;
H2SO4 đặc, nóng + NaCl; Fe3O4 + HNO3 loãng, nóng;
C6H5CH3 + Cl2 (Fe, to);
CH3COOH và C2H5OH (H2SO4 đặc).
Hãy cho biết có bao nhiêu phản ứng xảy ra thuộc loại phản ứng oxi hóa - khử ?
A. 7
B. 4.
C. 6
D. 5
Cho phản ứng sau : KMnO4 + HCl đặc, nóng; SO2 + dd KMnO4; Cl2 + dd NaOH; H2SO4 đặc, nóng + NaCl; Fe3O4 + HNO3 loãng, nóng; C6H5CH3 + Cl2 (Fe, to); CH3COOH và C2H5OH (H2SO4 đặc). Hãy cho biết có bao nhiêu phản ứng xảy ra thuộc loại phản ứng oxi hóa - khử ?
A. 7
B. 4
C. 6.
D. 5.
Chọn D
KMnO4 + HCl đặc, nóng; SO2 + dd KMnO4; Cl2 + dd NaOH,Fe3O4 + HNO3 loãng, nóng; C6H5CH3 + Cl2 (Fe, to)
nhiệt phân hoàn toàn 15,8 gam KMnO4 thu được một lượng khí O2. Thể tích O2 [ở đktc] thu được sau phản ứng nhiệt phân KMnO4 là ?
\(2KMnO4-->K2MnO4+MnO2+O2\)
\(n_{KMnO4}=\frac{15,8}{158}=0,1\left(mol\right)\)
\(n_{O2}=\frac{1}{2}n_{KMnO4}=0,05\left(mol\right)\)
\(V_{O2}=0,05.22,4=1,12\left(l\right)\)
45. Hoà tan hoàn toàn 61g hỗn hợp KMNO4 và K2CR2O7 vào dd HCl đặc , dư. Sau phản ứng thu đc 17,92 lít khí Cl2(ở đktc) . Thành phần % số mol KMnO4 và K2CR2O7 trong hỗn hợp ban đầu lần lượt là?
Gọi số mol KMnO4: x
K2Cr2O7: y
2KMnO4+16HCl→2KCl+2MnCl2+5Cl2+8H2O
K2Cr2O7+14HCl→2KCl+2CrCl3+3Cl2+7H2O
nCl2=17,92\22,4=0,8
158x+294y=61
5/2x+3y=0,8
⇒{x=0,2
y=0,1
%nKMnO4=0,2\0,3.100=66,67%
%nK2Cr2O7=100−66,67=33,33%
Cho phản ứng sau: (1) KMnO4 + HCl đăc̣, nóng; (2) SO2 + dung dịch KMnO4; (3) Cl2 + dung dịch NaOH; (4) H2SO4 đăc̣, nóng + NaCl; (5)Fe3O4 + dung dịch HNO3 loãng, nóng; (6) C6H5CH3 + Cl2 (Fe, to); (7) CH3COOH và C2H5OH (H2SO4 đăc̣). Hãy cho biết có bao nhiêu phản ứng xảy ra thuôc̣ loaị phản ứng oxi hóa - khử ?
A. 7.
B. 4.
C. 6.
D. 5.
Đáp án D
Phản ứng oxi hóa – khử gồm (1) (2) (3) (5) và (6)