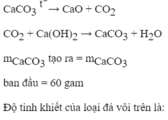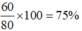Nhiệt phân hoàn toàn 4,86g Ca(HCO3)2. Sau phản ứng thu được V(l) khí CO2 (dktc). Tìm V. (Ca = 40; H = 1; C = 12; O = 16).

Những câu hỏi liên quan
Nhiệt phân hoàn toàn 50,0 gam CaCO3 thu được V lít khí CO2 (đktc). Giá trị của V là (Ca=40, C=12, O=16)
A. 22,4
B. 11,2
C. 33,6
D. 5,6
Đáp án : B
CaCO3 -> CaO + CO2
100g 22,4 lit
50g -> 11,2 lit
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 81 gam Ca(HCO3)2 thu được V lít khí CO2 (đktc). Giá trị của V là:
A. 5,6.
B. 33,6.
C. 11,2.
D. 22,4.
Đáp án D
Ca(HCO3)2 → CaCO3 + CO2 + H2O (nCa(HCO3)2 = 81: 162 = 0,5 mol)
Mol 0,5 → 0,5 → 0,5
CaCO3 → CaO + CO2
Mol 0,5 → 0,5
=> nCO2 = 0,5 + 0,5 = 1 mol
=> VCO2 = 1.22,4 = 22,4 lít
Đúng 0
Bình luận (0)
Dẫn V lít khí CO2 qua dung dịch NaOH, phản ứng xảy ra vừa đủ. Sau phản ứng chỉ thu được muối natri hidrocacbonat với khối lượng là 33,6g. Tìm thể tích khí CO2 (dktc) đã dùng. (Na = 23; H = 1; C = 12; O = 16).
nNaHCO3 = 0,4 (mol)
BTNT C, có: nCO2 = nNaHCO3 = 0,4 (mol)
⇒ VCO2 = 0,4.22,4 = 8,96 (l)
Đúng 1
Bình luận (0)
Khử hoàn toàn 12,32 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 bằng khí CO. Khí đi ra sau phản ứng được dẫn vào dung dịch Ca(OH)2 dư thấy tạo ra 7 gam kết tủa. Khối lượng Fe thu được là: (Fe56;S32; O16; H1; Ca40; C12) A. 7,44 gam B. 14,0 gam C. 11,2 gam D. 7,36gam
Đọc tiếp
Khử hoàn toàn 12,32 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 bằng khí CO. Khí đi ra sau phản ứng được dẫn vào dung dịch Ca(OH)2 dư thấy tạo ra 7 gam kết tủa. Khối lượng Fe thu được là: (Fe=56;S=32; O=16; H=1; Ca=40; C=12)
A. 7,44 gam
B. 14,0 gam
C. 11,2 gam
D. 7,36gam
Đáp án C
- Qui hỗn hợp ban đầu là FexOy
FexOy + yCO → t o xFe + yCO2
CO2 + Ca(OH)2 → CaCO3 + H2O
- Ta thấy nCO2 = nCaCO3 = 7/100 = 0,07 mol
BTKL: m hh đầu + mCO = mFe + mCO2 => 12,32 + 0,07.28 = mFe + 0,07.44 => mFe = 12,32 – 0,07.16 = 11,2g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 12 gam canxi vào dung dịch HCl dư, sau phản ứng thu được khí (dktc) và m(g) muối. Tìm m(g) muối. (Ca = 40; Cl = 35,5).
$n_{Ca} = \dfrac{12}{40} = 0,3(mol)$
$Ca + 2HCl \to CaCl_2 + H_2$
Theo PTHH :
$n_{CaCl_2} = n_{Ca} = 0,3(mol)$
$m_{CaCl_2} = 0,3.111 = 33,3(gam)$
Đúng 1
Bình luận (0)
Nhiệt phân 80g đá vôi, toàn bộ khí sinh ra được sục vào dung dịch nước vôi trong dư, thu được 60g kết tủa C a C O 3 . Giả thiết các phản ứng xảy ra hoàn toàn. Tính độ tinh khiết của loại đá vôi trên (Ca=40, O=16, C=12, Na=23, Si=28).
Dẫn V lít khí CO2 vào dung dịch có hoà tan Y mol Ca(OH)2 sau phản ứng thu được 0,1 mol Ca(HCO3)2 và 0,2 mol CaCO3
\(PTHH:Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
(mol)_______0,2________0,2____0,2
\(PTHH:Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
(mol)________0,1_______0,2_________0,1
\(V=V_{CO_2}=22,4.\left(0,2+0,2\right)=8,96\left(l\right)\)
\(Y=n_{Ca\left(OH\right)_2}=0,2+0,1=0,3\left(mol\right)\)
Đốt cháy hoàn toàn 6g canxi trong khí oxi dư. Sau phản ứng thu được m(g) một oxit. Tìm khối lượng oxit thu được. (Ca = 40; O = 16).
Ta có: \(n_{Ca}=\dfrac{6}{40}=0,15\left(mol\right)\)
PT: \(2Ca+O_2\underrightarrow{t^o}2CaO\)
\(n_{CaO}=n_{Ca}=0,15\left(mol\right)\Rightarrow m_{CaO}=0,15.56=8,4\left(g\right)\)
Đúng 2
Bình luận (0)
\(2Ca+O_2\rightarrow\left(t^o\right)2CaO\\ n_{Ca}=\dfrac{6}{40}=0,15\left(mol\right)\\ n_{CaO}=n_{Ca}=0,15\left(mol\right)\\ m_{CaO}=0,15.56=8,4\left(g\right)\)
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn v (l) khí co2 vào 600ml ca(oh)2 1m đến khi phản ứng kết thúc thu đc 40g kết tủa tìm v
Xem chi tiết
Ta có: \(n_{Ca\left(OH\right)_2}=0,6.1=0,6\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{40}{100}=0,4\left(mol\right)\)
TH1: Ca(OH)2 dư.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{CO_2}=n_{CaCO_3}=0,4\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,4.22,4=8,96\left(l\right)\)
TH2: Ca(OH)2 hết.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
___0,6_____0,6________0,6 (mol)
⇒ nCaCO3 (bị hòa tan) = 0,6 - 0,4 = 0,2 (mol)
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
0,2_____0,2 (mol)
⇒ ΣnCO2 = 0,6 + 0,2 = 0,8 (mol)
\(\Rightarrow V_{CO_2}=0,8.22,4=17,92\left(l\right)\)
Bạn tham khảo nhé!
Đúng 5
Bình luận (0)