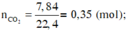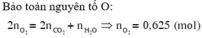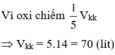Đốt cháy hoàn toàn 23.87 gam P cần V lít khí Oxi.
Giá trị của V là .... lít .Nếu dùng oxi không khí thì thể tích không khí cần là .... lít.
Những câu hỏi liên quan
Trả lờiĐốt cháy hoàn toàn gam P cần V lít khí Oxi.Giá trị của V là Trả lời lít .Nếu dùng oxi không khí thì thể tích không khí cần là Trả lời lít.
Đọc tiếp
Trả lời
Đốt cháy hoàn toànGiá trị của V là Trả lời lít .
Nếu dùng oxi không khí thì thể tích không khí cần là Trả lời lít.
\(n_P=\dfrac{23,87}{31}=0,77\left(mol\right)\\ 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\\ n_{O_2}=\dfrac{5}{4}.0,77=0,9625\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,9625.22,4=21,56\left(l\right)\\ V_{kk\left(đktc\right)}=21,56.5=107,8\left(lít\right)\)
Đúng 1
Bình luận (0)
Ta có: \(n_P=\dfrac{23,87}{31}=0,77\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Theo PT: \(n_{O_2}=\dfrac{5}{4}n_P=0,9625\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,9625.22,4=21,56\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=107,8\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 4,8 gam lưu huỳnh thành lưu huỳnh đioxit thì cần vừa đủ V lít không khí (đktc), biết trong không khí thì oxi chiếm 20% thể tích. Giá trị của V là A. 17,8 B. 18,8 C. 15,8 D. 16,8
Đọc tiếp
Đốt cháy hoàn toàn 4,8 gam lưu huỳnh thành lưu huỳnh đioxit thì cần vừa đủ V lít không khí (đktc), biết trong không khí thì oxi chiếm 20% thể tích. Giá trị của V là
A. 17,8
B. 18,8
C. 15,8
D. 16,8
Câu 7: Để đốt cháy hoàn toàn 3,6 gam than ( C) người ta đã dùng hết V lít không khí ở đktc . Biết khí oxi chiếm 1/5 thể tích không khí. Giá trị của V là :
A. 33,3 lít B.3,36 lít C. 33,6 lít D. 34,2 lít
\(n_C=\dfrac{3.6}{12}=0.3mol\)
\(C+O_2\underrightarrow{t^o}CO_2\)
0.3 0.3
\(V_{O_2}=0.3\times22.4=6.72l\)
\(V_{Kk}=6.72\times5=33.6l\)
Đúng 1
Bình luận (0)
Để đốt cháy hoàn toàn m gam lưu huỳnh cần 22,4 lít không khí, thu được V lít khí lưu huỳnh đioxit. Biết các khí đo ở đktc và khí oxi chiếm 20% thể tích không khí. Tìm giá trị của m và V. (Cho S = 32)
PTHH: \(S+O_2\xrightarrow[]{t^o}SO_2\)
Theo PTHH: \(V_{O_2}=22,4\cdot20\%=4,48\left(l\right)=V_{SO_2}\)
\(\Rightarrow n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_S\) \(\Rightarrow m_S=0,2\cdot32=6,4\left(g\right)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 3,2g hỗn hợp CH4,C2H4,C3H4,C4H4 cần 44,8 lít không khí ( oxi chiếm 20% thể tích không khí)(đktc) thu được V lít CO2 (đktc) và m gam nước . Tính giá trị của m và V?
\(n_{O_2}=\dfrac{44,8}{22,4}.20\%=0,4(mol)\)
Bảo toàn NT (O): \(n_{O_2}=n_{CO_2}=\dfrac{1}{2}n_{H_2O}\)
\(\Rightarrow n_{CO_2}=0,4(mol);n_{H_2O}=0,8(mol)\\ \Rightarrow V_{CO_2}=0,4.22,4=8,96(g);m_{H_2O}=0,8.18=14,4(g)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn m gam hh CH4,C2H4,C3H4,C4H4 cần 41,44 lít không khí(oxi chiếm 20% thể tích không khí)(đktc) thu được V lít CO2(đktc) và 4,68 g nước.Tính giá trị của m và V.
\(n_{O_2}=\dfrac{41,44}{22,4}.20\%=0,37(mol)\\ n_{H_2O}=\dfrac{4,68}{18}=0,26(mol)\)
Bảo toàn nguyên tố (O): \(n_{CO_2}=n_{O_2}=0,37(mol)\)
\(\Rightarrow V_{CO_2}=0,37.22,4=8,288(l)\)
BTKL: \(m_{hh}=m_{CO_2}+m_{H_2O}-m_{O_2}=0,37.44+4,68-0,37.32=9,12(g)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là: A. 70,0 lít B. 78,4 lít C. 84,0 lít D. 56,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
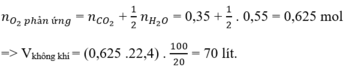
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí
CO
2
(đktc) và 9,9 gam nước. Thể tích không khí (dktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là A. 70,0 lít B. 78,4 lít C. 84,0 lít D. 56,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO 2 (đktc) và 9,9 gam nước. Thể tích không khí (dktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là : A. 78,4 lít B. 56,0 lít C. 70,0 lít D. 84,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
A. 78,4 lít
B. 56,0 lít
C. 70,0 lít
D. 84,0 lít