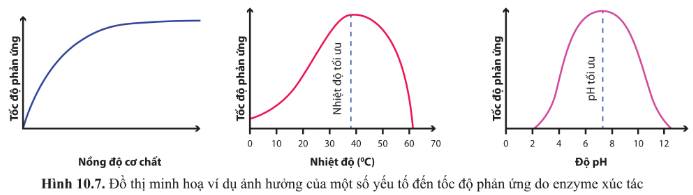
Quan sát hình 10.7 và cho biết khi tăng nồng độ cơ chất hay nhiệt độ, độ pH, tốc độ phản ứng thay đổi như thế nào? Nhận xét về giá trị tốc độ phản ứng ở nhiệt độ tối ưu và pH tối ưu.
Quan sát Hình 1.2, nhận xét về tốc độ của phản ứng thuận và tốc độ của phản ứng nghịch theo thời gian trong điều kiện nhiệt độ không đổi. Nồng độ các chất trong phản ứng thay đổi như thế nào?
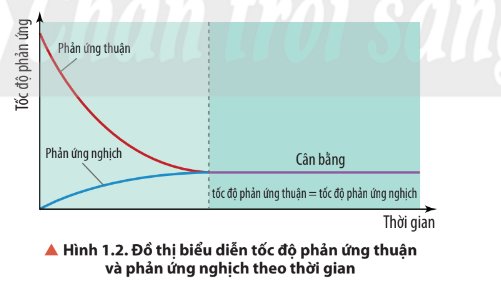
- Ban đầu:
+ Tốc độ phản ứng thuận giảm dần;
+ Tốc độ phản ứng nghịch tăng dần;
- Đến thời điểm cân bằng: Tốc độ phản ứng thuận = tốc độ phản ứng nghịch.
18. Cho phản ứng: H2 (k) + I2 (k) = 2 HI (k)
a) Viết biểu thức của định luật tác dụng khối lượng cho phản ứng trên, biết rằng bậc phản ứng riêng của phản ứng theo H2 và I2 đều bằng 1.
b) Ở 508o C nếu nồng độ của H2 là 0,04 M và I2 là 0,05 M thì tốc độ của phản ứng là 3,2.10−4 mol/l.s. Nếu nồng độ đầu của mỗi chất đều bằng 0,04 M thì cần bao lâu để 50% lượng H2 phản ứng?
c) Tốc độ phản ứng thay đổi ra sao khi tăng áp suất của hệ lên gấp đôi nhưng nhiệt độ của hệ vẫn giữ nguyên không đổi? 19. Khi tăng nhiệt độ từ 50o C lên 100o C, vận tốc của phản ứng tăng lên 243 lần. Hãy cho biết khi tăng nhiệt độ từ 50o C lên 80o C vận tốc phản ứng tăng lên bao nhiêu lần?
20. Phản ứng H2 + I2 à 2HI có năng lượng hoạt hoá bằng 171,71 kJ/mol. Tốc độ phản ứng thay đổi như thế nào khi có mặt chất xúc tác năng lượng hoạt hoá bằng 130,68 kJ/mol ở 300K? Biết hằng số khí lý tưởng R = 8,314 J/K.mol.
phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 tạo thành 2NH3 (phản ứng thuận nghịch)
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Trong các câu sau, câu nào đúng ?
A. Khi nồng độ chất phản ứng tăng thì tốc độ phản ứng tăng.
B. Khi nồng độ chất phản ứng giảm thì tốc độ phản ứng tăng.
C. Khi nồng độ chất phản ứng tăng thì tốc độ phản ứng giảm.
D. Nồng độ chất phản ứng không ảnh hưởng đến tốc độ phản ứng.
Cho phản ứng: Na2S2O3(l) + H2SO4(l) → Na2SO4(l) + SO2(k) + S(r) + H2O(l)?
Khi thay đổi một trong các yếu tố: (1) tăng nhiệt độ; (2) tăng nồng độ Na2S2O3; (3) giảm nồng độ H2SO4; giảm nồng độ Na2SO4; (5) giảm áp suất của SO2; (6) dùng chất xúc tác; có bao nhiêu yếu tố làm tăng tốc độ của phản ứng đã cho?
A. 4
B. 3
C. 2
D. 5
Đáp án B
Có 3 yếu tố làm tăng tốc độ của phản ứng:
(1) tăng nhiệt độ: Tăng sự hỗn loạn trong dung dịch, tăng va chạm giữa các ion, tăng tốc độ phản ứng.
(2) tăng nồng độ Na2S2O3: Tăng khả năng va chạm giữa các ion, tăng tốc độ phản ứng.
(6) dùng chất xúc tác làm tăng tốc độ phản ứng, đẩy nhanh đến cân bằng.
Note
Các yếu tố ảnh hưởng tốc độ phản ứng:
+ Nồng độ: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng.
+ Áp suất: Đối với phản ứng có chất khí, khi tăng áp suất, tốc độ phản ứng tăng.
+ Nhiệt độ: Khi tăng nhiệt độ, tốc độ phản ứng tăng.
+ Diện tích bề mặt: Khi tăng diện tích bề mặt chất phản ứng, tốc độ phản ứng tăng.
+ Chất xúc tác là chất làm tăng tốc độ phản ứng, nhưng còn lại sau khi phản ứng kết thúc
Cho phản ứng: Na2S2O3(l) + H2SO4(l) →S(r) + SO2(k) + Na2SO4(l)+H2O. Khi thay đổi một trong các yếu tố: (1) tăng nhiệt độ; (2) tăng nồng độ Na2S2O3; (3) giảm nồng độ H2SO4; (4) giảm nồng độ Na2SO4; (5) giảm áp suất của SO2; (6) dùng chất xúc tác; có bao nhiêu yếu tố làm tăng tốc độ của phản ứng đã cho?
A. 4
B. 3
C. 2
D. 5.
Cho phản ứng đơn giản xảy ra trong bình kín: 2NO(g) + O2(g) → 2NO2(g)
a) Viết biểu thức tốc độ tức thời của phản ứng.
b) Ở nhiệt độ không đổi, tốc độ phản ứng thay đổi thế nào khi
- nồng độ O2 tăng 3 lần, nồng độ NO không đổi?
- nồng độ NO tăng 3 lần, nồng độ O2 không đổi?
- nồng độ NO và O2 đều tăng 3 lần?
a) Công thức tính tốc độ tức thời của phản ứng là: v1 = k.CNO2.CO2
b)
- Nồng độ O2 tăng 3 lần, nồng độ NO không đổi: v2 = k.CNO2.(CO2.3)
=> v2 tăng 3 lần so với v1
- Nồng độ NO tăng 3 lần, nồng độ O2 không đổi: v3 = k.(CNO.3)2.CO2 = k.CNO2.9.CO2
=> v3 tăng 9 lần so với v1
- Nồng độ NO và O2 đều tăng 3 lần: v4 = k.(CNO.3)2.(CO2.3) = k.CNO2.27.CO2
=> v4 tăng 27 lần so với v1
Xét phản ứng: 2NO + O2->2NO2. Tốc độ phản ứng thay đổi như thế nào khi:
a/ Tăng nồng độ NO lên gấp đôi, giữ nguyên nồng độ O2.
b/ Thể bình bình giảm đi 1 nửa.
c/ Áp suất bình phản ứng tăng lên 2 lần.
d/ Tăng nhiệt độ từ 400C lên 1900C. Biết khi nhiệt độ tăng 150C thì tốc độ phản ứng tăng 3 lần.
Các bạn giúp mình với nha, mình cần lắm luôn!
Tốc độ tức thời của phản ứng:
\(v=k\left[NO\right]^2.\left[O_2\right]\)
a,
Khi tăng nồng độ NO lên gấp đôi:
\(v=k\left(2\left[NO\right]\right)^2.\left[O_2\right]=4k\left[NO\right]^2.\left[O_2\right]\)
Vậy tốc độ tăng gấp 4 lần
b,
Khi thể tích giảm 1 nửa, nồng độ mỗi chất tăng gấp đôi:
\(v=k\left(2\left[NO\right]\right)^2.2\left[O_2\right]=8k\left[NO\right]^2.\left[O_2\right]\)
Vậy tốc độ tăng gấp 8 lần
c,
Độ tăng nhiệt:
\(\Delta t^o=1900-400=1500\)
Với mỗi lần tăng nhiệt độ 150oC, tốc độ tăng 3 lần.
Vậy khi tăng nhiệt độ 10 lần như vậy, tốc độ tăng 310 = 59049 lần
phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 ⇔ 2NH3
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .