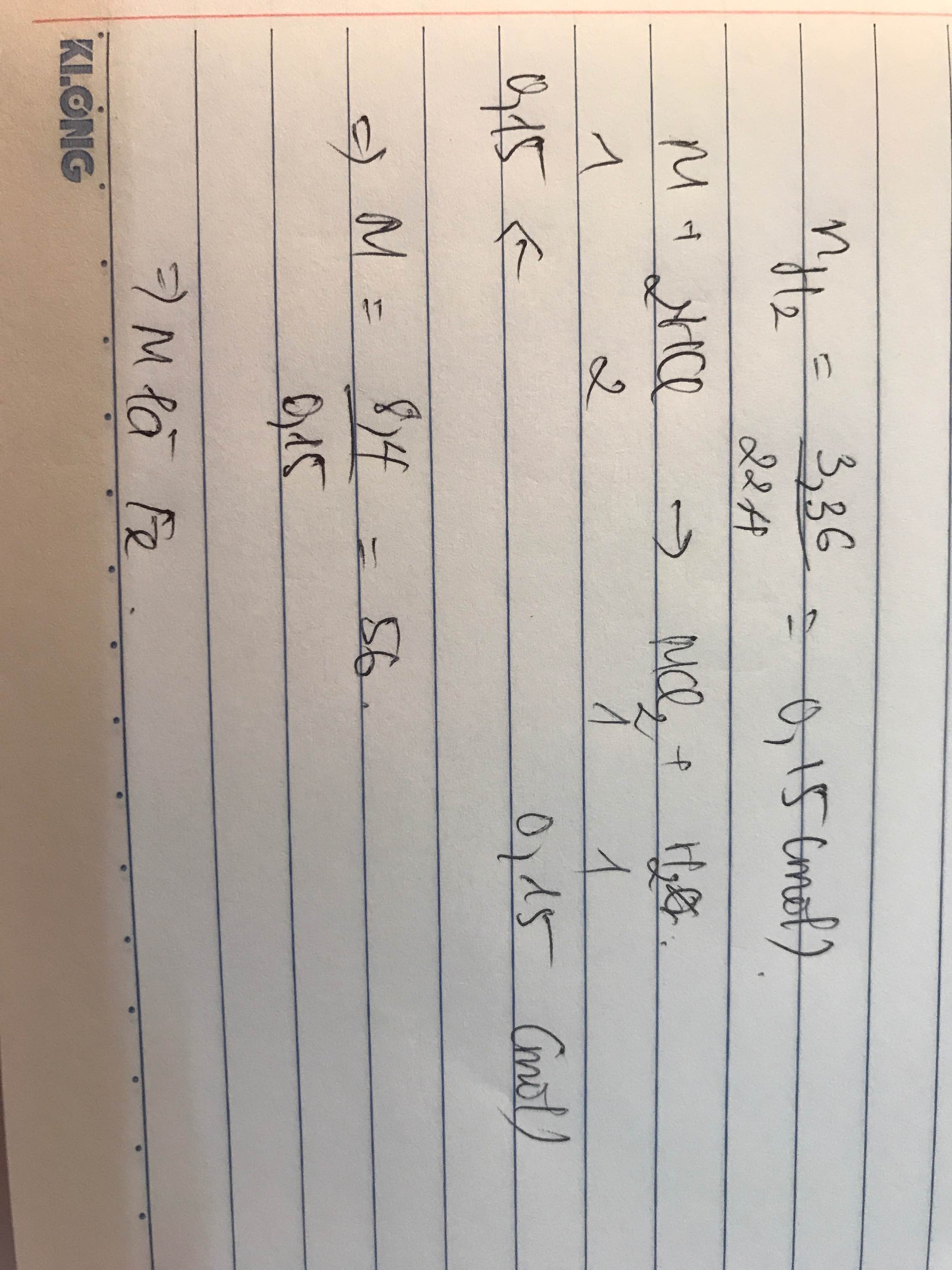hòa tan vừa hết 4 8 gam kim loại r(hoad trị 2) cần phải dùng m gam dung dịch hcl 7,3%.sau phản ứng thử được 4,48 lít khí h2(ở dktc).tìm tên kim loại r và nồng độ phần trăm muối trong dd thu được.

Những câu hỏi liên quan
Hòa tan hết 2,8 gam kim loại Fe vào cốc đựng 60 gam dung dịch HCl 7,3% thu được khí
H
2
và dung dịch X. Nồng độ phần trăm của muối sắt (II) clorua trong dung dịch sau phản ứng là A. 9,11%. B. 10,03%. C. 10,13%. D. 12,13%.
Đọc tiếp
Hòa tan hết 2,8 gam kim loại Fe vào cốc đựng 60 gam dung dịch HCl 7,3% thu được khí H 2 và dung dịch X. Nồng độ phần trăm của muối sắt (II) clorua trong dung dịch sau phản ứng là
A. 9,11%.
B. 10,03%.
C. 10,13%.
D. 12,13%.
Cho 4,8 gam kim loại M vào 50 gam dung dịch HCl nồng độ 36,5 % , phản ứng xong thu được 4,48 lít khí H2 , ( ở đktc ) và dung dịch X. Xác định kim loại M và tính nồng độ phần trăm các chất trong X.
PTHH: \(2M+2xHCl\rightarrow2MCl_x+xH_2\uparrow\) (x là hóa trị của M)
Tính theo sản phẩm
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_M=\dfrac{0,4}{x}\left(mol\right)\) \(\Rightarrow M=\dfrac{4,8}{\dfrac{0,4}{x}}=12x\)
Ta thấy với \(x=2\) thì \(M=24\) (Magie)
Mặt khác: \(n_{HCl}=\dfrac{50\cdot36,5\%}{36,5}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\\n_{HCl\left(dư\right)}=0,1\left(mol\right)\end{matrix}\right.\)
Ta lại có: \(m_{dd\left(sau.p/ứ\right)}=m_{Mg}+m_{ddHCl}-m_{H_2}=4,8+50-0,2\cdot2=54,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,2\cdot95}{54,4}\cdot100\%\approx34,93\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,1\cdot36,5}{54,4}\cdot100\%\approx6,71\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
hòa tan hoàn toàn 7,8 gam kim loại kiềm trong dung dịch hcl 10% sau phản ứng thu được dung dịch x và 2,24 lít khí
a .xác định tên của kim loại trên
b. tìm nồng độ phần trăm của các chất trong dung dịch sau phản ứng biết HCl dùng dư 20% so với lượng phản ứng
Xem chi tiết
Gọi kim loại cần tìm là A
a) PTHH: \(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\uparrow\)
\(AOH+HCl\rightarrow ACl+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{7,8}{0,2}=39\) \(\Rightarrow\) Kim loại cần tìm là Kali
b) Ta có: \(\left\{{}\begin{matrix}n_{KCl}=0,2mol\\n_{HCl\left(pư\right)}=0,2mol\Rightarrow n_{HCl\left(dư\right)}=0,2\cdot20\%=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KCl}=0,2\cdot74,5=14,9\left(g\right)\\m_{HCl\left(dư\right)}=0,04\cdot36,5=1,46\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{H_2}=2\cdot0,1=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_K+m_{ddHCl}-m_{H_2}=7,8+\dfrac{0,24\cdot36,5}{10\%}-0,2=95,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{KCl}=\dfrac{14,9}{95,2}\cdot100\%\approx15,65\%\\C\%_{HCl\left(dư\right)}=\dfrac{1,46}{95,2}\cdot100\%\approx1,53\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
cho 2,7 gam kim loại nhôm tác dụng được hết với 200 gam dung dịch HCl 7,3%.
1. tính thể tích H2 thu được sau phản ứng (dktc)
2. tính nồng độ phần trăm chất trong dung dịch thu được sau phản ứng
\(nAl=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(mHCl=\dfrac{200.7,3\%}{100\%}=14,6\left(g\right)\)
\(nHCl=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH:
\(2Al+6HCl\rightarrow2AlCl_2+3H_2\)
2 6 2 3 (mol)
0,1 0,3 0,1 0,15 (mol)
LTL : 0,1 / 2 < 0,4/6
=> Al đủ , HCl dư
1. \(VH_2=0,15.22,4=3,36\left(l\right)\)
2. \(mH_2=0,15.2=0,3\left(g\right)\)
mdd = mAl + mddHCl - mH2 = 2,7 + 200 - 0,3 = 202,4 (g)
\(mH_2SO_{4\left(dưsaupứ\right)}=0,1.98=9,8\left(g\right)\)
\(mAlCl_2=0,1.98=9,8\left(g\right)\)
\(C\%_{ddH_2SO_4}=\dfrac{9,8.100}{202,4}=4,84\%\)
\(C\%_{AlCl_2}=\dfrac{9,8.100}{202,4}=4,84\%\)
Đúng 1
Bình luận (2)
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc) a. Tính giá trị của V? b. Tính khối lượng dung dịch axit HCl đã phản ứng? c. Tính nồng độ phần trăm của muối trong X?
a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2-->0,4----->0,2--->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
b) mHCl = 0,4.36,5 = 14,6 (g)
=> \(m_{dd.HCl}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
c)
mdd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
mZnCl2 = 0,2.136 = 27,2 (g)
=> \(C\%=\dfrac{27,2}{212,6}.100\%=12,8\%\)
Đúng 2
Bình luận (0)
Câu 4. Cho 20, 05 gam một muối cacbonat của kim loại kiềm thổ vào 100 gam dung dịch HCl. Sau phản ứng thu được 4,4912 lít khí ở đktc. Tìm tên của kim loại trên và tính nồng độ phần trăm của dung dịch muối thu được.
Cho 20, 05 gam một muối cacbonat của kim loại kiềm thổ vào 100 gam dung dịch HCl. Sau phản ứng thu được 4,4912 lít khí ở đktc. Tìm tên của kim loại trên và tính nồng độ phần trăm của dung dịch muối thu được.
\(CT:ACO_3\)
\(n_{CO_2}=\dfrac{4.4912}{22.4}=0.2005\left(mol\right)\)
\(ACO_3+2HCl\rightarrow ACl_2+CO_2+H_2O\)
\(0.2005.....0.401.....0.2005...0.2005\)
\(M_{ACO_3}=\dfrac{20.05}{0.2005}=100\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow A=100-60=40\)
\(A:Ca\left(Canxi\right)\)
\(m_{CaCl_2}=0.2005\cdot111=22.2555\left(g\right)\)
\(m_{dd}=20.05+100-0.2005\cdot44=111.228\left(g\right)\)
\(C\%_{CaCl_2}=\dfrac{22.2555}{111.228}\cdot100\%=20\%\)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 5,5 gam hỗn hợp X gồm 2 kim loại Al và Fe cần vừa đủ V lít dung dịch HCl 1M, sau phản ứng thu được 4,48 lít khí H2 ( ở đktc) và dung dịch Y, cô cnaj Y thu được m gam muối khan.a) TÍnh % theo khối lượn các kim loại có trong Xb) Tính các giá trị V và mc) Lấy 1/5 dung dịch Y cho tác dụng với lượng AgNO3 dư thu được bao nhiêu gam chất kết tủa? Biết cá phản ứng đều xảy ra hoàn toàn
Đọc tiếp
Hoà tan hoàn toàn 5,5 gam hỗn hợp X gồm 2 kim loại Al và Fe cần vừa đủ V lít dung dịch HCl 1M, sau phản ứng thu được 4,48 lít khí H2 ( ở đktc) và dung dịch Y, cô cnaj Y thu được m gam muối khan.
a) TÍnh % theo khối lượn các kim loại có trong X
b) Tính các giá trị V và m
c) Lấy 1/5 dung dịch Y cho tác dụng với lượng AgNO3 dư thu được bao nhiêu gam chất kết tủa? Biết cá phản ứng đều xảy ra hoàn toàn