Tính thể tích khí hiđro (ở đktc) cần tác dụng với nhau để tạo ra đc 1,8 gam nước

Những câu hỏi liên quan
Tính thể tích khí hidro và khí oxi (ở đktc) cần tác dụng với nhau để tạo ra 1,8 gam nước.
Tính thế tích khí hiđro và oxi ( ở đktc) cần tác dụng với nhau để tạo ra được 3,6 gam nước
\(PTHH:2H_2+O_2\rightarrow2H_2O\)
Số mol của 3,6 gam nc là:
\(n_{H_2O}=\dfrac{m}{M}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Thể tích khí Oxi là:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Thể tích khí hidro là:
\(V_{H_2}=n.22,4=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(m\right)\)
\(PTHH:2H_2+O_2->2H_2O\)
tỉ lệ :2 1 2
số mol :0,2 0,1 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Tính thể tích khí hiđro và oxi(đktc) cần tác dụng với nhau để tạo ra được 1,8g nước.
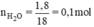
Phương trình phản ứng:
2H2 + O2 → 2H2O.
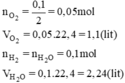
Đúng 0
Bình luận (0)
VD1:Khử 48 gam sắt (III) oxit bằng khí hiđro. Hãy tính(a) số gam sắt kim loại thu được? (b) thể tích khí hiđro (đktc) cần dùng?(c) thể tích khí oxi (đktc) cần dùng khi tác dụng với hiđro để tạo ra lượng nước gấp đôi lượng nước trong phản ứng trên.
Xem chi tiết
Ta có: \(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
_____0,3_____0,9___0,6____0,9 (mol)
a, \(m_{Fe}=0,6.56=33,6\left(g\right)\)
b, \(V_{H_2}=0,9.22,4=20,16\left(l\right)\)
c, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2O}=0,9\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,9.22,4=20,16\left(l\right)\)
Đúng 3
Bình luận (1)
Tính thể tích khí Hiđro và khí Oxi (ở đktc) cần tác dụng với nhau để tạo ra 5,4g nước.
- giúp mình với cần gấp trong đêm nay !!!
Số mol nước tạo thành là:
nH2OnH2O = 1,8/18 = 0,1 (mol)
Phương trình phản ứng:
2H2 + O2 → 2H2O
2 mol 1 mol 2 mol
0,1 mol 0,05 mol 0,1 mol
Thể tích khí hidro tham gia phản ứng:
V = 22,4 x 0,1 = 2,24 (lít)
Thể tích khí oxi tham gia phản ứng:
V = 22,4 x 0,05 = 1,12 (lít)
- cái này là Hóa 8 mà sao cho dzô thể loại toán 7 vậy má =))
Tính thể tích khí hiđro và khí oxi( ở đktc) cần tác dụng với nhau để tạo ra được 1,8 gam nước.
nH2O = 1,8 / 18 = 0,1 mol
Phương trình phản ứng:
2H2 + O2 —> 2H2O
2 mol 1 mol 2 mol
y mol x mol <— 0,1 mol
x = 0,1 / 2 = 0,05 mol -> VO2 = 0,05 x 22,4 = 1,12 lít
y = (2 x 0,1) / 2 = 0,1 mol -> VH2= 0,1 x 22,4 = 2,24 lít.
Đúng 0
Bình luận (0)
Ta có nH2O = \(\dfrac{1,8}{18}\) = 0,1 ( mol )
H2 + \(\dfrac{1}{2}\)O2 \(\rightarrow\) H2O
0,1.....0,05.......0,1
=> VH2 = 22,4 . 0,1 = 2,24 ( lít )
=> VO2 = 22,4 . 0,05 = 1,12 ( lít )
Đúng 0
Bình luận (0)
1/ khử 48 gam đồng (II) Oxit bằng khí hiđro.hãy
tính số gam đồng kim loại thu được
tính thể tích khí hiđro (đktc) cần dùng
2/ tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 3
Bình luận (0)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 19,5 gam kẽm tác dụng hết với dung dịch axit Clohiđric. Hãy tính :
A.thể tích khí hiđro sinh ra(đktc)
B.nếu dùng thể tích khí hiđro trên để khử 19,2 gam sắt(3) oxit thì thu đc bao nhiêu gam sắt?
\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH :
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,3 0,3
\(a,V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(b,PTHH:\)
\(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
trc p/u: 0,3 0,12
p/u: 0,3 0,1 0,2 0,3
sau : 0 0,02 0,2 0,3
----> Fe2O3 dư
\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
\(n_{Fe}=0,2.56=11,2\left(g\right)\)
Đúng 2
Bình luận (0)
Cho 4,48 lít khí hiđro tác dụng với khí oxi. Biết các thể tích khí đo ở đktc. Tính a/ số gam nước thu được b/ thể tích khí oxi cần dùng
Số mol của 4,48 lít H2:
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
tỉ lệ: 2 : 1 : 2
0,2-> 0,1 : 0,2( mol)
a/ số gam của 0,2 mol nước:
\(m_{H_2O}=n.M=0,2.=3,6\left(g\right)\)
b/ thể tích của 0,1 mol khí O2:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)























