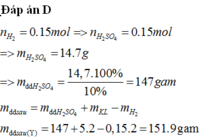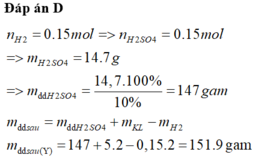cho 16,2g hỗn hợp Zn và Cu tác dụng vừa đủ dung dịch H2SO4,thu được 4,48 lít khí h2(đkc).
a.Tính % khối lượng mỗi chất trong hỗn hợp ban đầu
b.Tính khối lượng muối thu được

Những câu hỏi liên quan
Cho 25,8 gam một hỗn hợp gồm Zn và Cu tác dụng với 200g dung dịch H2SO4 thì thu được 4,48 lít một chất khí không màu. a.Tính % khối lượng mỗi chất trong hỗn hợp đầu? b. Tính nồng độ % của dung dịch thu được sau phản ứng?
\(a.Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ n_{Zn}=n_{H_2}=0,2\left(mol\right)\\ \Rightarrow\%m_{Zn}=\dfrac{0,2.65}{25.8}.100=50,39\%\\ \%m_{Cu}=100-50,39=49,61\%\\ b.m_{ddsaupu}=0,2.65+200-0,2.2=212,6\left(g\right)\\ n_{ZnSO_4}=n_{H_2}=0,2\left(mol\right)\\ C\%_{ZnSO_4}=\dfrac{0,2.161}{212,6}.100=15,15\%\)
Đúng 0
Bình luận (0)
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%, thu được 2,24 lít khí H2 (đkc). Khối lượng dung dịch thu được sau phản ứng là
A. 101,48 gam
B. 101,68 gam
C. 88,20 gam
D. 97,80 gam.
Theo ĐL bao toàn nguyên tố, số mol H2SO4 tham gia phan ứng là:
n(H2SO4) = n(H2) = 2,24/22,4 = 0,1 mol
→ m(H2SO4) = 0,1.98 = 9,8g
Khối lượng dd H2SO4 đa d ng:
m(dd H2SO4) = m9H2SO4)/C% = 9,8/10% = 98g
Khối lượng dung dich thu được sau pư:
m(dd sau) = m(dd H2SO4) + m(hh KL) - m(H2) = 98 + 3,68 - 0,1.2 = 101,48g
=> Đáp án A
Đúng 0
Bình luận (0)
Cho 19,4 gam hỗn hợp gồm Zn và Cu tác dụng vừa đủ với dung dịch HCl. Sau phản ứng thu được 4,48 lít khí H2 đktc
a/ Viết PT phản ứng
b/ Tính khối lượng mỗi kim loại trong hỗn hợp
\(n_{H2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,2
b) \(n_{Zn}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{Zn}=0,2.65=13\left(g\right)\)
\(m_{Cu}=19,4-13=6,4\left(g\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
. Cho 19,4 gam hỗn hợp gồm Zn và Cu tác dụng vừa đủ với dung dịch HCl. Sau phản ứng thu được 4,48 lít khí H2 đktc a/ Viết PTP ứ b/ Tính khối lượng mỗi kim loại trong hỗn hợp.
a, \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,2 0,2
(do Cu ko tác dụng với HCl loãng)
b, \(m_{Zn}=0,2.65=13\left(g\right)\)
\(m_{Cu}=19,4-13=6,4\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 21,1g hỗn hợp Zn và ZnO tác dụng vừa đủ với 200g dd HCl thu được 4,48 lít khí đktc. Tính phần trăm khối lượng mỗi chất có trong hỗn hợp ban đầu, nồng độ phần trăm dd axit và khối lượng muối thu
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,2<--0,4<------0,2<-----0,2
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,2.65}{21,1}.100\%=61,61\%\\\%m_{ZnO}=100\%-61,61\%=38,39\%\end{matrix}\right.\)
\(n_{ZnO}=\dfrac{21,1-0,2.65}{81}=0,1\left(mol\right)\)
PTHH: ZnO + 2HCl ---> ZnCl2 + H2O
0,1---->0,2------>0,1
=> \(C\%_{HCl}=\dfrac{\left(0,2+0,4\right).36,5}{200}.100\%=10,95\%\)
\(m_{mu\text{ố}i}=m_{ZnCl_2}=\left(0,1+0,2\right).136=40,8\left(g\right)\)
Đúng 1
Bình luận (0)
BÀI 2. Cho 19,4 gam hỗn hợp gồm Zn và Cu tác dụng vừa đủ với dung dịch HCl. Sau phản ứng thu được 4,48 lít khí H2 đktc/ a )Viết PTP ứ / b) Tính khối lượng mỗi kim loại trong hỗn hợp.
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,2\left(mol\right)\)
⇒ mZn = 0,2.65 = 13 (g)
⇒ mCu = 19,4 - 13 = 6,4 (g)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Cho 5,2 gam hỗn hợp gồm Al, Mg và Zn tác dụng vừa đủ với dung dịch H2SO4 10% thu được dung dịch Y và 3,36 lít khí H2 (đkc). Khối lượng của dung dịch Y là:
A. 152 gam.
B. 146,7 gam.
C. 175,2 gam
D. 151,9 gam.
Cho 5,2 gam hỗn hợp gồm Al, Mg và Zn tác dụng vừa đủ với dung dịch H2SO4 10% thu được dung dịch Y và 3,36 lít khí H2 (đkc). Khối lượng của dung dịch Y là: A. 152 gam. B. 146,7 gam. C. 175,2 gam D. 151,9 gam.
Đọc tiếp
Cho 5,2 gam hỗn hợp gồm Al, Mg và Zn tác dụng vừa đủ với dung dịch H2SO4 10% thu được dung dịch Y và 3,36 lít khí H2 (đkc). Khối lượng của dung dịch Y là:
A. 152 gam.
B. 146,7 gam.
C. 175,2 gam
D. 151,9 gam.
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là: A. 13,8;7,6;11,8 B. 11,8;9,6;11,8 C. 12,8;9,6;10,8 D. kết quả khác
Đọc tiếp
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là:
A. 13,8;7,6;11,8
B. 11,8;9,6;11,8
C. 12,8;9,6;10,8
D. kết quả khác
Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)
Đúng 0
Bình luận (0)