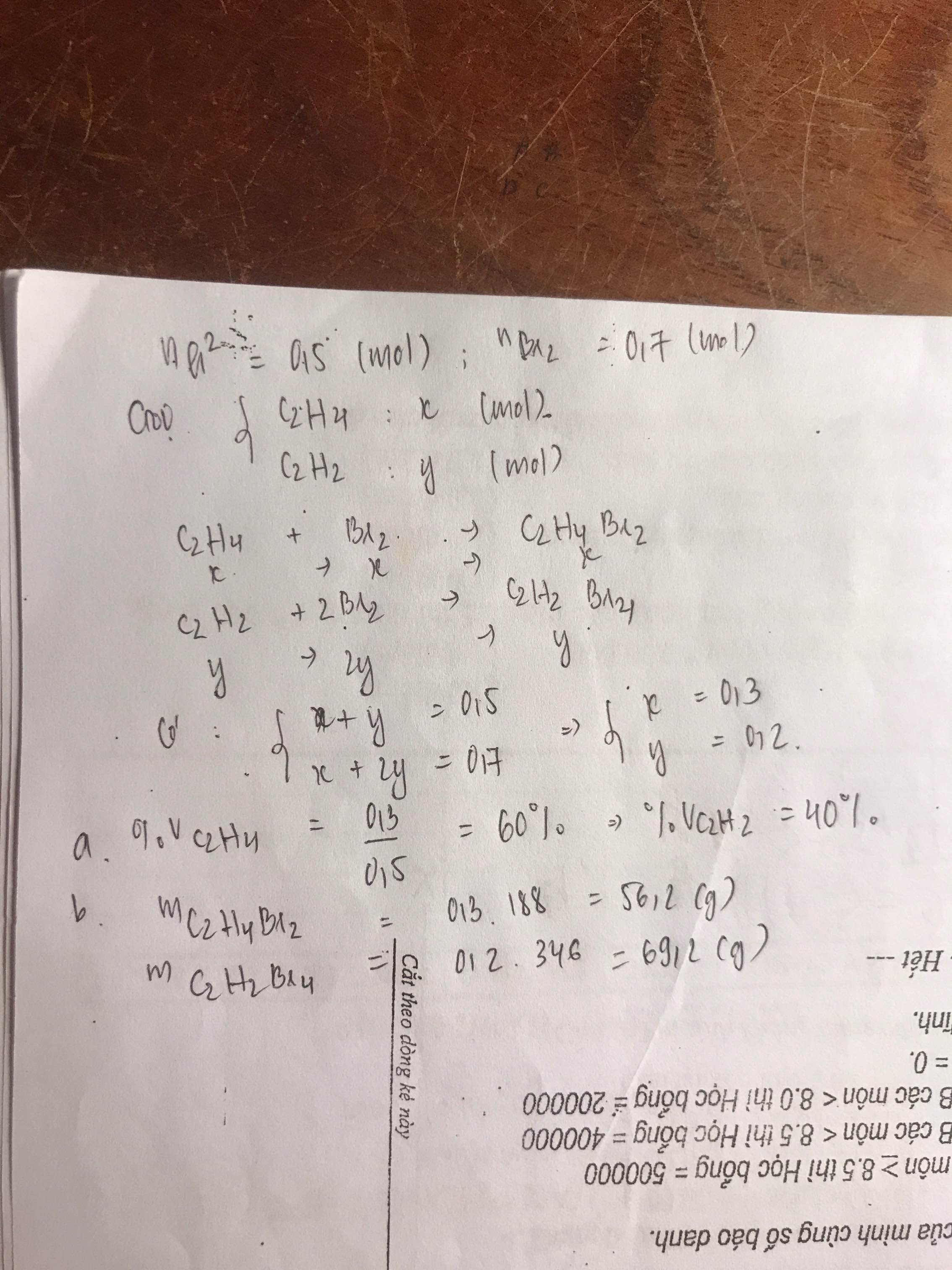Chỉ em bài này ạ cho 4,48l hỗn hợp etilen và axetilen phần cứng dd brom thì thấy có 48g dd brom phản ứng

Những câu hỏi liên quan
Câu 1: Khi cho 4g hỗn hợp gồm khí metan và etilen đi quabình đựng dd brom phản ứng xong thì thấy lượng brom tham gia phản ứng là 16ga) khí nào ở trên đã phản ứng với brom? viết PTHH
b)tính thành phần % khối lượng mỗi khí trong hỗn hợp ban đầu
Xem chi tiết
b)tính thành phần % khối lượng mỗi khí trong hỗn hợp ban đầu
a, - Khí pư với Brom là C2H4
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{0,1.28}{4}.100\%=70\%\\\%m_{CH_4}=100-70=30\%\end{matrix}\right.\)
Đúng 3
Bình luận (1)
Cho 0, 672 lít hỗn hợp etilen và axetilen (đktc) vào dd Br2 dư sau phản ứng có 8,8g hợp chất brom được tạo thành. Tính thành phần phần trăm theo thể tích các khí có trong hỗn hợp.
Gọi số mol C2H4, C2H2 là a, b (mol)
=> a + b = \(\dfrac{0,672}{22,4}=0,03\left(mol\right)\) (1)
PTHH: C2H4 + Br2 --> C2H4Br2
a-------------->a
C2H2 + 2Br2 --> C2H2Br4
b----------------->b
=> 188a + 346b = 8,8 (2)
(1)(2) => a = 0,01 (mol); b = 0,02 (mol)
=> \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,01}{0,03}.100\%=33,33\%\\\%V_{C_2H_2}=\dfrac{0,02}{0,03}.100\%=66,67\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho hỗn hợp 7.437 lít khí metan và etilen vào dd brom dư thấy có 200g dd brom dư thấy có 200g dd br2 8% phản ứng hết
a/viết pt
b/tính % V từng khí
c/tính Vo2 cháy hết lượng khí trên
a) \(n_{Br_2\left(p\text{ư}\right)}=\dfrac{200.8\%}{160}=0,1\left(mol\right);n_{hh}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1<-----0,1
b) \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,1}{0,3}.100\%=33,33\%\\\%V_{CH_4}=100\%-33,33\%=66,67\%\end{matrix}\right.\)
c) \(n_{CH_4}=0,3-0,1=0,2\left(mol\right)\)
PTHH: \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
0,2--->0,4
\(C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\)
0,1--->0,3
\(\Rightarrow V_{O_2}=\left(0,3+0,4\right).24,79=17,353\left(l\right)\)
Đúng 2
Bình luận (0)
dẫn 6,72 lít khí etilen và axetilen qua dd brom dư , phản ứng xảy ra hoàn toàn thì lượng brom phản ứng là 64 g
a viết pthh sảy ra
b tính % theo thể tích của mỗi chất trong hỗn hợp
\(n_{hh}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\)
Gọi số mol của \(C_2H_4\) là: \(a\)
Gọi số mol của \(C_2H_2Br_4\) là: \(b\)
\(PTHH:\\ +)C_2H_2+2Br_2\rightarrow C_2H_2Br_4\\+)C_2H_4+Br_2\rightarrow C_2H_4Br_2 \)
\(\left\{{}\begin{matrix}a+b=0,3\\a+2b=0,4\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\%V_{C_2H_4}=\dfrac{0,2}{0,3}.100\%=66,67\%\\ \%V_{C_2H_2}=100\%-66,67\%=33,33\%\)
Đúng 3
Bình luận (0)
Dẫn 7,84 lít hỗn hợp khí etilen và axetileen lội từ từ qua dd Brom dư thấy có 72 gam brom tham gia phản ứng. Tính thành phần % thể tích mỗi khí trong hỗn hợp đầu.
C2H4 + Br2 -> C2H4Br2
a a a
C2H2 + 2Br2 -> C2H2Br4
b 2b b
n hỗn hợp khí = \(\dfrac{7.84}{22.4}=0.35mol\)
Ta có: \(\left\{{}\begin{matrix}a+b=0.35\\160a+320b=72\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.25mol\\b=0.1mol\end{matrix}\right.\)
\(\%VC2H4=\dfrac{0.25\times22.4\times100}{7.84}=71.43\%\)
%VC2H2 = 100 - 71.43 = 28.57%
Đúng 10
Bình luận (0)
C2H4 + Br2 -> C2H4Br2
a a a
C2H2 + 2Br2 -> C2H2Br4
b 2b b
n hỗn hợp khí = %VC2H4=0.25×22.4×1007.84=71.43%%VC2H4=0.25×22.4×1007.84=71.43%
%VC2H2 = 100 - 71.43 = 28.57%
Đúng 0
Bình luận (0)
Dẫn 5, 6 lít khí đktc gồm metan etilen axetilen qua dung dịch agno3/nh3 thì thu được 24g kết tủa cũng lượng hỗn hợp trên nên cho qua dung dịch brom thì thấy có 48g br2 phản ứng . Tìm%m mỗi chất trong hỗn hợp đầu
Xem chi tiết
nhh = 5.6/22.4 = 0.25(mol)
nAg2C2 = nC2H2 = 24/240 = 0.1 (mol)
nBr2 = 0.3 (mol)
=> nC2H4 = 0.3 - 0.1*2 = 0.1 (mol)
nCH4 = 0.25 - 0.1 - 0.1 = 0.05 (mol)
mCH4 = 0.05*16 = 0.8 (g)
mC2H2 = 0.1*26 = 2.6 (g)
mC2H4 = 0.1*28 = 2.8 (g)
mhh = 0.8 + 2.6 + 2.8 = 6.2 (g)
%CH4 = 0.8/6.2 * 100% = 12.9%
%C2H4 = 2.8/ 6.2 * 100% = 45.16%
%C2H2 = 41.94%
Đúng 2
Bình luận (0)
Dẫn 2,8 lít hỗn hợp Metan (CH4), Etilen (C2H4) đi qua bình đựng dd Brom dư, thấy có 4 gam Brom phản ứng. Viết PTHH và tính phần trăm thể tích mỗi khí trong hỗn hợp ban đầu?
\(n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right);n_{hh}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,025<-0,125
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,025}{0,125}.100\%=20\%\\\%V_{CH_4}=100\%-20\%=80\%\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Cho 11,2 lít hỗn hợp etilen và axetilen tác dụng với dung dịch brom dư thấy có 112 g brom phản ứng .
a/ Tính Phần trăm theo thể tích trong hỗn hợp ban đầu ?
b/ Tính khối lượng sản phảm sau phản ứng ?
Bài 6: Cho 0,224 lít hỗn hợp etilen và axetilen (ở đktc) sục qua dung dịch brom dư, thấy có 1,92 g brom tham gia phản ứng. Tính % thể tích mỗi khí có trong hỗn hợp.
\(n_{Br_2}=\dfrac{1,92}{160}=0,012\left(mol\right)\)
Gọi số mol C2H4, C2H2 là a, b (mol)
=> \(a+b=\dfrac{0,224}{22,4}=0,01\) (1)
PTHH: C2H4 + Br2 --> C2H4Br2
a---->a
C2H2 + 2Br2 --> C2H2Br4
b----->2b
=> a + 2b = 0,012 (2)
(1)(2) => a = 0,008 (mol); b = 0,002 (mol)
=> \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,008}{0,01}.100\%=80\%\\\%V_{C_2H_2}=100\%-80\%=20\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)