NHỮNG quá trình nào sau đây xảy ra phản ứng hóa hợp?(1 Point)Đốt thanĐốt sắt (II) sunfuaĐốt sắtĐốt sắt (II) oxit

Những câu hỏi liên quan
NHỮNG quá trình nào sau đây xảy ra phản ứng hóa hợp?
(1 Point)
A.Đốt than
B.Đốt sắt (II) sunfua
C.Đốt sắt
D.Đốt sắt (II) oxit
Cho 14,4 gam sắt (II) oxit tác dụng với dung dịch axit clohiđric 10% thu được muối sắt (II) clorua và nước.
a.Viết phương trình hóa học của phản ứng xảy ra ?
b.Tính khối lượng muối sắt (II) clorua tạo thành ?
c.Tính khối lượng axit HCl cần dùng
d.Tính C% dung dịch sau phản ứng
GIÚP TỚ VỚI Ạ
`n_[FeO]=[14,4]/72=0,2(mol)`
`a)PTHH:`
`FeO + 2HCl -> FeCl_2 + H_2 O`
`0,2` `0,4` `0,2` `(mol)`
`b)m_[FeCl_2]=0,2.127=25,4(g)`
`c)m_[dd HCl]=[0,4.36,5]/10 .100=146(g)`
`d)C%_[FeCl_2]=[25,4]/[14,4+146].100~~15,84%`
Đúng 3
Bình luận (0)
Hãy cho biết trong những phản ứng hóa học xảy ra quanh ta sau đây, phản ứng nào là phản ứng oxi hóa – khử? Lợi ích và tác hại của mỗi phản ứng? a) Đốt than trong lò: C + O2 → CO2. b) Dùng cacbon oxit khử sắt (III) oxit trong luyện kim. Fe2O3 + 3CO → 2Fe + 3CO2. c) Nung vôi: CaCO3 → CaO + CO2. d) Sắt bị gỉ trong không khí: 4Fe + 3O2 → 2Fe2O3.
Đọc tiếp
Hãy cho biết trong những phản ứng hóa học xảy ra quanh ta sau đây, phản ứng nào là phản ứng oxi hóa – khử? Lợi ích và tác hại của mỗi phản ứng?
a) Đốt than trong lò: C + O2 → CO2.
b) Dùng cacbon oxit khử sắt (III) oxit trong luyện kim.
Fe2O3 + 3CO → 2Fe + 3CO2.
c) Nung vôi: CaCO3 → CaO + CO2.
d) Sắt bị gỉ trong không khí: 4Fe + 3O2 → 2Fe2O3.
Những phản ứng oxi hóa – khử là a), b) ,d).
Phản ứng a) Lợi: sinh ra nhiệt năng để sản xuất phục vụ đời sống. Tác hại: sinh ra khí CO2 làm ô nhiễm môi trường.
Phản ứng b) Lợi: luyện quặng sắt thành gang điều chế sắt. Tác hại: sinh ra khí CO2 làm ô nhiễm môi trường.
Phản ứng d) Tác hại: Làm sắt bị gỉ, làm hư hại các công trình xây dựng, các dụng cụ và đồ dùng bằng sắt.
Đúng 0
Bình luận (0)
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?. b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao? c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
Đọc tiếp
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?.
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 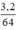 = 0,05 mol
= 0,05 mol
nFe = 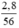 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 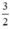 . nFe =
. nFe = 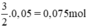 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)
Đúng 0
Bình luận (0)
Cho khí hiđro dư đi qua m gam hỗn hợp đồng (II) oxit và sắt (III) oxit nung nóng, sau khi phản ứng xảy ra hoàn toàn thu được 6 gam hỗn hợp kim loại trong đó có 2,8 gam sắt.
a) Viết các phương trình hóa học xảy ra.
b) Tính thể tích khí hiđro (đktc) đã tham gia phản ứng.
c) Tính m.
a, PTHH:
Fe2O3 + 3H2 ---to---> 2Fe + 3H2O (1)
CuO + H2 ---to---> Cu + H2O (2)
b, nFe = \(\dfrac{2,8}{56}=0,05\left(mol\right)\)
nCu = \(\dfrac{6-2,8}{64}=0,05\left(mol\right)\)
Theo pt (1): nH2 (1) = 2nFe = 2 . 0,05 = 0,1 (mol)
Theo pt (2): nH2 (2) = nCu = 0,05 (mol)
=> VH2 = (0,1 + 0,05) . 22,4 = 3,36 (l)
c, Theo pt (1): nCuO = nCu = 0,05 (mol)
Theo pt (2): nFe2O3 = \(\dfrac{1}{2}n_{Fe}=\dfrac{1}{2}.0,05=0,025\left(mol\right)\)
=> m = 0,05 . 80 + 0,025 . 160 = 8 (g)
Đúng 5
Bình luận (0)
\(a.CuO+H_2-^{t^o}\rightarrow Cu+H_2O\\ Fe_2O_3+3H_2-^{t^o}\rightarrow2Fe+3H_2O\\ b.m_{Cu}=6-2,8=3,2\left(g\right)\\ n_{Cu}=0,05\left(mol\right);n_{Fe}=0,05\left(mol\right)\\ \Sigma n_{H_2}=n_{Cu}+\dfrac{3}{2}n_{Fe}=0,125\left(mol\right)\\ \Rightarrow V_{H_2}=2,8\left(l\right)\\ c.n_{CuO}=n_{Cu}=0,05\left(mol\right);n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,025\left(mol\right)\\ m_{hh}=m_{CuO}+m_{Fe_2O_3}=0,05.80+0,025.160=8g\)
Đúng 3
Bình luận (0)
Viết phương trình hóa học của phản ứng hiđro khử các oxit sau:
a) Sắt (III) oxit.
b) Thủy ngân(II) oxit.
c) Chì(II) oxit.
a) Fe2O3 + 3H2 → 2Fe + 3H2O.
b) HgO + H2 → Hg + H2O.
c) PbO + H2 → Pb + H2O.
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm người ta dùng khí hiđro để khử sắt(II) oxit và thu được 11,2 g Fe.
a) Viết phương trình hóa học của phản ứng đã xảy ra.
b) Tính khối lượng sắt (III) oxit đã phản ứng.
c) Tính thể tích khí hiđro đã tiêu thụ (đktc).
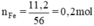
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.
Đúng 0
Bình luận (0)
a. Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit, và sắt (III) oxit ở nhiệt đô thích hợp?
b.Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c. Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,80 gam sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxi và sắt (III) oxit là bao nhiêu?
Đọc tiếp
a. Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit, và sắt (III) oxit ở nhiệt đô thích hợp?
b.Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c. Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,80 gam sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxi và sắt (III) oxit là bao nhiêu?
a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
Đúng 0
Bình luận (0)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)
Đúng 0
Bình luận (1)
a) Phương trình hoá học của các phản ứng:
H2 + CuO —> Cu + H2O (1)
3H2 + Fe2O3 —> Fe + 3H2O (2)
b) Trong phản ứng (1), (2): Chất khử là H2 vì chiếm oxi của chất khác, chất oxi hoá là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được: 6g - 2,8g = 3,2g
VH2 cần dùng (theo phương trình phản ứng (1)) :

VH2 cần dùng (theo phương trình phản ứng (2)) :

Đúng 0
Bình luận (0)
1. a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?.b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?2.Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.a) Viết các phương trìn...
Đọc tiếp
1. a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?.
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
2.Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
CuO+H2-t0-> Cu +H2O
Fe2O3+3H2-t0->2Fe+3H2O
chất khử là H2
chất oxi hóa là CuO và Fe2O3. vì chất khử là chất chiếm oxi của chất khác, còn chất oxi hóa là chất nhường oxi cho chất khác
theo đề bài ->mFe=2,8 g->nFe=0,05 mol
=>mCu=6-2,8=3,2 g->nCu=0,05mol
theo PTPỨ =>nCu=nH2=0,05 mol
3nH2=2nFe->nH2=(2/3)*0,05=1/30 mol
do đó VH2 phản ứng là: (0,05+1/30)*22,4=1,867 lít
Đúng 2
Bình luận (0)
câu 2
a)Zn+H2SO4->ZnSO4+H2
2Al+3H2SO4->Al2(SO4)3+3H2
Fe+H2SO4->FeSO4+H2
b) Fe
cậu chỉ cần đặt a là số gam của từng kim loai.(vì khối lượng của mỗi kim loại bằng nhau). Sau đó theo phương trình cậu tính khối lượng khí H2 ở mỗi phương trình rồi so sánh là được
c) Fe cách tính gần giống phần b nên tự logic nha
Đúng 1
Bình luận (0)



















