: Đốt cháy 1,55 gam photpho trong bình chứa 1,344 lit oxi (đktc). Tính khối lượng chất rắn có trong bình sau khi đốt?
Câu 1:Đốt cháy 12,4 gam photpho trong bình chứa khí oxi tạo thành điphotpho pentaoxit (chất rắn, màutrắng). Tính khối lượng chất rắn tạo thành sau phản ứng.
Câu 2:Đốt cháy 12,4 gam photpho trong bình chứa 5,6 lít khí oxi (đktc) tạo thành điphotpho pentaoxit (chất rắn, màu trắng). Tính khối lượng chất rắn tạo thành sau phản ứng.
Câu 1 :
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
Pt : \(4P+5O_2\underrightarrow{t^o}2P_2O_5|\)
4 5 2
0,4 0,2
\(n_{P2O5}=\dfrac{0,4.2}{4}=0,2\left(mol\right)\)
⇒ \(m_{P2O5}=0,2.142=28,4\left(g\right)\)
Chúc bạn học tốt
Câu 2 :
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
\(n_{O2\left(dktc\right)}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Pt : \(4P+5O_2\underrightarrow{t^o}2P_2O_5|\)
4 5 2
0,4 0,25 0,1
Lập tỉ số só sánh : \(\dfrac{0,4}{4}>\dfrac{0,25}{5}\)
⇒ P dư , O2 phản ứng hết
⇒ Tính toán dựa vào số mol của O2
\(n_{P2O5}=\dfrac{0,25.2}{5}=0,1\left(mol\right)\)
⇒ \(m_{P2O5}=0,1.142=14,2\left(g\right)\)
\(n_{P\left(dư\right)}=0,4-\left(\dfrac{0,25.4}{5}\right)=0,2\left(mol\right)\)
⇒ \(m_{P\left(dư\right)}=0,2.31=6,2\left(g\right)\)
\(m_{rắn}=14,2+6,2=20,4\left(g\right)\)
Chúc bạn học tốt
<Bài 6 Đốt cháy 16,8 gam sắt trong bình chứa 6,72 lit oxi (đktc) thu được oxit sắt từ.
a. Viết PTHH?
b. Tính khối lượng sản phẩm thu được?
Bài 7: Đốt cháy hoàn toàn Photpho trong bình chứa 1,12 lit oxi (dktc) thu được hợp chất có công thức P2O5.
a. Viết phương trình hóa học? b. Tính khối lượng sản phẩm thu được?
c. Tính khối lượng Kali clorat KC1O, cần dùng để điều chế được lượng oxi dùng cho phản ứng trên?
Đốt cháy 6,2g photpho trong bình chứa 7,84 lit oxi (đktc). Hãy cho biết sau khi cháy: Photpho hay oxi, chất nào còn thừa và khối lượng là bao nhiêu?
B1: Để đốt cháy hoàn toàn 10,8 gam nhôm thì thể tích oxi (đktc) cần dùng là bao nhiêu?
B2: Đốt cháy 12,4 gam photpho trong bình chứa khí oxi tạo thành điphotpho pentaoxit (chất rắn, màu trắng). Tính khối lượng chất rắn tạo thành sau phản ứng.
Bài 2:
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
PTHH: 4P + 5O2 → 2P2O5
Mol: 0,4 0,2
\(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
Bài 1:
\(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 4Al + 3O2 ---to→ 2Al2O3
Mol: 0,4 0,3
\(V_{O_2}=0,3.22,4=6,72\left(l\right)\)
Đốt cháy 6,2g photpho trong bình chứa 7,84 lit oxi (đktc). Hãy cho biết sau khi cháy: Chất nào được tạo thành và khối lượng là bao nhiêu?
Đốt cháy hoàn toàn 6,2 g photpho trong bình chứa 8,96 lit khi oxi (ở đktc), ản phẩm thu được là chất rắn, màu trắng. Nếu hiệu suất phản ứng là 80% thì khối lượng chất rắn thu được là bao nhiêu?
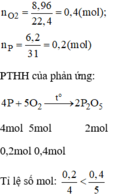
→ Oxi dư, vậy bài toán tính theo số mol của P
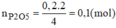
Do H = 80% nên khối lượng chất rắn thu được sau phản ứng là:
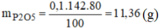
đốt cháy 7,44g photpho trong bình chứa 6,16 lit khí oxi (đktc) tạo thành Điphotpho pentaoxit.Tính khối lượng chất tạo thành
nP = 7,44/31 = 0,24 (mol)
nO2 = 6,16/22,4 = 0,275 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
LTL: 0,24/4 > 0,275/5 => P dư
nP2O5 = 0,275 : 5 . 2 = 0,11 (mol)
mP2O5 = 0,11 . 142 = 15,62 (g)
\(4P+5O_2->2P_2O_5\)
4 5 2
0,24 0,3 0,12 (mol)
\(n_P=\dfrac{m}{M}=\dfrac{7,44}{31}=0,24\left(mol\right)\)
\(m_{P_2O_5}=n\text{×}M=0,12\text{×}\left(31\text{×}2+16\text{×}5\right)=0,12\text{×}142=17,04\left(g\right)\)
Đốt cháy 6,2 gam photpho trong bình chứa 7,84 lít khí oxi ở đktc
a. Viết ptpu xảy ra
b. tính khối lượng chất dư sau phản ứng ?
c. tính khối lượng chất rắn tạo ra ?
$a) 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
$n_P = \dfrac{6,2}{31} = 0,2(mol) ; n_{O_2} = \dfrac{7,84}{22,4} = 0,35(mol)$
$n_P : 4 = 0,05 < n_{O_2} :5 = 0,07$ nên $O_2$ dư
$n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,25(mol)$
$\Rightarrow m_{O_2\ dư} = (0,35 - 0,25).32 = 3,2(gam)$
c) $n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)$
$m_{P_2O_5} = 0,1.142 = 14,2(gam)$
\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\\a, 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\\ V\text{ì}:\dfrac{0,35}{5}>\dfrac{0,2}{4}\Rightarrow O_2d\text{ư}\\ n_{O_2\left(d\text{ư}\right)}=0,35-\dfrac{5}{4}.0,2=0,1\left(mol\right)\\b, m_{O_2\left(d\text{ư}\right)}=0,1.32=3,2\left(g\right)\\ c,n_{P_2O_5}=\dfrac{n_P}{2}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ m_{r\text{ắn}}=m_{P_2O_5}=142.0,1=14,2\left(g\right)\)
đốt cháy hoàn toàn 3,1g photpho trong bình chứa 4,48 lit khí oxi (đktc) phản ứng tạo thành điphotpho pentaoxit a. photpho hay oxi dư và dư bao nhiêu gam b. chất nào được tạo thành ? khối lượng là bao nhiêu
nP= 0.1 mol
nO2= 0.15 mol
4P + 5O2 -to-> 2P2O5
4____5
0.1___0.15
Lập tỉ lệ: 0.1/4 < 0.15/5 => O2 dư
nO2 dư= 0.15 - 0.125=0.025 mol
mO2 dư= 0.8g
nP2O5= 0.05 mol
mP2O5= 7.1g