Câu 5: Hỗn hợp khí X gồm o6zon và oxi có tỉ khối đối với hidro bằng 17,2. Tính phần trăm theo thể tích mỗi khí trong hỗn hợp X.

Những câu hỏi liên quan
Câu 5: Đốt cháy 6 gam cacbon trong khí oxi vừa đủ thì thu được hỗn hợp khí (X) gồm CO và CO 2 có tỉ khối hơi đối với hidro là 17,2. Tính thành phần % về thể tích của các khí?
Xem chi tiết
\(n_C=\dfrac{6}{12}=0,5mol\) \(\overline{M}_{hh}=17,2\cdot2=34,4\)
\(\Rightarrow\dfrac{V_{CO}}{V_{CO_2}}=\dfrac{9,6}{6,4}=\dfrac{3}{2}\\ \Rightarrow\%V_{CO}=60\%\\ \Rightarrow\%V_{CO_2}=40\%\)
Đúng 1
Bình luận (0)
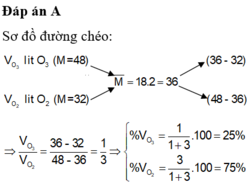
Hỗn hợp khí X gồm ozon và oxi có tỉ khối đối với hiđro bằng 18. Phần trăm theo thể tích mỗi khí trong hỗn hợp X lần lượt là:
A. 25% và 75%
B. 30% và 70%
C. 35% và 65%
D. 40% và 60%
Cho hỗn hợp khí X gồm H2 và CH4 (ở đktc) có tỉ khối đối với khí oxi là 0,325.a. Tính thành phần phần trăm theo thể tích của mỗi khí trong hỗn hợp X.b. Trộn 11,2 lít hỗn hợp khí X với 28,8 gam khí oxi rồi thực hiện phản ứng đốt cháy, phản ứng xong làm lạnh để ngưng tụ hết hơi nước thì thu được khí Y. Xác định phần trăm thể tích và phần trăm khối lượng các chất trong hỗn hợp Y.
Đọc tiếp
Cho hỗn hợp khí X gồm H2 và CH4 (ở đktc) có tỉ khối đối với khí oxi là 0,325.
a. Tính thành phần phần trăm theo thể tích của mỗi khí trong hỗn hợp X.
b. Trộn 11,2 lít hỗn hợp khí X với 28,8 gam khí oxi rồi thực hiện phản ứng đốt cháy, phản ứng xong làm lạnh để ngưng tụ hết hơi nước thì thu được khí Y. Xác định phần trăm thể tích và phần trăm khối lượng các chất trong hỗn hợp Y.
Cho hỗn hợp khí X gồm CO2 và N2 (ở đktc) có tỉ khối đối với khí oxi là 1,225.
1. Tính thành phần % theo thể tích của mỗi khí trong hỗn hợp X.
2. Tính khối lương của 1 lít hỗn hợp khí X ở đktc.
1)
Coi \(n_X = 1(mol)\)
Gọi : \(n_{CO_2} = a(mol) ; n_{N_2} = b(mol)\)
Ta có :
\(n_X = a + b = 1(mol)\\ m_X = 44a + 28b = 1.1,225.32(gam)\\ \Rightarrow a = 0,7 ; b = 0,3\)
Vậy :
\(\%V_{CO_2} = \dfrac{0,7}{1}.100\% = 70\%\\ \%V_{N_2} = 100\% - 70\% = 30\%\)
2)
\(n_X = \dfrac{1}{22,4}(mol)\\ \Rightarrow m_X = n.M = \dfrac{1}{22,4}.1,225.32 = 1,75(gam)\)
Đúng 2
Bình luận (2)
1) Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có tỉ khối đối vs hidro là 18. Hãy xác đimhj thành phần phần trăm theo thể tích của hỗn hợp khí2) Hỗn hợp khí A gồm O2 và O3, tỉ khối hơi của hỗn hợp khí A và khí H2 là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hh khí B đối vs H2 là 3,6.@a) Tính thành phần % theo thể tích của mỗi khí có trong hh khí A và Bb) Một mol khí A có thể đốt cháy hoàn toàn bao nhiêu mol khí COGiải theo pp tăng giảm khối lượng hoặc phương pháp trung bình
Đọc tiếp
1) Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có tỉ khối đối vs hidro là 18. Hãy xác đimhj thành phần phần trăm theo thể tích của hỗn hợp khí
2) Hỗn hợp khí A gồm O2 và O3, tỉ khối hơi của hỗn hợp khí A và khí H2 là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hh khí B đối vs H2 là 3,6.
@
a) Tính thành phần % theo thể tích của mỗi khí có trong hh khí A và B
b) Một mol khí A có thể đốt cháy hoàn toàn bao nhiêu mol khí CO
Giải theo pp tăng giảm khối lượng hoặc phương pháp trung bình
Hỗn hợp khí X gồm ozon và oxi có tỉ khối đối với hiđro bằng 20. Phần trăm theo thể tích oxi trong X là
50%
25%
75%
54%
Hỗn hợp khí A gồm có
O
2
và
O
3
tỉ khối của hỗn hợp khí A đối với khí
H
2
là 19,2. Hỗn hợp khí B gồm có
H
2
và khí CO, tỉ khối của hỗn hợp khí B đối với
H
2...
Đọc tiếp
Hỗn hợp khí A gồm có O 2 và O 3 tỉ khối của hỗn hợp khí A đối với khí H 2 là 19,2. Hỗn hợp khí B gồm có H 2 và khí CO, tỉ khối của hỗn hợp khí B đối với H 2 là 3,6.
Tính thành phần phần trăm theo thể tích của mỗi khí có trong hỗn hợp khí A và B.
Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí
Hỗn hợp khí A : (48x + 32y)/(x+y) = 19,2 x 2 = 38,4
→ 3x = 2y → 40% O 3 và 60% O 2
Đặt x và y là số mol H 2 và CO có trong 1 mol hỗn hợp khí
Hỗn hợp khí B : (2x + 28y)/(x+y) = 3,6 x 2 = 7,2
→ x = 4y → 80% H 2 và 20% CO
Đúng 0
Bình luận (1)
Hỗn hợp khí gồm NO 2 và NO có tỉ khối so với khí hidro là 18,2. Hãy xác định phần trăm theo thể tích, phần trăm theo khối lượng của mỗi khí trong hỗn hợp ban đầu
Xem chi tiết
\(Đặt:n_{hh}=1\left(mol\right)\)
\(n_{NO_2}=a\left(mol\right),n_{NO}=b\left(mol\right)\)
\(\Leftrightarrow a+b=1\left(1\right)\)
\(\overline{M}=\dfrac{46a+30b}{a+b}=18.2\cdot2=36.4\)
\(\Leftrightarrow46a+30b=36.4\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.4,b=0.6\)
Tới đây tự tính tiếp nhé !!
Đúng 3
Bình luận (0)
Ta có: \(\overline{M}_{hh}=18,2\cdot2=36,4\left(đvC\right)\)
Theo sơ đồ đường chéo: \(\dfrac{n_{NO_2}}{n_{NO}}=\dfrac{6,4}{9,6}=\dfrac{2}{3}\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{NO_2}=\dfrac{2}{5}\cdot100\%=40\%\\\%V_{NO}=60\%\end{matrix}\right.\)
Giả sử \(n_{NO_2}=2\left(mol\right)\) \(\Rightarrow n_{NO}=3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{NO_2}=\dfrac{2\cdot46}{2\cdot46+3\cdot30}\cdot100\%\approx50,55\%\\\%m_{NO}=49,45\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hỗn hợp khí X gồm (CH4 ,CO2 ,O2) cùng đo ở điều kiện nhiệt độ và áp suất ,trong đó tỉ lệ số mol CH4 và CO2 lần lượt là 1:1 biết tỉ khối hỗn hợp X so với Hidro là 15,5
-tính phần trăm thể tích mỗi khí ý trong hỗn hợp X
-Tính phần trăm khối lượng mỗi khí trong hỗn hợp X