Câu 2: Cho phương trình CaCO3 → CO2 + H2O
Để thu được 2,24 lit CO2 thì khối lượng CaCO3 cần dùng là bao nhiêu?

Những câu hỏi liên quan
Câu 1: Cho thanh magie cháy trong không khí thu được hợp chất magie oxit. Biết mMg 7,2 g. Tính khối lượng MgO tạo thành.Mg + O2 MgOCâu 2: Cho phương trình CaCO3 → CO2 + H2OĐể thu được 2,24 lit CO2 thì khối lượng CaCO3 cần dùng là bao nhiêu?Câu 3: Ba + 2HCl → BaCl2 + H2Để thu dược 4,16 g BaCl2 cần khối lượng HCl cần dùng là bao nhiêu?Câu 4: Cho 19,6 g H2SO4 phản ứng với nhôm thấy có khí bay lên. Xác định thể tích khí H2 bay lên.Al + H2SO4 Al2(SO4)3 + H2
Đọc tiếp
Câu 1: Cho thanh magie cháy trong không khí thu được hợp chất magie oxit. Biết mMg = 7,2 g. Tính khối lượng MgO tạo thành.
Mg + O2 MgO
Câu 2: Cho phương trình CaCO3 → CO2 + H2O
Để thu được 2,24 lit CO2 thì khối lượng CaCO3 cần dùng là bao nhiêu?
Câu 3: Ba + 2HCl → BaCl2 + H2
Để thu dược 4,16 g BaCl2 cần khối lượng HCl cần dùng là bao nhiêu?
Câu 4: Cho 19,6 g H2SO4 phản ứng với nhôm thấy có khí bay lên. Xác định thể tích khí H2 bay lên.
Al + H2SO4 Al2(SO4)3 + H2
Câu 1:
2Mg + O2 \(\underrightarrow{t^o}\) 2MgO
\(n_{Mg}=\dfrac{7,2}{24}=0,3mol\)
\(\Rightarrow n_{MgO}=\dfrac{0,3.2}{2}=0,3mol\)
\(m_{MgO}=0,3.40=12g\)
Câu 2:
CaCO3 \(\rightarrow\) CO2\(\uparrow\) + CaO
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(\Rightarrow m_{CaCO_3}=0,1.100=10g\)
Câu 3:
Ba + 2HCl \(\rightarrow\) BaCl2 + H2
\(n_{BaCl_2}=\dfrac{4,16}{208}=0,02mol\)
\(\Rightarrow n_{HCl}=0,02.2=0,04mol\)
\(m_{HCl}=0,04.36,5=1,46g\)
Câu 4:
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2mol\)
\(n_{H_2}=\dfrac{0,2.3}{3}=0,2mol\\ V_{H_2}=0,2.22,4=4,48l\)
Đúng 5
Bình luận (3)
chỉ cân câu 1 câu3 4 thôi nha
nếu đc thêm chú thích giúp tui một ti:)))
Đúng 0
Bình luận (0)
1)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\\ n_{MgO}=n_{Mg}=0,3\left(mol\right)\\ m_{MgO}=0,3.40=12\left(g\right)\)
2)
\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\uparrow\\ n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ m_{CaCO_3}=0,1.100=10\left(g\right)\)
3)
\(Ba+2HCl\rightarrow BaCl_2+H_2\uparrow\\ n_{BaCl_2}=\dfrac{4,16}{208}=0,02\left(mol\right)\\ n_{HCl}=0,02.2=0,04\left(mol\right)\\ m_{HCl}=0,04.36,5=1,46\left(g\right)\)
4)
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\\ n_{H_2}=n_{H_2SO_4}=0,2\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
Cho phương trình hóa học:
C
a
C
O
3
→
t
o
C
O
2
+
H
2
O
Để thu được 2,24 lít
C
O
2
ở đktc thì số mol
C
a
C
O...
Đọc tiếp
Cho phương trình hóa học: C a C O 3 → t o C O 2 + H 2 O
Để thu được 2,24 lít C O 2 ở đktc thì số mol C a C O 3 cần dùng là
A. 1 mol
B. 0,1 mol
C. 0,001 mol
D. 2 mol
Đáp án B
n C O 2 = 2 , 24 / 22 , 4 = 0 , 1 m o l C a C O 3 → t o C O 2 + H 2 O 0 , 1 ← 0 , 1 ( m o l )
Đúng 0
Bình luận (0)
Có phương trình hóa học sau: CaCO3 → CaO + CO2. a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO? b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3? c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc). d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Đọc tiếp
Có phương trình hóa học sau:
CaCO3 → CaO + CO2.
a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO?
b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3?
c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc).
d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 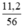 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 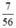 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 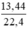 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)
Đúng 0
Bình luận (0)
Có phương trình hóa học sau:
CaCO3 → CaO + CO2.
a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO?
b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3?
c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc).
d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Phương trình hóa học CaCO\(_3\) → CaO + CO\(_2\).
a) nCaO = \(\frac{11,2}{56}\) = 0,2 mol.
Theo PTHH thì nCaCO\(_3\) = nCaO = 0,2 (mol)
b) nCaO = \(\frac{7}{56}\) = 0,125 (mol)
Theo PTHH thì nCaCO\(_3\) = nCaO = 0,125 (mol)
mCaCO\(_3\) = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO\(_2\) = nCaCO\(_3\) = 3,5 (mol)
VCO\(_2\) = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO\(_2\) = \(\frac{13,44}{22,4}\) = 0,6 (mol)
Theo PTHH nCaO = nCaCO\(_3\) = nCO\(_2\) = 0,6 (mol)
mCaCO\(_3\) = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)
#shin
PTHH : CaCO3 --> Cao + CO2
a, nCaO = \(\frac{11,2}{56}=0,2\left(mol\right)\)
Theo PTHH : nCaO = nCaCO3 = 0,2 mol
Vậy : Cần dùng 0,2 mol CaCO3 để điều chế đc 11,2 g CaO
b, Mấy câu sau dễ tự làm
Cho 20 g CaCO3 tác dụng với 400ml dung dịch CH COOH.
a). Viết phương trình hóa học xảy ra.
b). Tính thể tích CO2 thu được (đktc CO )
c.) Tính khối lượng muối thu được sau phản ứng
d) Để điều chế lượng CH3COOH ở trên ta cần dùng bao nhiêu gam butan C.Ho. Biết hiệu suất là 50%.
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\\ a,PTHH:CaCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Ca+CO_2+H_2O\\ b,n_{CO_2}=n_{\left(CH_3COO\right)_2Ca}=n_{CaCO_3}=0,2\left(mol\right)\\ b,V_{CO_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ c,m_{\left(CH_3COO\right)_2Ca}=0,2.158=31,6\left(g\right)\\ d,C_4H_{10}+\dfrac{5}{2}O_2\rightarrow2CH_3COOH+H_2O\\ n_{C_4H_{10}\left(LT\right)}=\dfrac{0,4}{2}=0,2\left(mol\right)\\ n_{C_4H_{10}\left(TT\right)}=0,2:50\%=0,4\left(mol\right)\\ m_{C_4H_{10}\left(tt\right)}=58.0,4=23,2\left(g\right)\)
Đúng 1
Bình luận (0)
Phải dùng bao nhiêu lit
C
O
2
(đktc) để hòa tan hết 20 g
C
a
C
O
3
trong nước, giả sử chỉ có 50%
C
O
2
tác dụng. Phải thêm tối thiểu bao nhiêu lit dd
C
a
O
H
2
0,01 M vào dung dịch sau phản ứng để thu...
Đọc tiếp
Phải dùng bao nhiêu lit C O 2 (đktc) để hòa tan hết 20 g C a C O 3 trong nước, giả sử chỉ có 50% C O 2 tác dụng. Phải thêm tối thiểu bao nhiêu lit dd C a O H 2 0,01 M vào dung dịch sau phản ứng để thu được kết tủa tối đa. Tính khối lượng kết tủa:
A. 4,48 lit C O 2 , 10 lit dd C a O H 2 , 40 g kết tủa.
B. 8,96 lit C O 2 , 10 lit dd C a O H 2 , 40 g kết tủa.
C. 8,96 lit C O 2 , 20 lit dd C a O H 2 40 g kết tủa.
D. 4,48 lit C O 2 , 12 lit dd C a O H 2 , 30 g kết tủa.
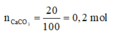
C O 2 + C a C O 3 + H 2 O → C a H C O 3 2
x……….x………..x
Theo PTHH ta có:
n C O 2 l t = x = n C a C O 3 =0,2mol
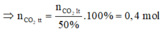
⇒ V C O 2 t t = 0,4.22,4 = 8,96 lit
Ta lại có:
C a O H 2 + C a H C O 3 2 → 2 C a C O 3 + 2 H 2 O
x………..x………2x
Vậy tối thiểu cần là x = 0,2 mol ⇒
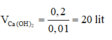
n C a C O 3 = 2x = 0,4 mol
⇒ m↓ = 0,4.100 = 40g
⇒ Chọn C.
Đúng 0
Bình luận (0)
có PTHH sau CaCO3->CaO+CO2
a, nếu có 30 gam CaCO3 phản ứng thì thu dược bao nhiêu gam CaO và bao nhiêu lít CO2(đktc)
b,để thu được 0,3 mol CaO cần bao nhiêu gam CaCO3 phản ứng? Thể tích CO2 thu được(đktc) là bao nhiêu lít?
c, Nếu thu được 33,6 lít CO2(đktc) thì khối lượng chất rắn ttham gia phản ứng, khối lượng chất rắn tạo thành là bao nhiêu gam
Theo PTHH: \(n_{CaCO_3}=n_{CaO}=n_{CO_2}\)
a) \(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)=n_{CaO}=n_{CO_2}\) \(\Rightarrow\left\{{}\begin{matrix}m_{CaO}=0,3\cdot56=16,8\left(g\right)\\V_{CO_2}=0,3\cdot22,4=6,72\left(l\right)\end{matrix}\right.\)
b) Tương tự câu a
c) \(n_{CO_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)=n_{CaO}=n_{CaCO_3}\) \(\Rightarrow\left\{{}\begin{matrix}m_{CaCO_3}=1,5\cdot100=150\left(g\right)\\m_{CaO}=1,5\cdot56=84\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
a. \(CaCO_3\rightarrow CaO+CO_2\)
\(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
- Cứ 1 mol CaCO3 sẽ tạo ra 1 mol CaO và 1 mol CO2.
=> 0,3 mol CaCO3 sẽ tạo ra 0,3 mol CaO và 0,3 mol CO2.
\(m_{CaO}=0,3.56=16,8\left(g\right)\)
\(V_{CO_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 1
Bình luận (0)
2. Nung đá vôi thu được vôi sống và khí carbon dioxide: CaCO3 → CaO + CO2 Tính khối lượng CaCO3 cần dùng để điều chế được 42 gam CaO
`n_(CaO) = m/M=42/(40+16)=0,75(mol)`
`PTHH: CaCO_3 -> CaO + CO_2`
tỉ lệ 1 ; 1 : 1
n(mol) 0,75<----------0,75--->0,75
`m_(CaCO_3)=nxxM=0,75xx(40+12+16xx3)=75(g)`
Đúng 3
Bình luận (0)
Bài 1: Tính thể tích khí oxi ở đktc cần dùng để đốt cháy 11,6 gam C4H10 và tính khối lượng của CO2 và H2O sinh raBài 2. Nung 100 gam CaCO3 thu được 11,2 lít khí CO2 đktc. Tính khối lượng CaO sinh ra và % CaCO3 đã phân hủyBài 3. Cho 12 gam Mg vào dung dịch HCl thu được 4,48 lít khí hidro ở đktc, Tính khối lượng muối MgCl2 sinh ra.Mình đang Cần Khá Gấp Ạ Cảm Ơn
Đọc tiếp
Bài 1: Tính thể tích khí oxi ở đktc cần dùng để đốt cháy 11,6 gam C4H10 và tính khối lượng của CO2 và H2O sinh ra
Bài 2. Nung 100 gam CaCO3 thu được 11,2 lít khí CO2 đktc. Tính khối lượng CaO sinh ra và % CaCO3 đã phân hủy
Bài 3. Cho 12 gam Mg vào dung dịch HCl thu được 4,48 lít khí hidro ở đktc, Tính khối lượng muối MgCl2 sinh ra.
Mình đang Cần Khá Gấp Ạ Cảm Ơn
Bài 1:
PTHH: \(2C_4H_{10}+13O_2\xrightarrow[]{t^o}8CO_2+10H_2O\)
Ta có: \(n_{C_4H_{10}}=\dfrac{11,6}{58}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}=0,8\left(mol\right)\\n_{H_2O}=1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{CO_2}=0,8\cdot44=35,2\left(g\right)\\m_{H_2O}=1\cdot18=18\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Bài 2:
PTHH: \(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\uparrow\)
Ta có: \(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)=n_{CaO}=n_{CaCO_3\left(p.ứ\right)}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CaO}=0,5\cdot56=28\left(g\right)\\\%m_{CaCO_3\left(p.ứ\right)}=\dfrac{0,5\cdot100}{100}\cdot100\%=50\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Bài 3:
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
Tính theo sản phẩm
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_{MgCl_2}\) \(\Rightarrow m_{MgCl_2}=0,2\cdot95=19\left(g\right)\)
Đúng 2
Bình luận (0)



















