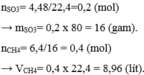Cho VCO2 = 4,48 lít (ở đktc) thì mC=

Những câu hỏi liên quan
Cho Al tác dụng với 100ml dung dịch HCl là 2M thì thể tích khí thu được sau phản ứng (ở đktc) là A.2,24 lít B.6,72 lít C.4,48 lít D.3,36 lít
Câu 2:Tính khối lượng KMnO4 dùng để khi phân hủy thì thu được thể tích khí O2 là 6,72 lít (ở đktc)Câu 3:Cho kẽm tác dụng vừa đủ với HCl. Sau phản ứng thu được 4,48 lít khí hidro ở đktc và muối ZnCl2. tìm khối lượng của kẽm cần dùng cho phản ứng.Câu 4:Cho 22,4g sắt tác dùng vừa đủ với HCl thu được khí hidro và muối FeCl2. Toàn bộ lượng hidro sinh ra cho tác dụng vừa đủ với m (g) CuO. Tìm khối lượng CuO đã tham gia phản ứng (m)
Đọc tiếp
Câu 2:Tính khối lượng KMnO4 dùng để khi phân hủy thì thu được thể tích khí O2 là 6,72 lít (ở đktc)
Câu 3:Cho kẽm tác dụng vừa đủ với HCl. Sau phản ứng thu được 4,48 lít khí hidro ở đktc và muối ZnCl2. tìm khối lượng của kẽm cần dùng cho phản ứng.
Câu 4:Cho 22,4g sắt tác dùng vừa đủ với HCl thu được khí hidro và muối FeCl2. Toàn bộ lượng hidro sinh ra cho tác dụng vừa đủ với m (g) CuO. Tìm khối lượng CuO đã tham gia phản ứng (m)
Câu 2:
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
0,6<------------------------------------0,3
\(\Rightarrow m_{KMnO_4}=0,6.158=94,8\left(g\right)\)
Câu 3:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2<-----------------------0,2
=> mZn = 0,2.65 = 13 (g)
Câu 4:
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,4------------------------->0,4
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
0,4<---0,4
\(\Rightarrow m_{CuO}=0,4.80=32\left(g\right)\)
Đúng 1
Bình luận (0)
a, Tính khối lượng của 2,5 mol CuO b, Tính số mol của 4,48 lít khí CO2 (đktc) c, Tính khối lượng của 4,48 lít khí SO2 (đktc) d, Khối lượng hỗn hợp khí ở đktc gồm 11,2 lít H2 và 5,6 lít O2 là:
a, khối lượng của 2,5 mol CuO là:
\(m=n.M=2,5.80=200\left(g\right)\)
b, số mol của 4,48 lít khí CO2 (đktc) là:
\(n=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Đúng 1
Bình luận (0)
b.nCO2=V/22,4=4,48:22,4=0,2 mol
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
X là kim loại thuộc phân nhóm chính nhóm II (hay nhóm IIA). Cho 10,5 gam hỗn hợp gồm kim loại X và Zn tác dụng với lượng dư dung dịch HCl, sinh ra 4,48 lít khí
H
2
(đktc). Mặt khác, khi cho 6 gam X tác dụng với lượng dư dung dịch
H
2
SO
4
loãng, thì thể tích khí hiđro sinh ra chưa đến 4,48 lít (ở đktc). Kim loại X là A. Ba B. Ca C. Sr D. Mg
Đọc tiếp
X là kim loại thuộc phân nhóm chính nhóm II (hay nhóm IIA). Cho 10,5 gam hỗn hợp gồm kim loại X và Zn tác dụng với lượng dư dung dịch HCl, sinh ra 4,48 lít khí H 2 (đktc). Mặt khác, khi cho 6 gam X tác dụng với lượng dư dung dịch H 2 SO 4 loãng, thì thể tích khí hiđro sinh ra chưa đến 4,48 lít (ở đktc). Kim loại X là
A. Ba
B. Ca
C. Sr
D. Mg
X là kim loại thuộc nhóm IIA. Cho 8 gam hỗn hợp gồm kim loại X và Fe tác dụng với lượng dư dung dịch HCl, sinh ra 4,48 lít khí
H
2
(ở đktc). Mặt khác, khi cho 4,8 gam X tác dụng với lượng dư dung dịch
H
2
S
O
4
loãng, thì thể tích khí hiđro sinh ra chưa đến 5,6 lít (ở đktc). Kimloại X là A. Ba B. Ca C. Sr D. Mg
Đọc tiếp
X là kim loại thuộc nhóm IIA. Cho 8 gam hỗn hợp gồm kim loại X và Fe tác dụng với lượng dư dung dịch HCl, sinh ra 4,48 lít khí H 2 (ở đktc). Mặt khác, khi cho 4,8 gam X tác dụng với lượng dư dung dịch H 2 S O 4 loãng, thì thể tích khí hiđro sinh ra chưa đến 5,6 lít (ở đktc). Kimloại X là
A. Ba
B. Ca
C. Sr
D. Mg
Dẫn từ từ 4,48 lít (ở đktc) c2h4 qua dd brom dư. tính khối lượng brom đã phản ứng (thấy t thì giả mù đi tm ☺️🙏🏻)
\(n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,2---->0,2
=> mBr2 = 0,2.160 = 32 (g)
Đúng 2
Bình luận (0)
Tính khối lượng của 4,48 lít khí S O 3 (ở đktc).
Tính thể tích ở đktc của 6,4 gam khí C H 4 .
Khối lượng nước thu được khi cho 4,48 lít H2 (đktc) tác dụng với 4,48 lít O2 (đktc) là
a. 9g
b. 3,6 g
c. 4,8 g
d. 7,2g
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
\(\dfrac{0,2}{2}\) < \(\dfrac{0,2}{1}\) ( mol )
0,2 0,2 ( mol )
\(m_{H_2O}=0,2.18=3,6g\)
=> Chọn B
Đúng 1
Bình luận (0)
Cho 12,4 gam hỗn hợp Fe, Cu phản ứng vừa đủ với 5,04 lít Cl2 (đktc). Cũng cho 12,4 gam hỗn hợp trên phản ứng với dd HCl dư sinh ra khí H2 có thể tích ở đktc là: A. 4,48 lítB. 5,04 lítC. 1,12 lítD. 1,68 lít
Gọi số mol Fe, Cu là a, b (mol)
=> 56a + 64b = 12,4 (1)
PTHH: 2Fe + 3Cl2 --to--> 2FeCl3
a---->1,5a
Cu + Cl2 --to--> CuCl2
b--->b
=> 1,5a + b = \(\dfrac{5,04}{22,4}=0,225\) (2)
(1)(2) => a = 0,05 (mol); b = 0,15 (mol)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,05------------------>0,05
=> VH2 = 0,05.22,4 = 1,12 (l)
=> C
Đúng 3
Bình luận (0)