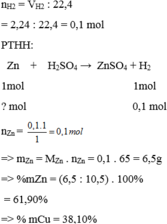
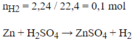Câu 34:Cho , g h n hợp 2 kim loại Cu và Zn vào dd H2SO4loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần theo khối lượng của Cu và Zn lần lượt là:A. 61,9% và 38,1%B. 38,1 % và 61,9%C. 65% và 35%D. 35% và 65%

Những câu hỏi liên quan
Cho 10,5 gam hỗn hợp hai kim loại Zn, Cu vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là:
A. 61,9% và 38,1% B. 63% và 37%
C. 61,5% và 38,5 D. 65% và 35%
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
Theo PTHH :
$n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$\%m_{Zn} = \dfrac{0,1.65}{10,5}.100\% = 61,9\%$
Chọn đáp án A
Đúng 2
Bình luận (0)
Cho 10,5g hỗn hợp 2 kim loại Cu và Zn vào dd H 2 S O 4 loãng dư, người ta thu được 2,24 lít khí (đktc). Hãy tính thành phần % theo khối lượng của Cu và Zn
: Cho 10,5g hỗn hợp 2 kim loại Cu và Zn vào dd H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Hãy tính thành phần % theo khối lượng của Cu và Zn .
Đọc tiếp
: Cho 10,5g hỗn hợp 2 kim loại Cu và Zn vào dd H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Hãy tính thành phần % theo khối lượng của Cu và Zn .
Cu ko phản ứng với H2SO4 loãng
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\Rightarrow m_{Cu}=4\left(g\right)\)
\(\Rightarrow\%Zn=\dfrac{6,5}{10,5}=62\%;\%Cu=100\%-62\%=28\%\)
Đúng 1
Bình luận (0)
https://hoidap247.com/cau-hoi/1072966
Đúng 0
Bình luận (0)
Câu 1: Cho 10,5 gam hỗn hợp 2 kim loại Zn, Cu vào dd H2SO4 loãng dư, người ta thu được 2,24 lít (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu:
A. 61,9% và 38,1% B. 63% và 37% C. 61,5% và 38,5% D. 65% và 35%
Câu 2: Hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 100 ml dd HCl 3M. Thành phần phần trăm theo khối lượng 2 oxit trên lần lượt là:
A. 33,06% và 66,94% B. 66,94% và 33,06% C. 33,47% và 66,...
Đọc tiếp
Câu 1: Cho 10,5 gam hỗn hợp 2 kim loại Zn, Cu vào dd H2SO4 loãng dư, người ta thu được 2,24 lít (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu:
A. 61,9% và 38,1% B. 63% và 37% C. 61,5% và 38,5% D. 65% và 35%
Câu 2: Hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 100 ml dd HCl 3M. Thành phần phần trăm theo khối lượng 2 oxit trên lần lượt là:
A. 33,06% và 66,94% B. 66,94% và 33,06% C. 33,47% và 66,53% D. 66,53% và 33,47%
Câu 1: Cho 10,5 gam hỗn hợp 2 kim loại Zn, Cu vào dd H2SO4 loãng dư, người ta thu được 2,24 lít (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu:
A. 61,9% và 38,1% B. 63% và 37% C. 61,5% và 38,5% D. 65% và 35%
Câu 2: Hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 100 ml dd HCl 3M. Thành phần phần trăm theo khối lượng 2 oxit trên lần lượt là:
A. 33,06% và 66,94% B. 66,94% và 33,06% C. 33,47% và 66,53% D. 66,53% và 33,47%
Đúng 0
Bình luận (0)
Cho 10,5 gam hỗn hợp hai kim loại Zn và Cu vào dung dịch
H
2
S
O
4
loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là A. 63% và 37%. B. 61,9% và 38,1%. C. 61,5% và 38,5% D. 65% và 35%
Đọc tiếp
Cho 10,5 gam hỗn hợp hai kim loại Zn và Cu vào dung dịch H 2 S O 4 loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là
A. 63% và 37%.
B. 61,9% và 38,1%.
C. 61,5% và 38,5%
D. 65% và 35%
Chọn B
Chỉ có Zn phản ứng với H 2 S O 4 , Cu không phản ứng

Đúng 0
Bình luận (0)
Cho 10,5 gam hỗn hợp hai kim loại Zn và Cu vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu?
- Cu không tác dụng được với dd H2SO4 loãng.
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{Zn}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow\%m_{Zn}=\dfrac{0,1.65}{10,5}.100\approx61,905\%\\ \Rightarrow\%m_{Cu}\approx38,095\%\)
Đúng 1
Bình luận (1)
Cho 10g hỗn hợp hai kim loại Cu và Zn vào 100ml dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc); biết rằng Cu không phản ứng dung dịch H2SO4 loãng. a) Tính thành phần % theo khối lượng của các kim loại trong hỗn hợp ban đầu. b) Tính nồng độ mol (CM) của dung dịch H2SO4 đã dùng.
Zn+ H2SO4→ ZnSO4+ H2↑
(mol) 0,1 0,1 0,1
a)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(lít\right)\)
→mZn=n.M=0,1.65= 6,5(g)
→mCu= 10- 6,5= 3,5(g)
=> \(\%m_{Zn}=\dfrac{6,5}{10}.100\%=65\%\)
\(\%m_{Cu}=100\%-65\%=35\%\)
b) \(C_{M_{H_2SO_4}}=\dfrac{n}{V}=\dfrac{0,1}{0,1}=1M\)
Đúng 1
Bình luận (0)
Cho 10,5 gam hỗn hợp hai kim loại Cu và Zn vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (ở đktc). Thành phần phần trăm của hỗn hợp kim loại là:
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
_____0,1<-------------------------0,1
=> mZn = 0,1.65 = 6,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{6,5}{10,5}.100\%=61,9\%\\\%Cu=\dfrac{10,5-6,5}{10,5}.100\%=38,1\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 10,5 gam hỗn hợp hai kim loại Zn, Cu vào dung dịch
H
2
S
O
4
loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là: A. 61,9% và 38,1% B. 63% và 37% C. 61,5% và 38,5% D. 65% và 35%
Đọc tiếp
Cho 10,5 gam hỗn hợp hai kim loại Zn, Cu vào dung dịch H 2 S O 4 loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là:
A. 61,9% và 38,1%
B. 63% và 37%
C. 61,5% và 38,5%
D. 65% và 35%