đốt cháy hoàn toàn 0.025 mol HCHC A cần dùng 1.12l O2 dktc dẫn toàn bộ sp cháy thu dc lần lượt vào P2O5 và bình 2 chứa Ca oh 2 dư thấy bình 1 tăng 0.9 g bình 2 tăng 2.2 gam CTPT của HCHC A

Những câu hỏi liên quan
Đốt cháy hoàn toàn 0,1 mol este hai chức X cần V lít O2 (đktc). Sản phẩm đốt cháy được dẫn lần lượt qua bình 1 đựng P2O5 (dư), bình 2 đựng Ca(OH)2 (dư), thấy khối lượng bình 1 tăng 5,4 gam, bình 2 tăng 17,6 gam. Giá trị của V là A. 7,84 B. 3,92 C. 15,68 D. 5,6
Đọc tiếp
Đốt cháy hoàn toàn 0,1 mol este hai chức X cần V lít O2 (đktc). Sản phẩm đốt cháy được dẫn lần lượt qua bình 1 đựng P2O5 (dư), bình 2 đựng Ca(OH)2 (dư), thấy khối lượng bình 1 tăng 5,4 gam, bình 2 tăng 17,6 gam. Giá trị của V là
A. 7,84
B. 3,92
C. 15,68
D. 5,6
Đáp án: A
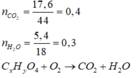
Bảo toàn nguyên tử oxi
2 n O 2 = 2 n C O 2 + n H 2 O - 4 n X ⇒ n O 2 = 0 , 35 ⇒ V = 7 , 84
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,1 mol este hai chức X cần V lít O2 (đktc). Sản phẩm đốt cháy được dẫn lần lượt qua bình 1 đựng P2O5 (dư), bình 2 đựng Ca(OH)2 (dư), thấy khối lượng bình 1 tăng 5,4 gam, bình 2 tăng 17,6 gam. Giá trị của V là A. 7,84 B. 3,92 C. 15,68 D. 5,6
Đọc tiếp
Đốt cháy hoàn toàn 0,1 mol este hai chức X cần V lít O2 (đktc). Sản phẩm đốt cháy được dẫn lần lượt qua bình 1 đựng P2O5 (dư), bình 2 đựng Ca(OH)2 (dư), thấy khối lượng bình 1 tăng 5,4 gam, bình 2 tăng 17,6 gam. Giá trị của V là
A. 7,84
B. 3,92
C. 15,68
D. 5,6
Đoota cháy hoàn toàn 0,1mol este 3 chức X cần 11,2 lít O2(đktc) . Sp cháy thu đc dẫn lần lượt qua bình 1 đựng P2O5(dư) bìn 2 đựng Ca (OH)2 dư thấy khối lượng bình 1 tăng m gam, bình 2 tăng 26,4g . Giá trị m
\(m_{CO_2}=26.4\left(g\right)\Rightarrow n_{CO_2}=\dfrac{26.4}{44}=0.6\left(mol\right)\)
\(n_{O_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
Bảo toàn nguyên tố O :
\(n_{H_2O}=0.1\cdot6+0.5\cdot2-0.6\cdot2=0.4\left(mol\right)\)
\(m=0.4\cdot18=7.2\left(g\right)\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 4,6g HCHC X (chỉ chứa C H O). dẫn sp cháy lần lượt qua bình 1 đựng dd h2so4 đặc, bình 2 đựng dd koh dư. sau thí nghiệm, KL bình 1 tăng 5,4g, kl bình 2 tăng 8,8g. tỉ khối X đối với H là 23. xác định CTPT của X
Xem chi tiết
KL bình 1 tăng = m H2O = 5,4 gam (vì H2SO4 đặc hút nước mạnh) ==> nH2O = 0,3 mol , nH = 2 nH2O = 0,6 mol
KL bình 2 tăng = mCO2 = 8,8 gam ==> nCO2 = 0,2 mol, nC = nCO2 = 0,2 mol
mC + mH = 0,2.12 + 0,6.1 = 3 gam .
Mà mX = mC + mH + mO
==> mO = 4,6 - 3 = 1,6 gam , nO = 0,1 mol
Ta có nC : nH : nO = 0,2 : 0,6: 0,1 = 2:6:1
CTĐGN của X là : C2H6O
X có tỉ khối so với H2 =23 ==> MX = 2.23 = 46
CTPT của X có dạng : (C2H6O)n = 46 ==> (2.12 + 6 + 16 )n = 46
==> n = 1 , CTPT của X trùng với CTĐGN là C2H6O
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,66g chất X cần 9,072lít O2( đktc). Sản phẩm cháy được dẫn qua bình 1 chứa H2SO4đ, bình 2 chứa Ca(OH)2 dư, thấy bình 1 tăng 3,78g; bình 2 tăng m gam và có a(g) kết tủa.
Tính m? a? Xác định CTPT của X biết MX < 250
đót cháy hoàn toàn 0,1 mol este hai chức X cần V lit O2.sản phẩm đốt cháy được dẫn lần lượt qua bình 1 đựng P2O5(dư).bình 2 đựng Ca(OH)2 (dư),thấy khối lượng bình 1 tăng5,4g,bình 2 tăng 17,6g.giá trị của V là
mình làm thế này, bn xem thử nhé:
mb1 tăng 5.4g==>mH2O=5.4(g)==>nH2O=0.3(mol)
mb2 tăng 17.6g==>mCO2=17.6(g)==>nCO2=0.4(mol)
áp dụng bảo toàn nguyên tố oxi: 4.0,1+2.V/22.4=0,3+0,4.2==>V=7,84(L)![]()
Đúng 0
Bình luận (2)
Đốt cháy hoàn toàn 6 g một chất hữu cơ X trong oxi dư. Sau phản ứng, dẫn hh lần lượt qua bình 1 chứa P2O5 khan và bình 2 chứa Ca(OH)2 (đều lấy dư) thì thấy khối lượng bình 1 tăng 3,6 g còn bình 2 tăng 8,8 g. Xác định CTPT và viết CTCT của X, biết tỉ khối của X so với nitơ oxit là 2.
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
Bảo toàn C: nC = 0,2 (mol)
Bảo toàn H: nH = 0,4 (mol)
=> \(n_O=\dfrac{6-0,2.12-0,4.1}{16}=0,2\left(mol\right)\)
nC : nH : nO = 0,2 : 0,4 : 0,2 = 1 : 2 : 1
=> CTPT: (CH2O)n
Mà MX = 2.30 = 60 (g/mol)
=> n = 2
=> CTPT: C2H4O2
CTCT:
(1) CH3COOH
(2) HCOOCH3
(3) HO-CH2-CHO
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 0,1mol este no mạch hở X cần V lít O2 ( đktc) . Sản phẩm đốt cháy đc dẫn lần lượt qua bình 1 đựng P2O5 ( dư) , bình 2 đựng Ca(OH)2 dư thấy khối lượng bình 1 tăng 5,4g bình 2 tăng 17,6g . Giá trị V là?
$n_{H_2O} = \dfrac{5,4}{18} = 0,3(mol)$
$n_{CO_2} = \dfrac{17,6}{44} = 0,4(mol)$
Ta có :
$n_{CO_2} - n_{H_2O} = (k-1).n_X$
Suy ra :$0,4 - 0,3 = (k - 1)0,1 \Rightarrow k = 2$
Vậy X là este no, hai chức
Bảo toàn O :
$4n_X + 2n_{O_2} = 2n_{CO_2} + n_{H_2O}$
$\Rightarrow n_{O_2} = \dfrac{0,4.2 + 0,3 -0,1.4}{2} = 0,35(mol)$
$V = 0,35.22,4 = 7,84(lít)$
Đúng 2
Bình luận (0)
Câu 6: Đốt cháy hoàn toàn một hiđrocacbon X, dẫn toàn bộ sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc, bình 2 đựng dd Ca (OH) 2 dư, thì khối lượng bình 1 tăng lên 9 gam, bình 2 tăng lên 22 gam. Xác định CTPT của X. biết khối lượng mol của X nhỏ hơn 30.
Ta có: \(n_{H_2O}=\dfrac{9}{18}=0,5\left(mol\right)\Rightarrow n_H=0,5.2=1\left(mol\right)\)
\(n_{CO_2}=\dfrac{22}{44}=0,5\left(mol\right)=n_C\)
Gọi CTPT của X là CxHy.
⇒ x:y = 0,5:1 = 1:2
→ CTPT của X có dạng là (CH2)n. ( n nguyên dương)
Mà: MX < 30
\(\Rightarrow n< \dfrac{30}{12+2.1}=2,14\)
n = 1 → không thỏa mãn hóa trị của C.
n = 2 (tm)
Vậy: CTPT của X là C2H4.
Đúng 2
Bình luận (0)
Đốt cháy hết 9,2 gam một chất hữu cơ X bằng khí O2 vừa đủ, thu đuợc hỗn hợp khí và hơi. Dẫn toàn bộ sản phẩm thu được lần lượt qua bình 1 chứa H2SO4 đậm đặc dư và bình 2 chứa dung dịch nước vôi trong dư thì bình 1 tăng m1 gam, còn bình 2 tăng 17,6 gam. Cũng đốt cháy một lượng chất X như trên, nhưng dẫn hỗn hợp khí sau khi đốt cháy lần luợt qua bình 1 chứa CaO dư và bình 2 chứa P2O5 dư thì thấy bình 1 tăng lên 28,4 gam, còn bình 2 tăng lên m2 gam. Công thức phân tử của chất X là: A. C3H6O2 B. C2...
Đọc tiếp
Đốt cháy hết 9,2 gam một chất hữu cơ X bằng khí O2 vừa đủ, thu đuợc hỗn hợp khí và hơi. Dẫn toàn bộ sản phẩm thu được lần lượt qua bình 1 chứa H2SO4 đậm đặc dư và bình 2 chứa dung dịch nước vôi trong dư thì bình 1 tăng m1 gam, còn bình 2 tăng 17,6 gam. Cũng đốt cháy một lượng chất X như trên, nhưng dẫn hỗn hợp khí sau khi đốt cháy lần luợt qua bình 1 chứa CaO dư và bình 2 chứa P2O5 dư thì thấy bình 1 tăng lên 28,4 gam, còn bình 2 tăng lên m2 gam. Công thức phân tử của chất X là:
A. C3H6O2
B. C2H6O
C. C2H6O2
D. C3H8O
Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
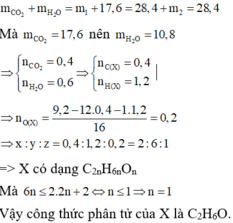
Đúng 0
Bình luận (0)


















