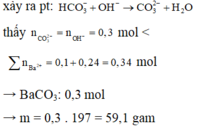Sục V lít CO2 vào 200ml dd hỗn hợp KOH 0,5M và Ba(OH)2 0,375M thu được 11,82 gam kết tủa. Tính V

Những câu hỏi liên quan
Sục V lít CO2 vào 200ml dd hỗn hợp KOH 0,5M và Ba(OH)2 0,375M thu được 11,82 gam kết tủa. Tính V
nBaCO3=11,82.197=0,06mol
nKOH=0,2.0,5=0,1mol;
nBa(OH)2=0,2.0,375=0,075mol
→nOH−=nKOH+2nBa(OH)2=0,1+2.0,075=0,25mol
Ta có: nBaCO3<nBa(OH)2→CO32-phản ứng hết, Ba2+ dư.
→nCO32-=0,06mol
Mặt khác: nOH−>2n↓→ có hai trường hợp.
TH1: CO2phản ứng hết, OH- dư, chỉ tạo muối CO32-
Bảo toàn nguyên tố C: nCO2=nCO32-=0,06mol
→VCO2=0,06.22,4=1,344l
TH2:CO2,OH− đều phản ứng hết, tạo hai muối HCO3;CO32-
Phương trình hóa học:
CO2+OH−→HCO3−
0,13←0,13mol
CO2+2OH−→CO32-+H2O
0,06 0,06←0,06mol
→nCO2=0,13+0,06=0,19mol
→VCO2=0,19.22,4=4,256(l)
Đúng 0
Bình luận (0)
Sục 5,6 lít khí CO2 (đktc) vào 200ml dung dịch hỗn hợp NaOH 1M, Ba(OH)2 0,5M, KOH 0,5M. Kết thúc phản ứng thu được m gam kết tủa. Trị số của m là:
A. 49,25 gam
B. 21,7 gam
C. 54,25 gam
D. 19,7 gam
Đáp án D
Ta có: nCO2= 5,6/22,4=0,25 mol
nBa(OH)2= 0,2. 0,5= 0,1 mol;
nNaOH= 0,2.1= 0,2 mol;
nKOH= 0,2.0,5= 0,1 mol
nOH-= 0,1.2 + 0,2 + 0,1= 0,5 mol; nBa2+= 0,1 mol
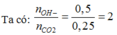
→ CO2 phản ứng với OH- theo PT sau:
CO2+ 2OH- → CO32-+ H2O (1)
0,25 0,5 0,25 mol
Ba2++ CO32- → BaCO3 (2)
Ta có 0,1 < 0,25 nên Ba2+ phản ứng hết
→ nBaCO3= nBa2+= 0,1 mol
→ mBaCO3= 0,1.197= 19,7 gam
Đúng 0
Bình luận (0)
Nhỏ từ từ 200ml dd X có chứa HCl 2M và NaHSO4 0,5M vào 100ml dd Y chứa Na2CO3 2M và K2CO3 1M, sau khi phản ứng xảy ra hoàn toàn thu được V lít CO2 và dd Z, nhỏ tiếp Ba(OH)2 đến dư vào dd Z thì thu được m gam kết tủa. Tính V,m ?
Đốt cháy hoàn toàn m gam một mẫu than chứa 4% tạp chất bằng oxi , thu được 1,12 lít hỗn hợp 2 khí (đktc). Sục từ từ hỗn hợp khí đó vào 200ml dd Ba(OH)2 1M. Sau phản ứng thu được 29,55 gam kết tủa. Tìm m và V của oxi đã dùng.
$n_{Ba(OH)_2}= 0,2(mol)$
$n_{BaCO_3} = 0,15(mol)$
TH1 : $Ba(OH)_2$ dư
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
$n_{CO_2} = n_{BaCO_3} = 0,15(mol) > n_{hh\ khí} = 0,05$(loại)
TH2 : Kết tủa bị hòa tan 1 phần
$n_{Ba(HCO_3)_2} = n_{Ba(OH)_2} - n_{BaCO_3} = 0,05(mol)$
$n_{CO_2} = n_{BaCO_3} + 2n_{Ba(HCO_3)_2} = 0,3(mol) >n_{hh}$
(Sai đề)
Đúng 2
Bình luận (0)
Sục 13,44 lít CO2 (đktc) vào 200ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được dung dịch Y. Cho dung dịch Y tác dụng với 200ml dung dịch hỗn hợp BaCl2 1,2M và KOH 1,5M thu được m gam kết tủa. Giá trị của m là A. 66,98 B. 39,40 C. 47,28. D. 59,10
Đọc tiếp
Sục 13,44 lít CO2 (đktc) vào 200ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được dung dịch Y. Cho dung dịch Y tác dụng với 200ml dung dịch hỗn hợp BaCl2 1,2M và KOH 1,5M thu được m gam kết tủa. Giá trị của m là
A. 66,98
B. 39,40
C. 47,28.
D. 59,10
Sục 13,44 lít CO2 (đktc) vào 200ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được dung dịch Y. Cho dung dịch Y tác dụng với 200ml dung dịch hỗn hợp BaCl2 1,2M và KOH 1,5M thu được m gam kết tủa. Giá trị của m là A. 66,98. B. 39,40. C. 47,28. D. 59,10.
Đọc tiếp
Sục 13,44 lít CO2 (đktc) vào 200ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được dung dịch Y. Cho dung dịch Y tác dụng với 200ml dung dịch hỗn hợp BaCl2 1,2M và KOH 1,5M thu được m gam kết tủa. Giá trị của m là
A. 66,98.
B. 39,40.
C. 47,28.
D. 59,10.
Sục 9,52 lít SO2 (đktc ) vào 200ml dung dịch hỗn hợp : NaOH 1M - Ba(OH)2 0,5M - KOH 0,5M . Kết thcs phản ứng thu được m gam kết tủa . Trị số của m là
n NaOH= 0,2 mol, n KOH=0,1 mol , n Ba(OH)2= 0,1 mol , nSO2=0,425 mol
Ta có :
Ba(OH)2 + SO2--> BaSO3 + H2O
0,1 ----> 0,1----> 0,1 mol
2 NaOH + SO2 ---> Na2SO3 + H2O
0,2 mol ->0,1 mol ---> 0,1 mol
2 KOH + SO2 --> K2SO3 + H2O
0,1 --> 0,05 --> 0,05
Sau 3 phản ứng trên n SO2 dư= 0,425- (0,1+0,1+0,05)=0,175 mol nên xảy ra phản ứng tạo muối axit
Na2SO3 + SO2 + H2O --> 2 NaHSO3
0,1 -------> 0,1
K2SO3 + SO2 + H2O ---> 2KHSO3
0,05 --> 0,05
Sau 2 phản ứng trên n SO2 còn lại = 0,175 - (0,1+0,05)=0,025 mol
BaCO3 + SO2 + H2O --> Ba(HSO3)2
0,025 <---0,025
Số mol kết tủa còn lại là: n BaSO3=0,1-0,025 =0,075 mol => m kết tủa thu được= 0,075.217=16,275 g
Đúng 0
Bình luận (0)
Sục từ từ V lít khí CO2 (đktc) vào 300ml dung dich chứa Ba(OH)2 0,1 M và KOH 0,2 M thu được 5,91 gam kết tủa. Tính V.
\(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,1.0,3=0,03\left(mol\right)\\n_{KOH}=0,2.0,3=0,06\left(mol\right)\end{matrix}\right.\)
\(n_{BaCO_3}=\dfrac{5,91}{197}=0,03\left(mol\right)\)
Do nBaCO3 = nBa(OH)2 => Ba2+ bị kết tủa hết
PTHH:
(1) Ba(OH)2 + CO2 --> BaCO3 + H2O
(2) 2NaOH + CO2 --> Na2CO3 + H2O
(3) Na2CO3 + CO2 + H2O --> 2NaHCO3
- Nếu CO2 chỉ tham gia vào pư (1)
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,03<---0,03
=> nCO2(min) = 0,03 (mol) (*)
- Nếu CO2 tham gia vào pư (1), (2), (3)
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,03----->0,03----->0,03
2NaOH + CO2 --> Na2CO3 + H2O
0,06--->0,03------>0,03
Na2CO3 + CO2 + H2O --> 2NaHCO3
0,03---->0,03
=> nCO2(max) = 0,09 (mol) (**)
(*)(**) => \(0,03\le n_{CO_2}\le0,09\)
=> \(0,672\le V\le2,016\)
Đúng 3
Bình luận (0)
Sục V lít CO2 ở ĐKTC vào 100ml hỗn hợp dd NaOH 2M và Ba(OH)2 0,5M kết thúc phản ứng thu được 3,94g kết tủa.Tính VCO2