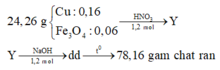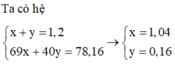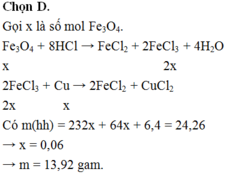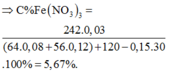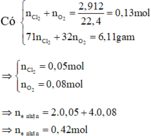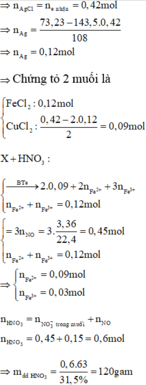Hòa tan hết 24,16 gam hỗn hợp X gồm Cu và Fe3O4 trong dung dịch HCl loãng dư thấy còn lại 6,4 gam Cu không tan. Mặt khác hòa tan hết 24,16 gam hỗn hợp trên trong 240 gam dung dịch HNO3 31,5% (dùng dư) thu được dung dịch Y. Cho 600 ml dung dịch NaOH 2M vào dung dịch Y. Lọc bỏ kết tủa, cô cạn dung dịch nước lọc, sau đó nung tới khối lượng không đôi thu được 78,16 gam rắn khan. Nồng độ C% của Cu(NO3)2 trong dung dịch Y có giá trị gần nhất với
A. 11,60%.
B. 11,65%.
C. 11,70%.
D. 11,55%.