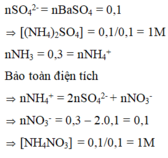Cho dung dịch Ba(OH)2 đến dư vào 200 ml (NH4)2SO4 0,4M. Đun nóng nhẹ, thu được thể tích khí thoát ra (đktc) và khối lượng kết tủa là:

Những câu hỏi liên quan
Cho dung dịch NaOH dư vào 150 ml dung dịch (NH4)2SO4 1M. Đun nóng nhẹ, thể tích khí thoát ra ở đktc là
A. 4,48 lít
B. 3,36 lít
C. 6,72 lít
D. 7,62 lít
Cho dung dịch KOH dư vào 50ml dung dịch
(
NH
4
)
2
SO
4
1M. Đun nóng nhẹ, thu được thể tích khí thoát ra (đktc) A. 2,24 lít B. 1,12 lít C. 0,112 lít D. 4,48 lít
Đọc tiếp
Cho dung dịch KOH dư vào 50ml dung dịch ( NH 4 ) 2 SO 4 1M. Đun nóng nhẹ, thu được thể tích khí thoát ra (đktc)
A. 2,24 lít
B. 1,12 lít
C. 0,112 lít
D. 4,48 lít
Cho dung dịch Ba(OH)2 đến dư vào 100ml dung dịch X có chứa các ion: NH4+, SO42-, NO3- thì có 23,3 gam một kết tủa được tạo thành và đun nóng thì chỉ có 6,72 lít (đktc) một chất khí thoát ra. Nồng độ mol của (NH4)2SO4 và NH4NO3 trong dung dịch X là bao nhiêu? A. 2M và 2M B. 1M và 1M C. 1M và 2M D. 2M và 2M
Đọc tiếp
Cho dung dịch Ba(OH)2 đến dư vào 100ml dung dịch X có chứa các ion: NH4+, SO42-, NO3- thì có 23,3 gam một kết tủa được tạo thành và đun nóng thì chỉ có 6,72 lít (đktc) một chất khí thoát ra. Nồng độ mol của (NH4)2SO4 và NH4NO3 trong dung dịch X là bao nhiêu?
A. 2M và 2M
B. 1M và 1M
C. 1M và 2M
D. 2M và 2M
Đáp án B
Ba2++ SO42- →BaSO4
0,1 ← 23,3/233
NH4++ OH- →NH3+ H2O
0,3← 0,3
Theo ĐLBT ĐT thì: nNO3(-)=0,1 mol
Vậy dung dịch X có 0,1 mol (NH4)2SO4 và 0,1 mol NH4NO3
Suy ra nồng độ mol (NH4)2SO4 1M và NH4NO3 1M
Đúng 0
Bình luận (0)
Cho dung dịch NaOH dư vào 150 ml dung dịch (NH4)2SO4 1M. Sau khi đun nóng nhẹ, thể tích khí thu được (đktc) là
A. 6,72 lít
B. 7,62 lít
C. 3,36 lít
D. 33,60 lít
Cho 100 gam dung dịch NH4HSO4 11,5% vào 100 gam dung dịch Ba(OH)2 13,68% và đun nhẹ. Thể tích khí (đktc) và khối lượng kết tủa thu được là (giả sử toàn bộ khí sinh ra thoát ra khỏi dung dịch) A. 2,24 lít và 23,3 gam B. 2,244 lít và 18,64 gam C. 1,344 lít và 18,64 gam D. 1,792 lít và 18,64 gam
Đọc tiếp
Cho 100 gam dung dịch NH4HSO4 11,5% vào 100 gam dung dịch Ba(OH)2 13,68% và đun nhẹ. Thể tích khí (đktc) và khối lượng kết tủa thu được là (giả sử toàn bộ khí sinh ra thoát ra khỏi dung dịch)
A. 2,24 lít và 23,3 gam
B. 2,244 lít và 18,64 gam
C. 1,344 lít và 18,64 gam
D. 1,792 lít và 18,64 gam
Cho dung dịch NaOH dư vào 150,0 ml dung dịch (NH4)2SO4 1,00M, đun nóng nhẹ. Tính thể tích khí (đktc) thu được?
n(NH4)2SO4 = 0,15. 1 = 0,15 mol
Theo phương trình: nNH3 = 2. n(NH4)2SO4 = 0,15. 2 = 0,3 mol
VNH3 = 0,3. 22,4 = 6,72 lít
Đúng 0
Bình luận (0)
cho dung dịch KOL đến dư vào 200ml (NH4)2SO4 0,8M. Đun nóng nhẹ, tính thể tích thoát ra được ( đktc )
\(2KOH+\left(NH_4\right)_2SO_4-^{t^o}\rightarrow2NH_3+2H_2O+K_2SO_4\\ n_{NH_3}=2n_{\left(NH_4\right)_2SO_4}=0,32\left(mol\right)\\ \Rightarrow V_{NH_3}=0,32.22,4=7,168\left(l\right)\)
Đúng 1
Bình luận (0)
\(n_{\left(NH_4\right)_2SO_4}=0,8.0,2=0,16\left(mol\right)\)
PTHH: \(2KOH+\left(NH_4\right)_2SO_4\rightarrow K_2SO_4+2NH_3+2H_2O\)
______________0,16----------------------->0,32
=> VNH3 = 0,32.22,4 = 7,168(l)
Đúng 0
Bình luận (0)
Cho dung dịch Ba(OH)2 dư vào 100ml dung dịch X chứa NH4+ ; SO42- ; NO3- rồi đun nóng thu được 23,3gam kết tủa và 6,72 lít khí đktc . Nồng độ mol/lít của (NH4)2SO4 và NH4NO3 lần lượt là: A. 1M và 2M B. 1M và 1M C. 2M và 2M D. 0,5M và 1M
Đọc tiếp
Cho dung dịch Ba(OH)2 dư vào 100ml dung dịch X chứa NH4+ ; SO42- ; NO3- rồi đun nóng thu được 23,3gam kết tủa và 6,72 lít khí đktc . Nồng độ mol/lít của (NH4)2SO4 và NH4NO3 lần lượt là:
A. 1M và 2M
B. 1M và 1M
C. 2M và 2M
D. 0,5M và 1M
nBaSO4 = 0,1 ; nNH3 = 0,3
Ba2+ + SO42- → BaSO4
0,1 ← 0,1 (mol)
NH4+ + OH- → NH3 + H2O
0,3 0,3 (mol)
Bảo toàn ion có nNO3- = 0,1
⇒ n(NH4)2SO4 = 0,1 ; nNH4NO3 = 0,1
⇒ Nồng độ mol/lít của (NH4)2SO4 và NH4NO3 lần lượt là 1M và 1M
Đáp án B.
Đúng 0
Bình luận (0)
Cho dung dịch Ba(OH)2 đến dư vào 100 ml dung dịch X có chứa các ion: NH4+, SO42-, NO3- thì có 23,3 gam một kết tủa được tạo thành và đun nóng thì có 6,72 lít (đktc) một chất khí bay ra. Nồng độ mol/lít của (NH4)2SO4 và NH4NO3 trong dung dịch X là bao nhiêu? A. 2M và 2M. B. 2M và 1M. C. 1M và 2M. D. 1M và 1M.
Đọc tiếp
Cho dung dịch Ba(OH)2 đến dư vào 100 ml dung dịch X có chứa các ion: NH4+, SO42-, NO3- thì có 23,3 gam một kết tủa được tạo thành và đun nóng thì có 6,72 lít (đktc) một chất khí bay ra. Nồng độ mol/lít của (NH4)2SO4 và NH4NO3 trong dung dịch X là bao nhiêu?
A. 2M và 2M.
B. 2M và 1M.
C. 1M và 2M.
D. 1M và 1M.