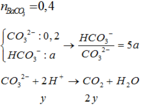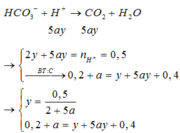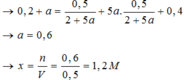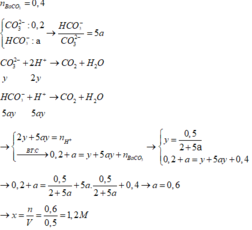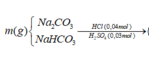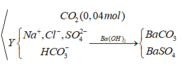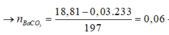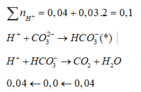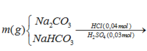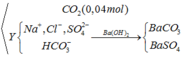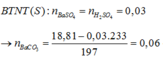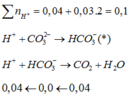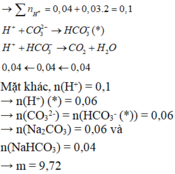Dung dịch Z gồm Na2CO3 0,4M; KHCO3 xM. Thêm từ từ 0,5 lít dung dịch Z vào 500 ml dung dịch HCl 1M sau phản ứng hoàn toàn thu được khí và dung dịch Y. Cho dung dịch Ba(OH)2 dư vào dung dịch Y sau phản ứng hoàn toàn thu được 78,8g kết tủa. Giá trị x là
A. 1,2
B. 1,6
C. 0,8
D. 2