X thuộc chu kì 3, nhóm IA, Y thuộc chu kì 3, nhóm VIIA. Công thức phân tử và bản chất liên kết của hợp chất giữa X và Y là
A. X 2 Y ; liên kết ion B. XY ; liên kết ion.
C. XY 2 ; liên kết cộng hoá trị. D. X 2 Y 2 ; liên kết cộng hoá trị.
nguyên tố X thuộc chu kì 3 nhóm IA , nguyên tố Y thuộc chu kì 3 nhóm VIIA : a) Viết cấu hình electron nguyên tử của các nguyên tố X và Y ; b) Viết sơ đồ hình thành liên kết trong phân tử tạo bởi 2 nguyên tố X và Y
HD:
X là nguyên tố Na: 1s22s22p63s1
Y là nguyên tố Cl: 1s22s22p63s23p5
Na. + Cl (7 e) ---> Na:Cl
Một hợp chất ion có công thức XY. Hai nguyên tố X,Y thuộc 2 chu kì kế cận nhau trong bảng tuần hoàn. X thuộc nhóm IA hoặc IIA, còn Y thuộc VIA hoặc VIIA. Biết tổng số electron trong XY bằng 20. XY là hợp chất nào sau đây
A. NaCl
B. NaF
C. MgO
D. B và C đúng
Đáp án D
Hướng dẫn X thuộc nhóm IA,IIA nên có điện hóa trị +1,+2
Y thuộc cùng nhóm VIA,VIIA nên Y có điện hóa trị -2 và -1
Ngoài ra ZX + ZY = 20. Vì X, Y thuộc hai chu kì kế cận nên nghiệm thích hợp là
ZX = 11 thì ZY = 9 ; X là Na , Y là F và XY là NaF
ZX = 12 thì ZY = 8 ; X là Mg , Y là O và XY là MgO
Cho 3 nguyên tố X, Y, M thuộc nhóm A của bảng tuần hoàn. X, Y cùng một chu kì và thuộc hai nhóm liên tiếp. M, X thuộc cùng một nhóm và ở hai chu kì liên tiếp. Tính kim loại: M > X > Y. Nguyên tử của nguyên tố X có 2 electron lớp ngoài cùng thuộc phân lớp 3s.
a. Viết cấu hình electron nguyên tử của X, Y, M.
b. Viết công thức hiđroxit ứng với oxit bậc cao nhất của Y.
Nguyên tố Y có Z=23, nêu tính chất hóa học cơ bản của Y. Nguyên tố X thuộc chu kì 3, nhóm VIIA của bảng tuần hoàn, xác định cấu tạo nguyên tử nguyên tố X
Cấu hình X: 1s22s22p63s23p5
=> X có 17e,17p,Z=17, có 3 lớp electron và 7 electron hóa trị.
Y thuộc chu kì IV, nhóm VB, là kim loại chuyển tiếp.
=>
Các kim loại chuyển tiếp có 4 tính chất cơ bản:
Tạo hợp chất có màu.Có thể có nhiều trạng thái oxy hóa khác nhau.Là chất xúc tác tốt.Tạo phức chất.Hợp chất A được tạo thành từ 2 nguyên tố X và Y có công thức phân tử là X,Y. X thuộc chu kì 4. Khối lượng phân tử của A là 94 đvC. Loại liên kết hóa học trong phân tử A?
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp ( Z X < Z Y ) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
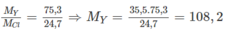
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))
Cho nguyên tố X thuộc chu kì 3 , nhóm IA , nguyên tố Y số e ở phân lớp P là 2 , Nguyên tố Z thuộc nhóm VIA có tổng số hạt cơ bản (p,e,n) là 24
a. Xác định nguyên tố X Y Z
b. viết phương trình tạo thành Ion từ X,Y,Z
c.Giải thích sự tạo thành liên kết giữa X và Z
a/ntố X ở chu kì 3 \(\Rightarrow\)có 3 lớp e.nhóm IA \(\Rightarrow\)CHe kết thúc ở 3s\(^1\)\(\Rightarrow\)CHe là .\(\Rightarrow\) z=......
ntố Y có số e phân lớp P là 2\(\Rightarrow\) CHe kết thúc ở 2p\(^2\) \(\Rightarrow\) CHe là .....
ntố Z có 2Z+N=24.áp dụng công thức Z\(\le\) N\(\le\) 1,5Z.công vào mỗi vế 2Z đẻ có 2z+n=24\(\Rightarrow\) z=.....(có vài trường hợp bạn tự loại nha)
b/ từ phần a là tự suy ra đc mà!GOOD LUCK!
Hợp chất A tạo bởi 3 nguyên tử của 2 nguyên tố thuộc cùng 1 nhóm, ở 2 chu kì liên tiếp, có tổng số proton là 32.
a, Hãy xác định công thức phân tử, công thức cấu tạo và cho biết kiểu liên kết trong A.
b,Trình bày tính chất hóa học của A và viết PTPƯ minh họa.
a) Vì 2 nguyên tố có tổng số proton là 32
=> 2 nguyên tố thuộc chu kì nhỏ
Gọi 2 nguyên tố cần tìm trong A là X, Y
Vì hợp chất A tạo bởi 3 nguyên tử của 2 nguyên tố thuộc cùng 1 nhóm, ở 2 chu kì liên tiếp => CT của A : XY2
Ta có : \(\left\{{}\begin{matrix}Z_X+2Z_Y=32\\\left|Z_X-Z_Y\right|=8\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z_X=16\left(S\right)\\Z_Y=8\left(O\right)\end{matrix}\right.\)
=> CTPT của hợp chất : SO2
CT cấu tạo :
SO2 là liên kết cộng hóa trị có cực
b) Lưu huỳnh đioxit (SO2) mang đầy đủ tính chất hóa học của một oxit axit.
Tính chất hóa học của SO2:
- Tác dụng với nước tạo thành dung dịch axit.
Ví dụ: SO2 + H2O → H2SO3
- Tác dụng với dung dịch bazơ tạo thành muối và nước.
Ví dụ: SO2 + 2NaOH → Na2SO3 + H2O
- Tác dụng với oxit bazơ tạo thành muối.
Ví dụ: SO2 + Na2O → Na2SO3
Một hợp chất có công thức XY2, X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32. Vị trí của X, Y trong BTH là:
A.X: Ô số 7, chu kì 2, nhóm VA; Y: ô số 18, chu kì 2, nhóm VIA
B.X: Ô số 16, chu kì 3, nhóm VIA; Y: ô số 15, chu kì 3, nhóm VA
C.X: Ô số 16, chu kì 3, nhóm VIA; Y: ô số 8, chu kì 2, nhóm VIA
D.X: Ô số 6, chu kì 2, nhóm IVA; Y: ô số 8, chu kì 2, nhóm VIA
X: P, N, E ; Y: P’, N’, E’
Ta có: P=N=E và P’=N’=E’
Trong hợp chất XY2, X chiếm 50% về khối lượng nên: X/2Y = 50/50 → (P+N)/2(P’+N’) = 1 → P=2P’.
Số proton trong XY2 là 32 nên P+2P’=32
→ P=2P’ và P+2P’=32 => P=16 và P’=8 → Hợp chất SO2
S: 1s22s22p63s23p4 => Ô 16, chu kì 3, nhóm VIA
O: 1s22s22p4 => Ô 8, chu kì 2, nhóm VIA