Cho 5,6 gam bột Fe tác dụng với 500 ml dung dịch AgNO3 0,5 M . Tính khối lượng muối thu được:
A. 21,1g
B. 10,55g
C. 42,2g
D. 18g
Cho 5,6 gam bột Fe tác dụng với 500 ml dung dịch AgNO3 0,5 M . Tính khối lượng muối và khối lượng kim loại thu được?
A. 21,1g; 27g.
B. 27g; 21,1g
C. 21g; 27g.
D. 27g; 21g.
Đáp án A.
![]()
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
0,1 0,25 0,1 0,2
→ AgNO3 dư : 0,05 mol , Fe(NO3)2 tạo thành : 0,1 mol
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
0,1 0,05 0,05 0,05
→ Fe(NO3)2 dư : 0,05 mol , Fe(NO3)3 tạo thành 0,05 mol
→ Tổng số mol Ag ở hai phản ứng : 0,25 mol → mAg = 0,25.108 = 27 gam
Khối lượng muối : 0,05.180 + 0,05.242 = 21,1 gam
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D = 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau.
– Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối.
– Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa.
a. Xác định tên kim loại M.
b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X.
c. Tính V và m.
Câu 8: Cho 5,6 gam sắt tác dụng hết với 250 gam dung dịch HCI.
a) Tính khối lượng muối thu được.
b. Tính nồng độ phần trăm axit cần dùng.
c. Tính C% dung dịch muối sau phản ứng.
Cho Fe=56,H=1, Cl=35,5
`Fe + 2HCl -> FeCl_2 + H_2`
`0,1` `0,2` `0,1` `0,1` `(mol)`
`n_[Fe]=[5,6]/56=0,1(mol)`
`a)m_[FeCl_2]=0,1.127=12,7(g)`
`b)C%_[HCl]=[0,2.36,5]/250 . 100=2,92%`
`c)C%_[FeCl_2]=[12,7]/[5,6+250-0,1.2].100~~4,97%`
Cho a gam KMnO4 tác dụng với 100ml dung dịch HCl bM thu được V lít khí Cl2. Lượng khí clo sinh ra tác dụng hết với x gam Fe thu được 39gam muối.
a. Giá trị a, b, x, V = ?
b. Lượng muối trên tác dụng với dung dịch AgNO3 5%, tính khối lượng chất kết tủa thu được, khối lượng dung dịch AgNO3 phản ứng ?
\(a,2KMnO_4+16HCl_{đặc}\rightarrow\left(t^o\right)2KCl+2MnCl_2+5Cl_2+8H_2O\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Ta.có:n_{FeCl_3}=\dfrac{39}{162,5}=0,24\left(mol\right)\\ n_{Fe}=n_{FeCl_3}=0,24\left(mol\right)\\ n_{Cl_2}=\dfrac{3}{2}.0,24=0,36\left(mol\right)\\ n_{K_2MnO_4}=\dfrac{2}{5}.0,36=0,144\left(mol\right)\\ n_{HCl}=\dfrac{16}{5}.0.36=1,152\left(mol\right)\\ \Rightarrow a=m_{KMnO_4}=0,144.158=22,752\left(g\right)\\ b=C_{MddHCl}=\dfrac{1,152}{0,1}=11,52\left(M\right)\\ x=m_{Fe}=0,24.56=13,44\left(g\right)\\ V=V_{Cl_2\left(đktc\right)}=0,36.22,4=8,064\left(l\right) \)
\(b,n_{KCl}=n_{MnCl_2}=\dfrac{2}{5}.0,36=0,144\left(mol\right)\\ KCl+AgNO_3\rightarrow AgCl\downarrow\left(trắng\right)+KNO_3\\ MnCl_2+2AgNO_3\rightarrow2AgCl\downarrow\left(trắng\right)+Mn\left(NO_3\right)_2\\ n_{AgNO_3}=n_{AgCl}=n_{KCl}+2.n_{MnCl_2}=0,144+2.0,144=0,432\left(mol\right)\\ \Rightarrow m_{AgCl\downarrow\left(trắng\right)}=143,5.0,432=61,992\left(g\right)\\ m_{AgNO_3}=0,432.170=73,44\left(g\right)\\ \Rightarrow m_{ddAgNO_3}=\dfrac{73,44.100}{5}=1468,8\left(g\right)\)
Cho m gam hỗn hợp A (dạng bột) gồm Cu và Fe tác dụng với 100 ml dung dịch AgNO3 1M, sau khi phản ứng kết thúc thu được dung dịch Y và 13,36 gam hỗn hợp chất rắn gồm 2 kim loại. Cho dung dịch Y tác dụng với dung dịch NaOH dư thu được kết tủa Z và dung dịch T, lọc bỏ lấy kết tủa Z đem nung trong không khí đến khối lượng không đổi thu được p gam chất rắn. Biết các phản ứng xảy ra hoàn toàn.
a. Tính giá trị của p.
b. Tính khối lượng của kim loại đồng có trong A. Biết m = 5,44 gam
Cho 5,6 gam Fe vào 220 ml dung dịch AgNO3 1M, sau phản ứng thu được dung dịch X. Khối lượng muối Fe(NO3)2 trong X là
A. 3,6
B. 7,2
C. 14,4
D. 18,0
Cho 13,9 gam hỗn hợp X gồm Al, Fe vào 500 ml dung dịch B chứa Cu(NO3)2 và AgNO3. Sau phản ứng hoàn toàn thu được 36,3 gam hỗn hợp kim loại C và dung dịch D. Lọc dung dịch D, chia làm hai phần bằng nhau:
- Phẩn 1: Tác dụng với dung dịch NH3 dư. Lấy kết tủa nung trong không khí đến khối lượng không đổi thu được 8,55 gam chất rắn.
- Phần 2: Tác dụng với dung dịch NaOH dư. Lấy kết tủa nung trong không khí đến khối lượng không đổi thu được 6 gam chất rắn khan.
Nồng độ mol/lít của AgNO3 trong B là:
A. 0,2 M
B. 0,3 M
C. 0,4 M
D. 0,5 M
Đáp án C
Sau phản ứng thu được hỗn hợp kim loại C => Chứng tỏ C chứa Ag, Cu, có thể có Fe dư, Al dư.
Có khối lượng chất rắn thu được ở phần 1 nhiều hơn phần 2 => Chứng tỏ trong dung dịch ngoài Al(NO3)3 còn chứa Fe(NO3)2
=> Al, Cu(NO3)2 và AgNO3 phản ứng hết, Fe có thể còn dư.
Đặt số mol Cu(NO3)2 và AgNO3 lần lượt là a, b.
Đặt số mol Al và Fe phản ứng lần lượt là x, ỵ
Chất rắn thu được ở phần 2 là Fe2O3 => 160.0,5y = 6,2 => y = 0,15
Chất rắn thu được ở phần 1 là Al2O3 và Fe2O3
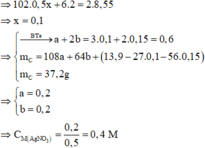
Bài 3: Hòa tan hoàn toàn 8 gam MgO bằng 200 ml dung dịch HCl . a/ Tính nồng độ mol dung dịch HCl cần dùng. b/ Tính khối lượng muối tạo thành.
c/ Cần dùng bao nhiêu ml dd AgNO3 0,5 M để tác dụng hết với lượng muối sinh ra ở phản ứng trên? d/ Tính khối lượng kết tủa thu được.
Cho một khối lượng bột sắt tác dụng vừa đủ với 500 ml dung dịch axit clohiđric có nồng độ 0,2 M a) viết phương trình phản ứng b) xác định khối lượng của sắt đã tham gia phản ứng c) tính khối lượng muối thu được sau phản ứng
\(n_{HCl}=0,2.0,5=0,1(mol)\\ a,Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=n_{FeCl_2}=\dfrac{1}{2}n_{HCl}=0,05(mol)\\ b,m_{Fe}=0,05.56=2,8(g)\\ c,m_{FeCl_2}=0,05.127=6,35(g)\)