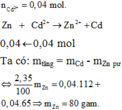Có hai lá kẽm khối lượng như nhau. Một lá cho vào dung dịch đồng(II) nitrat, lá kia cho vào dung dịch chì(II) nitrat. Sau cùng một thời gian phản ứng, khối lượng lá kẽm thứ nhất giảm 0,05 gam. Viết các phương trình hoá học.

Những câu hỏi liên quan
Có hai lá kẽm khối lượng như nhau. Một lá cho vào dung dịch đồng(II) nitrat, lá kia cho vào dung dịch chì(II) nitrat. Sau cùng một thời gian phản ứng, khối lượng lá kẽm thứ nhất giảm 0,05 gam. Khối lượng lá kẽm thứ 2 tăng hay giảm là bao nhiêu gam ? Biết rằng trong cả 2 phản ứng trên, khối lượng kẽm bị hoà tan bằng nhau.
n Zn = x
Theo đầu bài ta có : 65x - 64x = 0,05
=> x = 0,05 (mol) ; m Zn = 0,05 x 65 = 3,25 (gam).
Zn + Pb NO 3 2 → Zn NO 3 2 + Pb↓
0,05 mol 0,05 mol
Khối lượng lá kẽm thứ 2 tăng: ( 0,05 x 207) - 3,25 = 7,1 (gam).
Đúng 0
Bình luận (0)
Có hai lá kẽm khối lượng như nhau. Một lá cho vào dung dịch đồng(II) nitrat, lá kia cho vào dung dịch chì(II) nitrat. Sau cùng một thời gian phản ứng, khối lượng lá kẽm thứ nhất giảm 0,05 gam.
a) Viết các phương trình hoá học.
b) Khối lượng lá kẽm thứ 2 tăng hay giảm là bao nhiêu gam ? Biết rằng trong cả 2 phản ứng trên, khối lượng kẽm bị hoà tan bằng nhau.
Giải:
a, \(Zn+Cu\left(NO_3\right)_2\rightarrow Zn\left(NO_3\right)_2+Cu\downarrow\)
\(x.................................x\)
b, Theo đầu bài ta có: \(65x-64x=0,05\)
\(\Rightarrow x=0,05\left(mol\right)\)
\(m_{Zn}=0,05.65=3,25\left(g\right)\)
\(Zn+Pb\left(NO_3\right)_2\rightarrow Zn\left(NO_2\right)_2+Pb\downarrow\)
\(0,5.............................................0,5\)
Khối lượng lá kẽm thứ 2 tăng:
\(0,05.207-3,25=7,1\left(g\right)\)
Đúng 0
Bình luận (0)
Cho lá kẽm nặng 50g vào dung dịch CuSO4. Sau một thời gian phản ứng, khối lượng lá kẽm còn lại là 49,83g. Khối lượng lá kẽm đã tham gia phản ứng là 11,7%. Giải thích tại sao?
Ngâm một lá kẽm vào dung dịch có hoà tan 8,32 gam CdSO4. Phản ứng xong lấy lá kẽm ra khỏi dung dịch, rửa nhẹ, làm khô thì thấy khối lượng lá kẽm tăng thêm 2,35% so với khối lượng lá kẽm trước phản ứng. Khối lượng lá kẽm trước phản ứng là: A. 80 gam. B. 60 gam C. 20 gam D. 40 gam
Đọc tiếp
Ngâm một lá kẽm vào dung dịch có hoà tan 8,32 gam CdSO4. Phản ứng xong lấy lá kẽm ra khỏi dung dịch, rửa nhẹ, làm khô thì thấy khối lượng lá kẽm tăng thêm 2,35% so với khối lượng lá kẽm trước phản ứng. Khối lượng lá kẽm trước phản ứng là:
A. 80 gam.
B. 60 gam
C. 20 gam
D. 40 gam
Ngâm một lá kẽm vào trong 250ml dung dịch CuSO4 2M đến khi dung dịch không còn màu xanh
a. Viết phương trình hóa học
b. Tính khối lượng kẽm tan ra, khối lượng đồng tạo thành
c. Sau phản ứng thì khối lượng lá kẽm tăng hay giảm bao nhiêu ? Giả thiết đồng sinh ra bám hết vào lá kẽm.
a)
$Zn + CuSO_4 \to ZnSO_4 + Cu$
b)
Theo PTHH : $n_{Zn} = n_{Cu} = n_{CuSO_4} = 0,25.2 = 0,5(mol)$
$m_{Zn} = 0,5.65 = 32,5(gam)$
$m_{Cu} = 0,5.64 = 32(gam)$
c)
Khối lượng thanh kẽm giảm là $32,5 - 32 = 0,5(gam)$
Đúng 1
Bình luận (0)
Cho một lá kẽm có khối lượng 8,5 gam vào dung dịch FeSO4, sau phản ứng lấy lá kẽm ra làm khô, cân được 7,6 gam (giả thiết toàn bộ sắt sinh ra bám hết vào lá kẽm). Lượng Zn đã phản ứng là
A. 13gam.
B. 3,25gam.
C. 6,5gam.
D. 8,7gam.
Đáp án C
Zn + Fe2+ → Zn2+ + Fe
Mol x → x
=> Dmgiảm = mZn pứ - mFe tạo ra
=> 8,5 – 7,6 = 65x – 56x => x = 0,1 mol
=> mZn pứ = 65.0,1 = 6,5g
Đúng 0
Bình luận (0)
Cho một lá đồng có khối lượng là 6 gam vào dung dịch bạc nitrat. Phản ứng xong, đem lá kim loại ra rửa nhẹ, làm khô cân được 13,6 gam. Tính khối lượng đồng đã phản ứng
Khối lượng kim loại tăng : 13,6 - 6 = 7,6 (gam)
Gọi n Cu = x mol
n Ag = 2x mol
Có: 2x x 108 - 64x = 7,6
=> x = 0,05 → m Cu = 0,05 x 64 = 3,2g
Đúng 1
Bình luận (0)
Ngâm một lá sắt có khối lượng 20g vào dung dịch bạc nitrat, sau một thời gian phản ứng nhấc lá kim loại ra làm khô cân nặng 23,2g. Lá kim loại sau phản ứng có: A. 18,88g Fe và 4,32g Ag B. 1,880g Fe và 4,32g Ag C. 15,68g Fe và 4,32g Ag D. 18,88g Fe và 3,42g Ag
Đọc tiếp
Ngâm một lá sắt có khối lượng 20g vào dung dịch bạc nitrat, sau một thời gian phản ứng nhấc lá kim loại ra làm khô cân nặng 23,2g. Lá kim loại sau phản ứng có:
A. 18,88g Fe và 4,32g Ag
B. 1,880g Fe và 4,32g Ag
C. 15,68g Fe và 4,32g Ag
D. 18,88g Fe và 3,42g Ag
Một bạn học sinh tiến hành thí nghiệm sau :- Cho cùng thể tích V ml dung dịch gồm Fe(NO3)3 và AgNO3 vào hai cốc.- Thả vào cốc thứ nhất một lá kẽm và cốc thứ hai một lá đồng và đợi phản ứng xảy ra hoàn toàn.Bạn học sinh đó đã ghi lại những hiện tượng quan sát được như sau :(1) Khối lượng 2 lá kim loại cùng tăng lên.(2) Dung dịch ở cốc thứ nhất có màu trắng xanh.(3) Dung dịch ở cốc thứ hai có màu xanh lam.(4) Có vảy bạc bám vào lá kẽm.(5) Có vảy sắt bám vào lá đồng.Trong các hiện tượng trên, có ba...
Đọc tiếp
Một bạn học sinh tiến hành thí nghiệm sau :
- Cho cùng thể tích V ml dung dịch gồm Fe(NO3)3 và AgNO3 vào hai cốc.
- Thả vào cốc thứ nhất một lá kẽm và cốc thứ hai một lá đồng và đợi phản ứng xảy ra hoàn toàn.
Bạn học sinh đó đã ghi lại những hiện tượng quan sát được như sau :
(1) Khối lượng 2 lá kim loại cùng tăng lên.
(2) Dung dịch ở cốc thứ nhất có màu trắng xanh.
(3) Dung dịch ở cốc thứ hai có màu xanh lam.
(4) Có vảy bạc bám vào lá kẽm.
(5) Có vảy sắt bám vào lá đồng.
Trong các hiện tượng trên, có bao nhiêu hiện tượng được mô tả đúng ?
A. 2
B. 3
C.4
D. 5