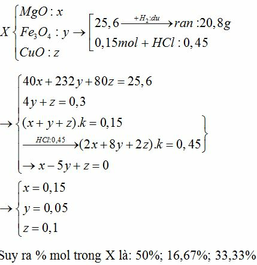Cho luồng khí H2 dư đi qua hỗn hợp X gồm Fe3O4 và CuO nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 29,6 gam chất rắn. Mặt khác, để hòa tan hết lượng X trên cần vừa đủ 600 ml dung dịch HCl 2M. Tính phần trăm khối lượng mỗi chất trong X

Những câu hỏi liên quan
Dẫn luồng khí H2 (dư) đi qua ống sứ đựng 25,6 gam hỗn hợp X gồm Fe3O4, MgO, CuO nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được 20,8 gam chất rắn. Mặt khác, 0,15 mol hỗn hợp X tác dụng vừa đủ với 225 ml dung dịch HCl 2M. Viết c ác phương trình phản ứng xảy ra và tính phần trăm số mol của mỗi chất trong hỗn hợp X
Hoà tan hoàn toàn 12 gam một hỗn hợp X gồm CuO, Fe2O3, MgO phải dùng vừa đủ dung dịch chứa 0,45 mol HC1. Mặt khác, nếu nung nóng 0,175 mol hỗn hợp X và cho một luồng khí CO dư đi qua để phản ứng xảy ra hoàn toàn thì thu được 10 gam chất rắn và khí Y. Tính khối lượng của CuO, Fe2O3, MgO trong 12 gam hỗn hợp X
Gọi: \(\left\{{}\begin{matrix}n_{CuO}=x\left(mol\right)\\n_{Fe_2O_3}=y\left(mol\right)\\n_{MgO}=z\left(mol\right)\end{matrix}\right.\) ⇒ 80x + 160y + 40z = 12 (1)
- Cho X pư với dd HCl.
PT: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
Theo PT: \(n_{HCl}=2n_{CuO}+6n_{Fe_2O_3}+2n_{MgO}=2x+6y+2z=0,45\left(2\right)\)
- Cho CO qua hh nung nóng.
Có: \(kx+ky+kz=0,175\)
PT: \(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
\(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
Theo PT: \(\left\{{}\begin{matrix}n_{Cu}=n_{CuO}=kx\left(mol\right)\\n_{Fe}=2n_{Fe_2O_3}=2ky\left(mol\right)\end{matrix}\right.\)
⇒ 64kx + 56.2ky + 40kz = 10
Ta có: \(\dfrac{kx+ky+kz}{64kx+56.2ky+40kz}=\dfrac{0,175}{10}\) \(\Rightarrow\dfrac{x+y+z}{64x+112y+40z}=\dfrac{7}{400}\)
⇒ 6x + 48y - 15z = 0 (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\y=0,025\left(mol\right)\\z=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CuO}=0,05.80=4\left(g\right)\\m_{Fe_2O_3}=0,025.160=4\left(g\right)\\m_{MgO}=0,1.40=4\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 13,92 gam hỗn hợp X gồm MgO, FeO và Fe2O3 phải dùng vừa hết 520 ml dung dịch HCl 1M. Mặt khác, khi lấy 0,27 mol hỗn hợp X đốt nóng trong ống sứ không có không khí rồi thổi một luồng H2 dư đi qua để phản ứng xảy ra hoàn toàn thì thu được m gam chất rắn và 4,86 gam nước. Xác định m ? A. 16,56 B. 20,88 C. 25,06 D. 16,02
Đọc tiếp
Hòa tan hoàn toàn 13,92 gam hỗn hợp X gồm MgO, FeO và Fe2O3 phải dùng vừa hết 520 ml dung dịch HCl 1M. Mặt khác, khi lấy 0,27 mol hỗn hợp X đốt nóng trong ống sứ không có không khí rồi thổi một luồng H2 dư đi qua để phản ứng xảy ra hoàn toàn thì thu được m gam chất rắn và 4,86 gam nước. Xác định m ?
A. 16,56
B. 20,88
C. 25,06
D. 16,02
Dẫn khi H2 dư đi qua 25.6 gam hỗn hợp X gồm Fe,O, MgO, CuO nung nóng. Sau phản ứng thu được 20,8 gam chất rắn. Mặt khác để hỏa tan hoàn toàn 0,15 mol hỗn hợp X cần dùng vừa đủ dung dịch chứa 16,425 gam HCl. Tính khối lượng mỗi chất trong hỗn hợp ban đầu
giúp mình với, mình cảm ơn ạ
Nung nóng 16,8 gam hỗn hợp gồm Mg, Cu, Al với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X (MgO, CuO, Al2O3). Tính thể tích dung dịch HCl 2M vừa đủ để hòa tan hết chất rắn X ?
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$MgO + 2HCl \to MgCl_2 + H_2O$
$CuO + 2HCl \to CuCl_2 + H_2O$
$Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O$
Gọi $n_{MgO} = a(mol) ; n_{CuO} = b(mol) ; n_{Al_2O_3} = c(mol)$
Bảo toàn khối lượng : $m_{O_2} = 23,2 - 16,8 = 6,4(gam)$
$n_{O_2} = 0,2(mol)$
$\Rightarrow 0,5a + 0,5b + 1,5c = 0,2(1)$
Theo PTHH :
$n_{HCl} =2 n_{MgO} + 2n_{CuO} + 6n_{Al_2O_3} = 0,8(theo (1))$
Suy ra : $V_{dd\ HCl} = \dfrac{0,8}{2} = 0,4(lít)$
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 12 gam hỗn hợp X gồm CuO, Fe2O3, MgO cần dùng vừa đủ 225 ml dung dịch HCl 2M. Mặt khác, nếu đốt nóng 12 gam X trong khí CO dư để phản ứng xảy ra hoàn toàn thì thu được 10 gam chất rắn Y. Phần trăm khối lượng Fe2O3 trong hỗn hợp X bằng: A. 33,33% B. 40,00% C. 66,67% D. 50,00%
Đọc tiếp
Hòa tan hoàn toàn 12 gam hỗn hợp X gồm CuO, Fe2O3, MgO cần dùng vừa đủ 225 ml dung dịch HCl 2M. Mặt khác, nếu đốt nóng 12 gam X trong khí CO dư để phản ứng xảy ra hoàn toàn thì thu được 10 gam chất rắn Y. Phần trăm khối lượng Fe2O3 trong hỗn hợp X bằng:
A. 33,33%
B. 40,00%
C. 66,67%
D. 50,00%
Đáp án A
Khi cho X tác dụng với HCl: nHCl= 0,225.2= 0,45 mol
CuO + 2HCl→ CuCl2+ H2O
Fe2O3+ 6HCl→ 2FeCl3+ 3H2O
MgO + 2HCl→ MgCl2+ H2O
Đặt nCuO = x mol; n F e 2 O 3 = y mol; nMgO = z mol
→ 80x+ 160y +40z= 12 gam (1)
nHCl= 2x+6y+2z= 0,45 mol (2)
C O + C u O → t 0 C u + C O 2 x x m o l F e 2 O 3 + 3 C O → t 0 2 F e + 3 C O 2 y 2 y m o l
Chất rắn Y chứa x mol Cu; 2y mol Fe và z mol MgO
→ 64x + 56.2y + 40z= 10 gam (3)
Từ các PT(1,2,3) ta có x= 0,05; y=0,025; z=0,1
→% m F e 2 O 3 =33,33%
Đúng 0
Bình luận (0)
Để hoà tan hoàn toàn 9,2 gam hỗn hợp X gồm kim loại M và một oxit của kim loại M cần dùng vừa hết 160ml dung dịch HCl 2M, còn nếu dẫn luồng H2 dư đi qua 9,2 gam hỗn hợp X nung nóng, sau khi phản ứng xảy ra hoàn toàn thu được 7,28 gam chất rắn. Tìm công thức của oxit kim loại trong hỗn hợp X.
Cho hỗn hợp A gồm: Fe, CuO, Fe3O4.- Cho khí CO dư đi qua a gam A nung nóng. Sau phản ứng hoàn toàn thu được 2,92 gam chất rắn và 3,136 lít (đktc) hỗn hợp khí X ( gồm CO và CO2 ) có dx/H2 16.- Mặt khác hòa tan hoàn toàn a gam hỗn hợp A cần dùng 100 gam hỗn hợp H2SO4 5,39%. Sau phản ứng kết thúc thu được dung dịch B ( gồm 3 muối sunfat và V lít khí H2 (đktc)).1. Xác định giá trị a và V.2. Tính C% mỗi chất trong dung dịch B.3. Cho lượng dư dung dịch Ba(OH)2 tác dụng với dung dịch B trong môi trườn...
Đọc tiếp
Cho hỗn hợp A gồm: Fe, CuO, Fe3O4.
- Cho khí CO dư đi qua a gam A nung nóng. Sau phản ứng hoàn toàn thu được 2,92 gam chất rắn và 3,136 lít (đktc) hỗn hợp khí X ( gồm CO và CO2 ) có dx/H2 = 16.
- Mặt khác hòa tan hoàn toàn a gam hỗn hợp A cần dùng 100 gam hỗn hợp H2SO4 5,39%. Sau phản ứng kết thúc thu được dung dịch B ( gồm 3 muối sunfat và V lít khí H2 (đktc)).
1. Xác định giá trị a và V.
2. Tính C% mỗi chất trong dung dịch B.
3. Cho lượng dư dung dịch Ba(OH)2 tác dụng với dung dịch B trong môi trường không khí. Khi các phản ứng hóa học xảy ra hoàn toàn, lọc lấy kết tủa làm khô, ẩm được b gam chất rắn khan. Xác định giá trị b.
giúp mình vs:((
1) \(\left\{{}\begin{matrix}n_{CO}+n_{CO_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\\\dfrac{28.n_{CO}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=16.2=32\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{CO}=0,105\left(mol\right)\\n_{CO_2}=0,035\left(mol\right)\end{matrix}\right.\)
nO = nCO2 = 0,035 (mol)
=> a = 2,92 + 0,035.16 = 3,48(g)
\(n_{H_2SO_4}=\dfrac{100.5,39\%}{98}=0,055\left(mol\right)\)
nH2O = nO = 0,035 (mol)
Bảo toàn H: \(n_{H_2}=\dfrac{0,055.2-0,035.2}{2}=0,02\left(mol\right)\)
=> \(V=0,02.22,4=0,448\left(l\right)\)
2) Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Fe_3O_4}=b\left(mol\right)\\n_{CuO}=c\left(mol\right)\end{matrix}\right.\)
=> 56a + 232b + 80c = 3,48 (1)
Bảo toàn Fe: nFe = a + 3b (mol)
Bảo toàn Cu: nCu = c (mol)
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,02<-0,02<------0,02<---0,02
Fe3O4 + 4H2SO4 --> Fe2(SO4)3 + FeSO4 + 4H2O
b--->4b------------>b-------------->b
CuO + H2SO4 --> CuSO4 + H2O
c---->c------------>c
=> a = 0,02
=> 0,02 + 4b + c = 0,055 => 4b + c = 0,035
(1) => 232b + 80c = 2,36
=> b = 0,005 (mol); c = 0,015 (mol)
B chứa \(\left\{{}\begin{matrix}FeSO_4:0,025\left(mol\right)\\Fe_2\left(SO_4\right)_3:0,005\left(mol\right)\\CuSO_4:0,015\left(mol\right)\end{matrix}\right.\)
mdd sau pư = 3,48 + 100 - 0,02.2 = 103,44 (g)
=> \(\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,025.152}{103,44}.100\%=3,674\%\\C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,005.400}{103,44}.100\%=1,933\%\\C\%_{CuSO_4}=\dfrac{0,015.160}{103,44}.100\%=2,32\%\end{matrix}\right.\)
3)
Rắn khan chứa \(\left\{{}\begin{matrix}BaSO_4\\Fe\left(OH\right)_3\\Cu\left(OH\right)_2\end{matrix}\right.\)
Có: \(n_{BaSO_4}=n_{SO_4}=0,055\left(mol\right)\)
Bảo toàn Fe: \(n_{Fe\left(OH\right)_3}=n_{FeSO_4}+2.n_{Fe_2\left(SO_4\right)_3}=0,035\left(mol\right)\)
Bảo toàn Cu: \(n_{Cu\left(OH\right)_2}=0,015\left(mol\right)\)
=> b = 0,055.233 + 0,035.107 + 0,015.98 = 18,03 (g)
Đúng 5
Bình luận (0)
Hỗn hợp X gồm MgO , FeO , CuO , Fe2O3 và Fe3O4 Để hòa hoàn toàn m gam X thì cần dùng vừa đủ 100 ml dung dịch gồm HCl 2M và H2SO4 1M . Mặt khác , cho khí CO qua m gam X nung nóng , sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho toàn bộ Z vào bình đựng 60 ml dung dịch Ca(OH)2 1M. đến khi phản ứng hoàn toàn thu được kết tủa và dung dịch T. Cho tiếp dung dịch Ba(OH)2 dư vào dung dịch T thấy kết tủa lại xuất hiện . Khi phản ứng kết thúc , tổng khối lượng hai lần kết tủa thu được là 12...
Đọc tiếp
Hỗn hợp X gồm MgO , FeO , CuO , Fe2O3 và Fe3O4 Để hòa hoàn toàn m gam X thì cần dùng vừa đủ 100 ml dung dịch gồm HCl 2M và H2SO4 1M . Mặt khác , cho khí CO qua m gam X nung nóng , sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho toàn bộ Z vào bình đựng 60 ml dung dịch Ca(OH)2 1M. đến khi phản ứng hoàn toàn thu được kết tủa và dung dịch T. Cho tiếp dung dịch Ba(OH)2 dư vào dung dịch T thấy kết tủa lại xuất hiện . Khi phản ứng kết thúc , tổng khối lượng hai lần kết tủa thu được là 12,895 gam . Cho toàn bộ chất rắn Y vào dung dịch H2SO4 đặc , nóng (dư ), kết thúc phản ứng thu được 2,688 lít khi SO2 (đkc sản phẩm khử duy nhất ) và dung dịch chứa 30,4 gam muối , tính m.