Cho a gam bột sắt tác dụng hết với dung dịch H 2 SO 4 loãng dư, thu được 560 ml một chất khí (đktc). Nếu cho a gam bột sắt tác dụng hết với dung dịch CuSO 4 dư thì thu được m gam một chất rắn. Giá trị m là
A. 1,4
B. 2,8.
C. 1,6
D. 3,2
Cho một ít bột sắt nguyên chất tác dụng hết với dung dịch H2SO4 loãng thu được 560 ml một chất khí ở đktc. Nếu cho một lượng gấp đôi bột sắt nói trên tác dụng hết với dung dịch CuSO4 thì thu được một chất rắn. Tính khối lượng bột sắt đã dùng trong hai trường hợp nói trên và khối lượng chất rắn thu được.
\(TH1.Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\\ \Rightarrow m_{Fe}=0,025.56=1,4\left(g\right)\\ TH2.Fe+CuSO_4\rightarrow FeSO_4+Cu\\ Lượnggấpđôi:n_{Fe}=0,025.2=0,05\left(mol\right)\\ \Rightarrow m_{Fe}=0,05.56=2,8\left(g\right)\\ n_{Cu}=n_{Fe}=0,05\left(mol\right)\\ \Rightarrow m_{Cu}=0,05.64=3,2\left(g\right)\)
Cho một ít bột sắt nguyên chất tác dụng hết với dung dịch H2SO4 loãng thu được 560 ml một chất khí ở đktc. Nếu cho một lượng gấp đôi bột sắt nói trên tác dụng hết với dung dịch CuSO4 thì thu được một chất rắn. Tính khối lượng bột sắt đã dùng trong hai trường hợp nói trên và khối lượng chất rắn thu được.
Số mol H2 là 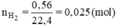
Fe + H2SO4 → FeSO4 + H2
Theo pt nFe = nH2 = 0,025(mol)
→ Khối lượng sắt dùng ở trường hợp 1 là: mFe = 0,025 x 56 = 1,4(g)
TH2: Lượng Fe gấp đôi khi đó số mol Fe là: 0,025. 2 = 0,05 (mol)
Fe + CuSO4 → FeSO4 + Cu
nFe = 0,05 mol.
Khối lượng Fe đã dùng ở trường hợp 2 là: mFe = 0,05 x 56 = 2,8 (g)
Khối lượng chất rắn m = mCu = 0,05 x 64 = 3,2(g)
Để xác định thành phần phần trăm khối lượng của hỗn hợp A gồm bột nhôm và bột magie, người ta thực hiện hai thí nghiệm sau:
– Thí nghiệm 1: cho m gam hỗn hợp A tác dụng hết với dung dịch HCl loãng dư, thu được 5,6 lít khí ở đktc.
– Thí nghiệm 2: cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư, thu được 3,36 lít khí ở đktc. Tính phần trăm khối lượng của mỗi chất trong hỗn hợp A.
Gọi số mol của Al và Fe lần lượt là a và b
Ta có 1,5a + b = 0,25
1,5a = 0,15
=> a = 0,1 và b = 0,1
=> %Al = 32,53%
%Fe= 67,47%
Nung hỗn hợp gồm a gam bột sắt và b gam bột s trong điều kiện không có không khí thu được chất rắn A. Cho A tác dụng với axit H2SO4 loãng (dư) thu được khí B có tỷ khối so với H2 bằng 10,6; dung dịch C và còn lại 1,6 gan chất rắn không tan. Sục toàn bộ khí B vào dung dịch Pb(NO3)2 dư thu được 43,02 gam kết tủa. Viết phương trình phản ứng xảy ra và tính các giá trị a, b
PT: \(Fe+S\underrightarrow{t^o}FeS\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(FeS+H_2SO_4\rightarrow FeSO_4+H_2S\)
\(H_2S+Pb\left(NO_3\right)_2\rightarrow2HNO_3+PbS\)
Ta có: mS (chưa pư) = 1,6 (g)
Theo PT: \(n_{S\left(pư\right)}=n_{FeS}=n_{H_2S}=n_{PbS}=\dfrac{43,02}{239}=0,18\left(mol\right)\)
⇒ ΣmS = 1,6 + 0,18.32 = 7,36 (g) = b
Ta có: dB/H2 = 10,6
\(\Rightarrow\dfrac{2n_{H_2}+34n_{H_2S}}{n_{H_2}+n_{H_2S}}=10,6.2\Rightarrow\dfrac{2n_{H_2}+34.0,18}{n_{H_2}+0,18}=10,6.2\)
\(\Rightarrow n_{H_2}=0,12\left(mol\right)\)
Theo PT: nFe (chưa pư) = nH2 = 0,12 (mol)
nFe (pư) = nFeS = 0,18 (mol)
⇒ mFe = (0,12 + 0,18).56 = 16,8 (g) = a
Cho 2,8 gam bột sắt và 0,81 gam bột nhôm vào 100 ml dung dịch A chứa Cu(NO3)2 và AgNO3 . Khuấy kĩ đến khi phản ứng hoàn toàn, thu được chất rắn B gồm 3 kim loại có khối lượng 8,12 gam. Cho B tác dụng với dung dịch HCl dư thu được 0,672 lít H2H2(đktc). Nồng độ mol của Cu(NO3)2 là
B gồm 3 kim loại là Fe, Cu, Ag
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,03<----------------0,03
Gọi số mol Cu, Ag là a, b (mol)
=> 64a + 108b = 8,12 - 0,03.56 = 6,44 (g) (1)
\(\left\{{}\begin{matrix}n_{Al^{3+}}=\dfrac{0,81}{27}=0,03\left(mol\right)\\n_{Fe^{2+}}=\dfrac{2,8}{56}-0,03=0,02\left(mol\right)\end{matrix}\right.\)
=> \(n_{NO_3^-}=0,03.3+0,02.2=0,13\left(mol\right)\)
\(\left\{{}\begin{matrix}n_{Cu\left(NO_3\right)_2}=a\left(mol\right)\\n_{AgNO_3}=b\left(mol\right)\end{matrix}\right.\)
=> 2a + b = 0,13 (2)
(1)(2) => a = 0,05 (mol); b = 0,03 (mol)
=> \(C_{M\left(Cu\left(NO_3\right)_2\right)}=\dfrac{0,05}{0,1}=0,5M\)
Lắc 0,81 gam bột nhôm trong 200 ml dung dịch X chứa AgNO3 và Cu(NO3)2 một thời gian, thu được chất rắn A và dung dịch B. Cho A tác dụng với dung dịch NaOH dư thu được 100,8 ml khí H2 (đktc) và cịn lại 6,012 gam hỗn hợp hai kim loại. Cho B tác dụng với dung dịch NaOH dư được kết tủa, đem nung kết tủa đến khối lượng khơng đổi thu được 1,6 gam oxit.
1. Viết các phương trình hóa học xảy ra.
2. Tính nồng độ mol/lít của AgNO3 và Cu(NO3)2 trong dung dịch X.
1)
- Trong A chứa Al, Cu, Ag
- Do trong A chứa Cu => Ag bị đẩy ra hết khỏi dd
- Do cho B tác dụng với NaOH dư thu được kết tủa
=> Trong B chứa Al(NO3)3, Cu(NO3)2
Al + 3AgNO3 --> Al(NO3)3 + 3Ag
2Al + 3Cu(NO3)2 --> 2Al(NO3)3 + 3Cu
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
Al(NO3)3 + 3NaOH --> Al(OH)3 + 3NaNO3
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
Cu(NO3)2 + 2NaOH --> Cu(OH)2 + 2NaNO3
Cu(OH)2 --to--> CuO + H2O
2)
Rắn sau khi nung là CuO
\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
=> \(n_{Cu\left(NO_3\right)_2\left(B\right)}=0,02\left(mol\right)\)
\(n_{H_2}=\dfrac{0,1008}{22,4}=0,0045\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,003<---------------------------------0,0045
Bảo toàn Al: \(n_{Al\left(NO_3\right)_3\left(B\right)}=\dfrac{0,81}{27}-0,003=0,027\left(mol\right)\)
Gọi số mol Cu, Ag trong hỗn hợp kim loại là a, b (mol)
=> 64a + 108b = 6,012 (1)
Bảo toàn Ag: \(n_{AgNO_3\left(X\right)}=b\left(mol\right)\)
Bảo toàn Cu: \(n_{Cu\left(NO_3\right)_2\left(X\right)}=a+0,02\left(mol\right)\)
Bảo toàn \(NO_3^-\): \(n_{AgNO_3\left(X\right)}+2.n_{Cu\left(NO_3\right)_2\left(X\right)}=3.n_{Al\left(NO_3\right)_3\left(B\right)}+2.n_{Cu\left(NO_3\right)_2\left(B\right)}\)
=> \(b+2a+0,04=3.0,027+2.0,02\)
=> 2a + b = 0,081 (2)
(1)(2) => a = 0,018 (mol); b = 0,045 (mol)
=> \(\left\{{}\begin{matrix}n_{AgNO_3\left(X\right)}=0,045\left(mol\right)\\n_{Cu\left(NO_3\right)_2\left(X\right)}=0,038\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(AgNO_3\right)}=\dfrac{0,045}{0,2}=0,225M\\C_{M\left(Cu\left(NO_3\right)_2\right)}=\dfrac{0,038}{0,2}=0,19M\end{matrix}\right.\)
Cho m gam bột sắt vào 200 ml dung dịch CuSO4 1M, sau phản ứng hoàn toàn thu được chất rắn X. Chia X thành 2 phần không bằng nhau:
Phần 1: cho tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí H2 (đktc).
Phần 2: cho tác dụng với dung dịch HNO3 loãng dư, thu được 6,72 lít khí NO (đktc). NO là sản phẩm khử duy nhất của HNO3.
Giá trị của m gần nhất với giá trị nào sau đây?
A. 28,2
B. 30,8
C. 26,4
D. 24,0
Đáp án A
- P1: hỗn hợp rắn X + HCl → H2 => chứng tỏ Fe dư, Cu2+ phản ứng hết.
Fe + 2HCl → FeCl2 + H2
=> nFe(1) = nH2 = 2,24: 22,4 = 0,1 mol
- P2: X + HNO3 → NO => Cả Fe và Cu đều phản ứng
Giả sử số mol ở phần 2 gấp k lần phần 1. Gọi số mol Cu phần 1 là a
Bảo toàn electron: 3nFe(2) + 2nCu(2) = 3nNO = 3.6,72: 22,4 = 0,9 mol
=> 3.0,1k + 2.ak = 0,9 (*)
Bảo toàn nguyên tố Cu: nCuSO4 = nCu(1) + nCu(2) => 0,2 = a + ak => a = 0 , 2 k + 1
Thay vào (*) =>0,3k + 2k. 0 , 2 k + 1 = 0,9
=> k = 2,097
- Vì Fe dư sau phản ứng nên: nFe pứ = nCuSO4 = 0,2 mol
=> nFe = nFe pứ + nFe(1) + nFe(2) = 0,3 + 0,1k = 0,5097 mol
=> mFe = 28,5432g (Gần nhất với giá trị 28,2g)
Cho 2,8 gam bột sắt và 0,81 gam bột nhôm vào 100 ml dung dịch A chứa Cu NO 3 2 và AgNO 3 . Khuấy kĩ đến khi phản ứng hoàn toàn, thu được chất rắn B gồm 3 kim loại có khối lượng 8,12 gam. Cho B tác dụng với dung dịch HCl dư thu được 0,672 lít H 2 (đktc). Nồng độ mol của Cu NO 3 2 là
A. 0.3M
B. 0,5M
C. 0,6M
D. 1M
Dung dịch Y có chứa các ion: N H + 4 , N O - 3 , S O 2 - 4 . Cho dung dịch Y tác dụng với lượng dư dung dịch Ba(OH)2, đun nóng thu được 11,65 gam kết tủa và 4,48 lít khí (đktc). Nếu cho m gam dung dịch Y cho tác dụng với một lượng bột Cu dư và H2SO4 loãng dư sinh ra V lít NO (sản phẩm khử duy nhất, đo ở đktc). Giá trị của V là
A. 1,87.
B. 2,24.
C. 1,49.
D. 3,36.