Khác với nguyên tử O, ion oxit O 2 - có
A. bán kính ion nhỏ hơn và ít electron hơn.
B. bán kính ion nhỏ hơn và nhiều electron hơn.
C. bán kính ion lớn hơn và ít electron hơn.
D. bán kính ion lớn hơn và nhiéu electron hơn.
Trong các nguyên tử và ion : Ne, Na, Mg, Al, Al3+, Mg2+, Na+ , O2–, F–, hạt có bán kính lớn nhất và hạt có bán kính nhỏ nhất là
A. Al3+, O2–
B. Na, Al3+
C. Na, Ne
D. O2–, Na+
Đáp án : B
Các nguyên tử ion có số lớp e nhiều hơn thì bán kính lớn hơn
Các nguyên tử ion có cùng số lớp e
cùng số e thì nguyên tử ion nào có điện tích âm sẽ có bán kính lớn hơn và ngược lại
Ion nào có bán kính nhỏ nhất trong các ion sau
A. Li+ B. K+ C. Be2+ D. Mg2+
A, Li+
vì Be2+ và Li+ là 2 ion có bán kính nhỏ hơn Mg2+ và K+. Xét 2 ion Li+ và Be2+ có số lớp e như nhau nhưng Be2+ mất đi 2e nên lực hút của p trong hạt nhân mạnh hơn lực hút p trong hạt nhân Li+ chỉ mất 1 e, do lực hút lớn hơn nên bán kính ion này bị thu nhỏ hơn.
C, Be2+
vì Be2+ và Li+ là 2 ion có bán kính nhỏ hơn Mg2+ và K+. Xét 2 ion Li+ và Be2+ có số lớp e như nhau nhưng Be2+ mất đi 2e nên lực hút của p trong hạt nhân mạnh hơn lực hút p trong hạt nhân Li+ chỉ mất 1 e, do lực hút lớn hơn nên bán kính ion này bị thu nhỏ hơn.
Cầu 11: Hai ion X+ và Y2- đều có câu hình electron của khí hiểm Ne (Z=10). Cho các nhận xét sau
(1) Số hạt mang điện của X nhiều hơn số hạt mang điên của Y là 6.
(2) Bán kính ion Y2- lớn hơn bản kính ion X+.
(3) X ở chu kỳ 2, còn Y ở chu kỷ 3 trong bảng hệ thống tuần hoàn.
(4) Độ âm điện của X nhỏ hơn độ âm điện của Y.
(5) X thuộc loại nguyên tố p.
(6) Cho 2,3 gam X phản ứng với nước dư thu được 0,224 lit khi ở điều kiện tiêu chuẩn
Số nhận xét đúng là:
А. 4.
В. 3.
С. 1.
D. 2.
------------
giúp tui câu hóa này với các bạn ơi
Cho các nguyên tử: N (Z=7), Cl (Z=17), O (Z=8) và F (Z=9). Bán kính ion được sắp xếp tăng dần theo thứ tự
A.N3-, O2-, F-, Cl-
B. Cl- N3-, O2-, F-
C. F-, O2-, N3-,Cl-
D. Cl-; F-, O2-, N3-
Đáp án C
+ Khi sắp xếp bán kính nguyên tử hay ion thì ưu tiên số lớp e (chu kì) trước
+ Sau đó cùng chu kì thì chất nào có Z nhỏ thì bán kính sẽ lớn
Trong nguyên tử Hidro, electron chuyển động quanh hạt nhân theo quỹ đạo tròn bán kính R = 5 . 10 - 9 cm. Năng lượng cần thiết để ion hóa nguyên tử Hidro (đưa electron ra xa vô cực) là:
A. 14,4 eV
B. 15,4 eV
C. 20 eV
D. 13,9 eV
a) Giải thích vì sao bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b) Vì sao cả Na2O và MgO đều là chất rắn ở nhiệt độ thường?
c) Vì sao nhiệt độ nóng chảy của MgO (2 852oC) cao hơn rất nhiều so với Na2O (1 132oC)?
a)
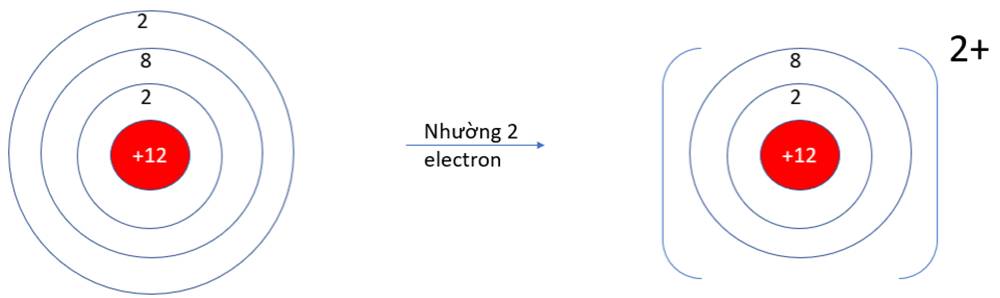
- Ở dạng nguyên tử, Na và Mg đều có 3 lớp electron. Ở dạng ion Na+, Mg2+ chỉ có 2 lớp electron
=> Bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b, Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion nên ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion nên ở điều kiện thường MgO tồn tại ở thể rắn.
c, Tá có:
+ Bán kính ion Na+ < bán kính ion Mg2+.
+ Điện tích ion Mg2+ < điện tích ion Na+.
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.
Các ion N a + , M g 2 + , O 2 - , F ¯ đều có cùng cấu hình electron. Thứ tự giảm dần bán kính của các ion trên là
A. N a + > M g 2 + > F ¯ > O 2 -
B. M g 2 + > N a + > F ¯ > O 2
C. F ¯ > N a + > M g 2 + > O 2 -
D. O 2 - > F ¯ > N a + > M g 2 +
D
Ta thấy các ion N a + , M g 2 + , O 2 - , F ¯ đều có cùng cấu hình electron 1 s 2 2 s 2 2 p 6 .
Các ion cùng electron so sánh điện tích trong nhân, điện tích hạt nhân càng lớn, lực hút electron càng mạnh, bán kính ion càng nhỏ.
Vậy thứ tự giảm dần bán kính là: O 2 - > F ¯ > N a + > M g 2 +
Phát biểu nào sau đây là đúng? Giải thích? A, Đồng vị là hiện tượng các hạt có cùng số khối. B, So với các nguyên tử thì các ion âm tạo thành từ nguyên tử đó luôn có bán kính lớn. C, Điện tích hạt nhân nguyên tử bằng số proton và bằng số electron trong nguyên tử. D, Các tiểu phân Ar, K+, Cl- đều có cùng số điện tích hạt nhân.
A. Sai vì đồng vì có cùng số hạt proton
B. Sai
C. Đúng
D. Sai vì có cùng số electron
Cho các nguyên tố M (Z= 11), X (Z = 8), Y (Z =9) , R (Z = 12). a. So sánh tính kim loại – tính phi kim của các nguyên tử của các nguyên tố trên. b. Dự đoán ion tạo thành của các nguyên tử các nguyên tố trên và so sánh bán kính của các ion tạo thành đó. Giải thích.