Số oxi hoá của nitơ trong NH 3 , HNO 2 và NO 3 lần lượt là
A.+5,-3,+3. B.-3,+3,+5. C.+3,-3,+5. D.+3,+5,-3.
Nguyên tố nitơ trong các hợp chất có số oxi hoá thấp nhất là -3 và cao nhất là +5. Xác định số oxi hoá của nitơ trong các hợp chất sau và xét xem trong hợp chất nào nitơ chỉ có tính oxi hoá, trong hợp chất nào nitơ chỉ có tính khử ?
NH 4 Cl , NO , HNO 2 , N 2 O 5
Nguyên tố nitơ trong các hợp chất có số oxi hoá thấp nhất là -3 và cao nhất là +5. Xác định số oxi hoá của nitơ trong các hợp chất sau và xét xem trong hợp chất nào nitơ chỉ có tính oxi hoá, trong hợp chất nào nitơ chỉ có tính khử ?
NH 3 , N 2 O , HNO 3 , NO 2
Số oxi hoá của nguyên tố nitơ trong các hợp chất : NH4Cl, HNO3, NO, NO2, N2,N2O lần lượt là :
A. - 4, +6, +2, +4, 0, +1
B. 0, +1,–4, +5, –2, 0
C. -3, +5, +2,+4, 0,+1
D. 0, +1.+3, –5, +2, –4
Đáp án C.
Gọi số oxi hóa của N là x, số oxi hóa trong hợp chất của H =+1, O = -2.

Số oxi hoá của nguyên tố nitơ trong các hợp chất: N H 4 C l , H N O 3 , N O , N O 2 , N 2 , N 2 O lần lượt là
A. - 4, +6, +2, +4, 0, +1.
B. 0, +1,–4, +5, –2, 0.
C. -3, +5, +2,+4, 0,+1.
D. 0, +1.+3, –5, +2, –4.
Chọn C
Gọi số oxi hóa của N là x, trong hợp chất số oxi hóa của H = +1, O = -2.

Trong phản ứng nhiệt phân các muối NH4NO2 và NH4NO3 số oxi hoá của nitơ biến đổi như thế nào? Nguyên tử nitơ trong ion nào của muối đóng vai trò chất khử và nguyên tử nitơ trong ion nào của muối đóng vai trò chất oxi hoá?
Phản ứng nhiệt phân:
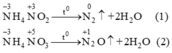
Trong hai phản ứng trên số oxi hoá của nitơ trong mỗi phản ứng đều thay đổi. Trong mỗi phân tử muối một nguyên tử nitơ có số oxi hoá tăng, một nguyên tử có số oxi hoá giảm, đây là phản ứng oxi hoá khử nội phân tử.Ở cả hai phản ứng nitơ nguyên tử trong ion NH+4 đều là chất khử (chất cho e) nitơ từ số oxi hoá -3 tăng lên 0 ở phản ứng (1) và lên +1 ở phản ứng (2).Nguyên tử nitơ trong ion NO2- và NO3- là chất oxi hoá (chất nhận e). Ở phản ứng (1) số oxi hoá của N từ +3 (trong NO2- ) xuống 0 và ở phản ứng (2) số oxi hoá của nitơ từ +5 (trong NO3-) xuống +1.
Cho biết số oxi hoá của nitrogen trong mỗi phân tử và ion sau: NH3, N2, N2O, NO, NO2, HNO2, HNO3.
Cho các phát biểu sau :
(1) Khoáng vật chính của photpho trong tự nhiên là pirit, apatit và photphoric.
(2) Các số oxi hoá có thể có của photpho là –3; +3; +5; 0.
(3) Tính chất hoá học điển hình của photpho là tính oxi hoá.
(4) Trong phòng thí nghiệm, axit photphoric được điều chế bằng phản ứng giữa P2O5 và H2O.
(5) Trong điều kiện thường, photpho hoạt động hoá học mạnh hơn nitơ là do độ âm điện của photpho (2,1) nhỏ hơn của nitơ (3,0).
Số phát biểu không đúng là:
A. 2.
B. 3.
C. 4.
D. 1.
(1) sai, khoáng vật chính của photpho trong tự nhiên là apatit và photphorit
(2) đúng
(3) đúng
(4) sai, trong phòng thí nghiệm, axit photphoric được điều chế bằng phản ứng giữa P và
H
N
O
3
đặc
(5)sai, P hoạt động hơn N do N tồn tại ở
N
2
có liên kết ba bền
Đáp án B
Từ ammonia có thể điều chế phân đạm ammonium nitrate theo sơ đồ chuyển hoá sau:
o
O , t , xt O O H O 2 2 2 2
NH NO NO HNO 3 2 3 ⎯⎯⎯⎯→ ⎯⎯⎯→ ⎯⎯⎯⎯→ + + + + → NH4NO3
a) Viết các phương trình hoá học xảy ra.
b) Xác định chất khử, chất oxi hóa trong 3 giai đoạn đầu của quá trình Ostwald
c) Tại sao giai đoạn đầu cần trộn ammonia với không khí theo tỉ lệ thể tích 1:9 ? (Biết không khí chứa
21% thể tích oxygen.)
b) Để điều chế 200 000 tấn phân đạm ammonium nitrate theo sơ đồ trên cần dùng bao nhiêu tấn
ammonia? Biết rằng hiệu suất của cả quá trình theo sơ đồ trên là 95%.
Trong các phân tử nào sau đây, nitơ có hoá trị và trị tuyệt đối của số oxi hoá bằng nhau ?
A.N2
B.NH3
C.NH4Cl
D.HNO3
Xét đáp án HNO3: N có hóa trị và trị tuyệt đối của số oxi hóa đều là 5.
Trong phản ứng nhiệt phân các muối NH4NO2 và NH4NO3, số oxi hóa của nitơ biến đổi như thế nào ? Nguyên tử nitơ trong ion nào của muối đóng vai trò chất khử và nguyên tử nitơ trong ion nào của muối đóng vai trò chất oxi hóa ?
NH4NO2 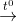 N2 + 2H2O; NH4NO3
N2 + 2H2O; NH4NO3 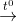 N2O + 2H2O
N2O + 2H2O
N có số oxi hóa +3 và +5 trong NO2- và NO3- : đóng vai trò chất oxi hóa.
N có số oxi hóa -3 trong NH4+: đóng vai trò chất khử.