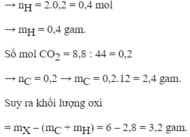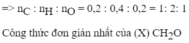Khi đốt 6g một chất có công thức C n H 2 n + 1 C O O H người ta thu được 4,48 lít khí C O 2 (đktc). Xác định trị của n trong chất hữu cơ trên (cho H=1, C=12, O=16).

Những câu hỏi liên quan
GIÚP EM VỚI ẠAA!
Câu 1: Đốt cháy hoàn toàn 6g hợp chất hữu cơ A thu được 8,8g khí CO2 và 3,6g H2O.
a, Hợp chất hữu cơ A gồm những nguyên tố nào?
b, Hãy xác định công thức phân tử của A. Biết khối lượng mol của A là 60g.
Câu 2: Một hợp chất hữu cơ A chứa 3 nguyên tố C,H và O. Đốt cháy hoàn toàn 3,75g chất A thì thu được 8,25g CO2 và 4,5g H2O.
a, Tìm công thức phân tử của A. Biết dA/H2 30.
b, Viết các công thức cấu tạo của chất A. Biết A có thể tác dụng với Na.
Câu 3: Đốt cháy hoàn toàn 4,...
Đọc tiếp
GIÚP EM VỚI ẠAA!
Câu 1: Đốt cháy hoàn toàn 6g hợp chất hữu cơ A thu được 8,8g khí CO2 và 3,6g H2O.
a, Hợp chất hữu cơ A gồm những nguyên tố nào?
b, Hãy xác định công thức phân tử của A. Biết khối lượng mol của A là 60g.
Câu 2: Một hợp chất hữu cơ A chứa 3 nguyên tố C,H và O. Đốt cháy hoàn toàn 3,75g chất A thì thu được 8,25g CO2 và 4,5g H2O.
a, Tìm công thức phân tử của A. Biết dA/H2 = 30.
b, Viết các công thức cấu tạo của chất A. Biết A có thể tác dụng với Na.
Câu 3: Đốt cháy hoàn toàn 4,5g một hợp chất hữu cơ A thấy sinh ra 6,6g khí CO2 và 2,7g H2O. Biết khối lượng mol của A bằng 60. Xác định công thức phân tử và viết công thức cấu tạo của A, biết A vừa tác dụng với Na, vừa tác dụng với NaOH.
EM CẢM ƠN NHIỀU Ạ ~
Câu 1:
Ta có :
nC=nCO2=8,8/44=0,2 mol
nH=2nH2O=3,6/18=0,4 mol
=> mC+ mH=(0,2.12) + (0,4.1)=2,8g
=> Hợp chất hữu cơ A có 3 nguyên tố : C,H,O
CxHyOz + (x+y/2-z/2)O2--------->xCO2 + y/2H2O
Ta có :
n O2=(6-2,8)/32=0,1 mol
=> n CO2=0,1x=0,2=>x=2
y=2x=>y=4
12x+y+16z=60=>z=2
Vậy A có CT: C2H4O2
Đúng 0
Bình luận (2)
Câu 2:Làm theo các bước như câu 1
Bổ sung thêm như này:
Ta có:
dA/H2=MA/MH2=30
=>MA=30.MH2=30.2=60g
b.CTCT:như SGK.
2CH3COOH + 2Na-------->2CH3COONa + H2
Đúng 0
Bình luận (0)
Đốt 6g một chất hữu cơ X sản phẩm khí C O 2 và hơi H 2 O cho qua bình 1 đựng H 2 S O 4 đặc, sau đó cho qua bình 2 đựng dung dịch NaOH dư, khối lượng 2 bình tăng lần lượt là 3,6g và 8,8g. Tìm công thức đơn giản nhất của X (cho H=1, C=12, O=16).
Câu 1: Đốt cháy hoàn toàn 3 gam hợp chất hữu cơ X (chứa C, H, O) thu đc 4,4 gam CO2 và 1,8 gam H2O.1. Lập công thức đơn giản nhất của X.2. Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với không khí xấp xỉ 2,069.(Biết: H1, O16, C12, N14, Ca40)Câu 2: Một hợp chất hữu cơ X có phần trăm khối lượng %C 54,54%, %H 9,1%, còn lại là oxi.1. Lập công thức đơn giản nhất của X2. Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với nitơ xấp xỉ bằng 3,143.(Biết: H1, O16, C12, N14, Ca40)
Đọc tiếp
Câu 1: Đốt cháy hoàn toàn 3 gam hợp chất hữu cơ X (chứa C, H, O) thu đc 4,4 gam CO2 và 1,8 gam H2O.
1. Lập công thức đơn giản nhất của X.
2. Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với không khí xấp xỉ 2,069.
(Biết: H=1, O=16, C=12, N=14, Ca=40)
Câu 2: Một hợp chất hữu cơ X có phần trăm khối lượng %C = 54,54%, %H = 9,1%, còn lại là oxi.
1. Lập công thức đơn giản nhất của X
2. Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với nitơ xấp xỉ bằng 3,143.
(Biết: H=1, O=16, C=12, N=14, Ca=40)
1)
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
Bảo toàn C: nC(X) = 0,1 (mol)
Bảo toàn H: nH(X) = 0,2 (mol)
=> \(n_O=\dfrac{3-0,1.12-0,2.1}{16}=0,1\left(mol\right)\)
Xét nC : nH : nO = 0,1 : 0,2 : 0,1 = 1:2:1
=> CTDGN: CH2O
2) MX = 2,069.29 = 60(g/mol)
CTPT: (CH2O)n
=> n = 2
=> CTPT: C2H4O2
Câu 2
1) Có: %mC : %mH : %mO = 54,54% : 9,1% : 36,36%
=> %nC : %nH : %nO = 4,545 : 9,1 : 2,2725 = 2:4:1
=> CTDGN: C2H4O
2) MX = 3,143.28 = 88(g/mol)
CTPT: (C2H4O)n
=> n = 2
=> CTPT: C4H8O2
Đúng 2
Bình luận (0)
Chất X chứa các nguyên tố C,H,O,N có khối lượng phân tử bằng 89. Biết rằng khi đốt cháy hoàn toàn 0,1mol X thu được C02, H2O và 1,12 lít N2. Công thức phân tử X là ?
Đốt cháy 6g 1 chất X thu được 4,48 l khí Co2 và 3,6g nước.
a) X chứa nguyên tố hóa học nào?
b) Tìm công thức hóa học của X biết rằng dX/H = 30.
\(n_{CO_2}=0,2\left(mol\right)=>n_C=0,2\left(mol\right)\)
\(n_{H_2O}=0,2\left(mol\right)=>n_H=0,4\left(mol\right)\)
=> \(\Sigma m_C+m_H=0,2.12+0,4.1=2,8< 6\left(g\right)\)
a) => X chứa C , H , O
b) \(m_O=6-2,8=3,2\left(g\right)=>n_O=0,2\left(mol\right)\)
Đặt CTPT : \(C_xH_yO_z\)
=> \(x:y:z=0,2:0,4:0,2=1:2:1\)
=> CTĐG : \(\left(CH_2O\right)_n\)
\(M_X=30.1=30\left(\frac{gam}{mol}\right)\)
=> 15n=30=> n=2
=> CTPT : \(C_2H_4O_2\)
nC=nCO2=4,48/22,4=0,2 (mol) ==> mC=0,2.12=2,4 (g)
nH=2nH2O=(3,36/22,4).2= 0,3 (mol) ==> mH=0,3.1=0,3 (mol)
==> Tổng khối lượng của mH và mC= 2,4 + 0,3=2,7 < mX=6 (g)
Vậy trong X có chứa C, H và O
=> mO= 6-2,7=3,3 (g) ==> nO=3,3/16=0,20625 (mol)
MX= 30.2=60 (g)
Gọi CTTQ của X là CxHyOz, ta có:
x:y:z= nC:nH:nO= 0,2:0,3:0,20625= 1:2:1
Vậy công thức đơn giản của X là (CH2O)n
⇔ M(CH2O)n = 12n + 2n + 16n=60
==> n=2
Vậy công thức hóa học của X là C2H4O2
Hợp chất X (C, H, O) chứa một nhóm chức trong phân tử, không tác dụng với Na, tác dụng với NaOH có thể theo tỉ lệ 1 :1 hay 1:2. Khi đốt cháy 1 mol X cho 7 mol CO2. Tìm công thức cấu tạo của X A. C2H5COOC4H9 B. C3H7COOC3H7 C. HCOOC6H5 D. Kết quả khác
Đọc tiếp
Hợp chất X (C, H, O) chứa một nhóm chức trong phân tử, không tác dụng với Na, tác dụng với NaOH có thể theo tỉ lệ 1 :1 hay 1:2. Khi đốt cháy 1 mol X cho 7 mol CO2. Tìm công thức cấu tạo của X
A. C2H5COOC4H9
B. C3H7COOC3H7
C. HCOOC6H5
D. Kết quả khác
Đáp án: C
Ta thấy:
HCOOC6H5 + NaOH → HCOONa + C6H5OH
và HCOOC6H5 + NaOH → HCOONa + C6H5ONa
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1 hợp chất hữu cơ A cần dùng 0,8g oxi, người ts thu đc 1,1g cacbonic và 0,45g nước và ko có sản phẩm nào khác. Xác định công thức phân tử của A biết thể tích khi hóa hơi 6g A bằng thể tích 3,2g oxi ở cùng điều kiện
mC = 1.1 x 12/44 = 0.3 (g)
mH = 0.45 x 2/18 = 0.05 (g)
Theo ĐLBTKL: ==> mA = 1.1 + 0.45 - 0.8 = 0.75 (g)
mO = 0.75 -(0.3 +0.05) = 0.4 (g)
Với 3.2 g oxi => nO2 = 0.1 (mol) => VO2 = 2.24 (l)
6g A ----> 2.24 (l); 0.75gA ----> 0.28 (l)
nA = 0.0125 (mol) ==> A = 0.75/0.0125 = 60
CxHyOz
12x/0.3 = y/0.05 = 16z/0.4 = 60/0.75
Suy ra: x = 2, y = 4; z = 2
CT: C2H4O2
Đúng 0
Bình luận (0)
Từ công thức hoá học của phân đạm ure CO(NH2)2. Cho biết ý nào sau đây không đúng ? ( Cho biết O16; H 1; N 14; C 12)A Phân tử khối của hợp chất là 60 đvCB Hợp chất trên do 4 nguyên tố là: N, H, O, C tạo nênC Có 4 nguyên tử H, 2 nguyên tử N, 1 nguyên tử C và 1 nguyên tử O trong 1 phân tửD Hợp chất trên có 7 nguyên tử
Đọc tiếp
Từ công thức hoá học của phân đạm ure CO(NH2)2. Cho biết ý nào sau đây không đúng ?
( Cho biết O=16; H = 1; N= 14; C = 12)
A Phân tử khối của hợp chất là 60 đvC
B Hợp chất trên do 4 nguyên tố là: N, H, O, C tạo nên
C Có 4 nguyên tử H, 2 nguyên tử N, 1 nguyên tử C và 1 nguyên tử O trong 1 phân tử
D Hợp chất trên có 7 nguyên tử
Đốt cháy hoàn toàn 6g hợp chất A thu được ( 4,48 l CO2 ) và 3,6 g H2O. Biết 1L hơi A nặng 2,67 g.
Tìm công thức phân tử A ? ( Khí đo ở đktc )
Vì sp cháy là CO2 và H2O => A có thể chứa các nguyên tố C, H, O
CTDC: CxHyOz
Theo đề, 1 lít hơi A nặng 2,67 gam \(\Rightarrow M_A=\dfrac{2,67}{1\div22,4}=60\left(\dfrac{g}{mol}\right)\)
nCO2 = 0,2 mol => nC = 0,2 mol
nH2O = 0,2 mol => nH = 0,4 mol
=> nO (sau pứ) = 0,6 (mol)
Bảo toàn khối lượng \(\Rightarrow m_{O_2}=6,4\left(gam\right)\Rightarrow n_{O_2}=0,2\left(mol\right)\) => nO (trong Oxi ) = 0,4 (mol)
=> nO (trong A) = 0,2 (mol)
\(x:y:z=0,2:0,4:0,2=1:2:1\)
\(\Rightarrow CTTN:\left[CH_2O\right]_n\)mà \(M_A=60\left(\dfrac{g}{mol}\right)\)
=> n = 2
=> \(C_2H_4O_2\)
Đúng 1
Bình luận (1)