Tìm phát biểu sai. Hạt nhân nguyên tử chì 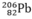 có:
có:
A. 206 n u c l ô n
B. đ i ệ n t í c h l à 1 , 312 . 10 - 18 C
C. 124 n ơ t r o n
D. 82 p r o t o n
Tìm phát biểu sai. Hạt nhân nguyên tử chì 20682Pb có
A. 206 nuclôn
B. điện tích là1,312.10-18C
C. 124 nơtron
D. 82 proton
82 là số proton của hạt nhân
Chọn đáp án D
Câu 9: Phát biểu nào sau đây là sai?
A. Nguyên tử gồm 2 phần là hạt nhân và lớp vỏ electron
B. Khối lượng nguyên tử tập trung hầu hết ở hạt nhân.
C. Kích thước của hạt nhân rất nhỏ bé so với kích thước của nguyên tử.
D. Khối lượng của electron, proton và nơtron đều xấp xỉ bằng nhau.
Câu 10 : Nguyên tử của nguyên tố X có tổng số hạt là 54. Trong đó số hạt không mang điện nhiều hơn số hạt mang điện âm là 3 hạt. Số nơtron trong nguyên tử X là
A. 17. B. 16. C. 20. D. 18.
Câu 11: Nguyên tử M có tổng số các loại hạt cơ bản là 60. Trong đó tổng số hạt ở nhân gấp đôi số hạt ở vỏ. Số hạt ở vỏ nguyên tử là
A. 20. B. 40. C. 15. D. 30.
Bài 12: Tìm số p,e,n của nguyên tố X trong các trường hợp sau :
⦁ Số hạt mang điện bằng 11 phần 6 số hạt không mang điện . Số hạt ở nhân nhiều hơn số hạt ở vỏ là 12 hạt.
⦁ Số hạt mang điện nhiều hơn số hạt không mang điện 7 hạt . Tỉ lệ hai loại hạt ở nhân là 9 phần 8
9.D
10.
Ta có: \(\left\{{}\begin{matrix}p+e+n=54\\p=e\\n-e=3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=17\\n=20\end{matrix}\right.\)
⇒ Chọn C
11.
Ta có: \(\left\{{}\begin{matrix}p+e+n=60\\p=e\\p+n=2e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=20\\n=20\end{matrix}\right.\)
⇒ Chọn A
Hạt nhân urani \(_{92}^{238}U\) sau một chuỗi phân rã, biến đổi thành hạt nhân chì \(_{82}^{206}Pb\) . Trong quá trình đó, chu kì bán rã của \(_{92}^{238}U\) biến đổi thành hạt nhân chì \(_{82}^{206}Pb\) là 4,47.109 năm. Một khối đá được phát hiện có chứa 1,188.1020 hạt nhân \(_{92}^{238}U\) và 6,239.1018 \(_{82}^{206}Pb\) hạt nhân . Giả sử khối đá lúc mới hình thành không chứa chì và tất cả lượng chì \(_{82}^{206}Pb\) có mặt trong đó đều là sản phẩm phân rã của \(_{92}^{238}U\). Tuổi của khối đá khi được phát hiện là
A.3,3.108 năm.
B.6,3.109 năm.
C.3,5.107 năm.
D.2,5.106 năm.
Cứ 1 hạt nhân \(_{92}^{238}U\) bị phân rã tạo ra 1 hạt nhân \(_{82}^{206}Pb\). Từ đó ta có nhận xét là số hạt nhân \(_{92}^{238}U\) bị phân rã chính bằng số hạt nhân \(_{82}^{206}Pb\) tạo thành.
Tỉ số giữa số hạt nhân \(_{92}^{238}U\) bị phân rã và số hạt nhân \(_{92}^{238}U\) còn lại là
\(\frac{\Delta N}{N}= \frac{6,239.10^{18}}{1,188.10^{20}}= 0,0525 = \frac{1-2^{-\frac{t}{T}}}{2^{-\frac{t}{T}}}\)
Nhân chéo => \(2^{-\frac{t}{T}}= 0,95.\)
=> \(t = -T\ln_2 0,95 = 3,3.10^8\)(năm)
=> Tuổi của khối đã là 3,3.108 năm.
Phát biểu nào sau đây đúng
A. Hạt nhân nguyên tử hiđro có 1 proton
B. Hạt nhân nguyên tử hiđro chỉ có 1 proton, không có nơtron
C. Hạt nhân nguyên tử của các đồng vị của hiđro đều có proton và nơtron
D. Hạt nhân nguyên tử của các đồng vị của hiđro đều có nơtron
Câu 1. Các phát biểu sau đúng hay sai? Vì sao?
(a) Bảng tuần hoàn hiện đại ngày nay, các nguyên tố được sắp xếp theo chiều tăng dần khối lượng nguyên tử.
(b) Số thứ tự của ô nguyên tố trong bảng tuần hoàn bằng số hạt proton trong nguyên tử.
(c) Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp thành một hàng theo chiều tăng dần của điện tích hạt nhân.
(d) Nhóm là tập hợp các nguyên tử có số electron lớp ngoài cùng giống nhau.
(e) Electron hóa trị là các electron có khả năng tham gia tạo thành liên kết hóa học.
(g) Nhóm A gồm các nguyên tố s, d; nhóm B gồm các nguyên tố p, f.
(a) Sai. Bảng tuần hoàn hiện đại sắp xếp các nguyên tố theo chiều tăng dần số nguyên tử , không phải theo chiều tăng dần khối lượng nguyên tử.
(b) Đúng. Số thứ tự của một nguyên tố trong bảng tuần hoàn bằng số proton trong hạt nhân của nó, không phải là số hạt proton trong nguyên tử.
(c) Sai. Chu kỳ là dãy các nguyên tố có cùng số lượng lớp electron và chúng được xếp thành một hàng ngang (không phải hàng dọc) trong bảng tuần hoàn.
(d) Đúng. Nhóm (còn gọi là cột) là tập hợp các nguyên tố có cùng số electron lớp ngoài cùng, và chúng thường có tính chất hóa học tương tự.
(e) Đúng. Electron hóa trị là các electron ở lớp ngoài cùng của một nguyên tử và có khả năng tham gia vào quá trình tạo liên kết hóa học.
(g) Sai. Nhóm A gồm các nguyên tố s và p, trong khi nhóm B gồm các nguyên tố d và f.
Phát biểu nào sau đây sai? A.Nguyên tử trung hoà về điện B.Hạt nhân nguyên tử có kích thước rất bé nhưng lại có khối lượng rất lớn C..Nguyên tử cí cấu tạo rỗng D.Khối lượng của nguyên tử gần bằng khối lượng của hạt nhân nguyên tử
Phát biểu nào sau đây sai?
A.Nguyên tử trung hoà về điện
B.Hạt nhân nguyên tử có kích thước rất bé nhưng lại có khối lượng rất lớn
C..Nguyên tử có cấu tạo rỗng
D.Khối lượng của nguyên tử gần bằng khối lượng của hạt nhân nguyên tử
Mình thấy B,C sai
Vì câu B nó không có kích thước lớn, câu C cấu tạo nguyên tử đặc khít mới đúng
Hoặc có thể C sai rõ ràng
Nhưng câu B thì khối lượng rất lớn (và rất lớn đó là so với tổng KL nguyên tử)
Nên chọn C là hợp lí nhất
Phát biểu nào sau đây đúng
A. Chỉ có hạt nhân nguyên tử oxi mới có 8 nơtron
B. Chỉ có hạt nhân nguyên tử oxi mới có 8 electron
C. Chỉ có hạt nhan nguyên tử oxi mới có 8 proton
D. Chỉ có ion O 2 - mới có 10 electron
A. CHƯƠNG I+II: NGUYÊN TỬ+ BẢNG TUẦN HOÀN
Câu 1: Hạt nhân nguyên tử có hạt nào sau đây không mang điện?
A. hạt p B. hạt n
C. hạt e D. hạt mang điện tích dương
Câu 2: Kí hiệu hóa học biểu thị đầy đủ đặc trưng cho nguyên tử của nguyên tố hóa học vì nó cho biết:
A. số hiệu nguyên tử B. số A
C. nguyên tử khối của nguyên tử D. số A và số Z
Câu 3: Nguyên tử có số khối là 19, số electron là 9. vậy số proton là
A. 9 B. 28 C. 10 D. 19
Câu 4: Nguyên tố Clo, lớp ngoài cùng có dạng 3s23p5.
Vị trí của Clo trong bảng tuần hoàn là ô thứ
A. 13 B. 12 C. 17 D. 16
Câu 5: Nguyên tử có số khối A là:
A. 58. B. 20 C. 39. D. 19
Câu 6: Trong phân lớp d có số electron tối đa là bao nhiêu?
A. 8 B. 10 C. 14 D. 2
Câu 7: Nguyêntố X thuộc ô số12, chu kì 3, nhóm IIA trong bảng tuần hoàn. X là nguyên tố gì?
A. Phi kim B. Khí hiếm C. Lưỡng tính D. Kim loại
Câu 8: Nguyên tố nào trong số các nguyên tố: 8O, 9F, 15P, 16S có tính phi kim yếu nhất?
A. O. B. P. C. S. D. F.
Câu 9: Số electron tối đa trong lớp M là
A. 8. B. 32. C. 18. D. 2.
Câu 10: Nguyên tử các nguyên tố X, Y, Z có cấu hình electron là
X: 1s22s22p63s23p4 Y: 1s22s22p63s23p6 Z: 1s22s22p63s23p64s2
Trong các nguyên tố X, Y, Z nguyên tố kim loại là
A. X B. Y C. Z D. X và Y
Câu 11: Nguyên tử khối trung bình của bạc là 107,87. Cho rằng bạc có hai đồng vị, trong đó 107Ag chiếm a% số nguyên tử, đồng vị 109Ag chiếm a% số nguyên tử . giá trị của a và b là Số khối của đồng vị còn lại là
A. 56,5% và 43,5% . | B. 35,5% và 65,5%. | C. 46,33% và 53,67%. | D. 10% và 90%. |
Câu 12: Oxit cao nhất của một nguyên tử R ứng với công thức RO2. Trong hợp chất của nguyên tố đó với H có 75%R và 25%H. Nguyên tố R đó là:
A. Cacbon. B. Nitơ. C. Magie. D. Photpho.
Câu 13: Hoà tan hoàn toàn 7,8 gam một kim loại thuộc nhóm IA bằng dung dịch HCl thu được 2,24 lít khí H2 (đktc). Kim loại đó là:
A. Na. B. K. C. Mg. D. Ca.
Câu 14: Cho 2,3 gam kim loại kali phản ứng hoàn toàn với lượng nước dư, thu được V lít khí H2 (ở đktc). Giá trị của V là
A. 1,12. | B. 2,24. | C. 4,48. | D. 3,36. |
Câu 1: Hạt nhân nguyên tử có hạt nào sau đây không mang điện?
A. hạt p B. hạt n
C. hạt e D. hạt mang điện tích dương
Câu 2: Kí hiệu hóa học biểu thị đầy đủ đặc trưng cho nguyên tử của nguyên tố hóa học vì nó cho biết:
A. số hiệu nguyên tử B. số A
C. nguyên tử khối của nguyên tử D. số A và số Z
Câu 3: Nguyên tử có số khối là 19, số electron là 9. vậy số proton là
A. 9 B. 28 C. 10 D. 19
Câu 4: Nguyên tố Clo, lớp ngoài cùng có dạng 3s23p5.
Vị trí của Clo trong bảng tuần hoàn là ô thứ
A. 13 B. 12 C. 17 D. 16
Câu 5: Nguyên tử có số khối A là:
A. 58. B. 20 C. 39. D. 19
Câu 6: Trong phân lớp d có số electron tối đa là bao nhiêu?
A. 8 B. 10 C. 14 D. 2
Câu 7: Nguyêntố X thuộc ô số12, chu kì 3, nhóm IIA trong bảng tuần hoàn. X là nguyên tố gì?
A. Phi kim B. Khí hiếm C. Lưỡng tính D. Kim loại
Câu 8: Nguyên tố nào trong số các nguyên tố: 8O, 9F, 15P, 16S có tính phi kim yếu nhất?
A. O. B. P. C. S. D. F.
Câu 9: Số electron tối đa trong lớp M là
A. 8. B. 32. C. 18. D. 2.
Câu 10: Nguyên tử các nguyên tố X, Y, Z có cấu hình electron là
X: 1s22s22p63s23p4 Y: 1s22s22p63s23p6 Z: 1s22s22p63s23p64s2
Trong các nguyên tố X, Y, Z nguyên tố kim loại là
A. X B. Y C. Z D. X và Y
Câu 11: Nguyên tử khối trung bình của bạc là 107,87. Cho rằng bạc có hai đồng vị, trong đó 107Ag chiếm a% số nguyên tử, đồng vị 109Ag chiếm a% số nguyên tử . giá trị của a và b là Số khối của đồng vị còn lại là
A. 56,5% và 43,5% . | B. 35,5% và 65,5%. | C. 46,33% và 53,67%. | D. 10% và 90%. |
Câu 12: Oxit cao nhất của một nguyên tử R ứng với công thức RO2. Trong hợp chất của nguyên tố đó với H có 75%R và 25%H. Nguyên tố R đó là:
A. Cacbon. B. Nitơ. C. Magie. D. Photpho.
Câu 13: Hoà tan hoàn toàn 7,8 gam một kim loại thuộc nhóm IA bằng dung dịch HCl thu được 2,24 lít khí H2 (đktc). Kim loại đó là:
A. Na. B. K. C. Mg. D. Ca.
Câu 14: Cho 2,3 gam kim loại kali phản ứng hoàn toàn với lượng nước dư, thu được V lít khí H2 (ở đktc). Giá trị của V là
A. 1,12. | B. 2,24. | C. 4,48. | D. 3,36. |
Thu gọn
Câu 13: Nguyên tử của nguyên tố X có tổng số hạt là 40 .Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt .Nguyên tố X có số khối là :
A. 27 B. 26 C. 28 D.23
Câu 14: Trong nguyên tử một nguyên tố A có tổng số các loại hạt là 58. Biết số hạt p ít hơn số hạt n là 1 hạt. Kí hiệu của A là
Câu 15: Tổng các hạt cơ bản trong một nguyên tử là 155 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 33 hạt. Số khối của nguyên tử đó là
A. 119 B. 113 C. 112 D. 108
Câu 16: Tổng các hạt cơ bản trong một nguyên tử là 82 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Số khối của nguyên tử đó là
A. 57 B. 56 C. 55 D. 65
Câu 17: Ngtử của nguyên tố Y được cấu tạo bởi 36 hạt .Trong hạt nhân, hạt mang điện bằng số hạt không mang điện.
1/ Số đơn vị điện tích hạt nhân Z là : A. 10 B. 11 C. 12 D.15
2/ Số khối A của hạt nhân là : A . 23 B. 24 C. 25 D. 27
Câu 18: Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện.Điện tích hạt nhân của X là:
A. 18 B. 17 C. 15 D. 16
Câu 19: Nguyªn tö nguyªn tè X ®îc cÊu t¹o bëi 36 h¹t, trong ®ã sè h¹t mang ®iÖn gÊp ®«i sè h¹t kh«ng mang ®iÖn. §iÖn tÝch h¹t nh©n cña X lµ:
A. 10 B. 12 C. 15 D. 18
Câu 20: Nguyên tử của một nguyên tố có 122 hạt p,n,e. Số hạt mang điện trong nhân ít hơn số hạt không mang điện là 11 hạt. Số khối của nguyên tử trên là:
A. 122 B. 96 C. 85 D. 74
Câu 21: Nguyên tử X có tổng số hạt p,n,e là 52 và số khối là 35. Số hiệu nguyên tử của X là
A. 17 B. 18 C. 34 D. 52
Câu 22: Nguyên tử X có tổng số hạt p, n, e là 28 hạt. Kí hiệu nguyên tử của X là
Câu 23:Tổng số hạt p,n,e là 13.số khối của nguyên tử là
A. 8 B. 10 C. 11 D. Tất cả đều sai
Câu 24: Tổng số hạt mang điện trong ion AB43- là 50. Số hạt mang điện trong nguyên tử A nhiều hơn số hạt mang điện trong hạt nhân nguyên tử B là 22. Số hiệu nguyên tử A, B lần lượt là:
A. 16 và 7 B. 7 và 16 C. 15 và 8 D. 8 và 15
Câu 25: Trong phân tử M2X có tổng số hạt p,n,e là 140, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của M lớn hơn số khối của X là 23. Tổng số hạt p,n,e trong nguyên tử M nhiều hơn trong nguyên tử X là 34 hạt. CTPT của M2X là:
A. K2O B. Rb2O C. Na2O D. Li2O
Câu 26: Trong phân tử MX2 có tổng số hạt p,n,e bằng 164 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 52 hạt. Số khối của nguyên tử M lớn hơn số khối của nguyên tử X là 5. Tổng số hạt p,n,e trong nguyên tử M lớn hơn trong nguyên tử X là 8 hạt. Tổng số hạt p,n,e trong nguyên tử M lớn hơn trong nguyên tử X là 8 hạt. Số hiệu nguyên tử của M là:
A. 12 B. 20 C. 26 D. 9
13.C
14.Kali(K)
15.D
16.B
17.C;B
18.D
19.B
20.C
21.A
22.Flo(F)
23.D
24.C
25.A
26.A