Những câu hỏi liên quan
C1: Viết các PTHH để thực hiện sơ đồ chuyển hóa sau:
Fe(OH)3 - Fe2O3 - Fe - FeSO4 - FeCl2 - Fe(OH)2
C2: Hòa tan hoàn toàn 11,1 gam hỗn hợp X gồm Al và Fe bằng 1 lượng dư dd HCl, thu được 6,72 lít khí H2 (đktc)
a. Viết PTHH của các pư xảy ra và tính phần trăm khối lượng của từng chất trong X
b) Khi cho 11,1 gam X pư hết với khí Cl2(dư) thì có q mol Cl2 tham gia pư. Tính giá trị của q
c) Bằng phương pháp hóa học hãy trình bày sơ đồ tách riêng kim loại ra khỏi hỗn hợp X
Đọc tiếp
C1: Viết các PTHH để thực hiện sơ đồ chuyển hóa sau: Fe(OH)3 -> Fe2O3 -> Fe -> FeSO4 -> FeCl2 -> Fe(OH)2 C2: Hòa tan hoàn toàn 11,1 gam hỗn hợp X gồm Al và Fe bằng 1 lượng dư dd HCl, thu được 6,72 lít khí H2 (đktc) a. Viết PTHH của các pư xảy ra và tính phần trăm khối lượng của từng chất trong X b) Khi cho 11,1 gam X pư hết với khí Cl2(dư) thì có q mol Cl2 tham gia pư. Tính giá trị của q c) Bằng phương pháp hóa học hãy trình bày sơ đồ tách riêng kim loại ra khỏi hỗn hợp X
viết các phương trình hóa học để thực hiện sơ đồ chuyển hóa sau: Fe(OH)3—Fe2O3—Fe—FeSO4—FeCl2—Fe(OH)2 Enter Viết cho Thân Huy Hùng
Đọc tiếp
viết các phương trình hóa học để thực hiện sơ đồ chuyển hóa sau: Fe(OH)3—>Fe2O3—>Fe—>FeSO4—>FeCl2—>Fe(OH)2 Enter Viết cho Thân Huy Hùng
2Fe(OH)3 --to-> Fe2O3 + 3H2O
Fe2O3 + 3H2 ---> 2Fe + 3H2O
Fe + H2SO4 --> FeSO4 + H2
FeSO4 + PbCl2 --> FeCl2+PbSO4
FeCl2 + Ba(OH)2 --> Fe(OH)2+BaCl2
Đúng 3
Bình luận (0)
Bài tập về nhà:1) Thực hiện dãy chuyển hóa sau:FeS2 (1) Fe2O3 (2) Fe (3) FeSO4 (4) Fe(NO)2 (5) Fe(OH)2 (6) Fe2O32. Chia m gam hỗn hợp X gồm Al và Fe thành 2 phần bằng nhau:Phần 1: Cho tác dụng với dung dịch NaOH dư thu được 3,36 lít H2 (đktc)Phần 2: Cho vào 146 gam dd HCl 20% thu được dung dịch Y và 6,72 lít khí (ddktc)a. Tính m?b. Tính nồng độ % các chất trong Y?c. Tính V Cl2 (dktc) để phản ứng hết với hỗn hợp X?
Đọc tiếp
Bài tập về nhà:
1) Thực hiện dãy chuyển hóa sau:
FeS2 (1) Fe2O3 (2) Fe (3) FeSO4 (4) Fe(NO)2 (5) Fe(OH)2 (6) Fe2O3
2. Chia m gam hỗn hợp X gồm Al và Fe thành 2 phần bằng nhau:
Phần 1: Cho tác dụng với dung dịch NaOH dư thu được 3,36 lít H2 (đktc)
Phần 2: Cho vào 146 gam dd HCl 20% thu được dung dịch Y và 6,72 lít khí (ddktc)
a. Tính m?
b. Tính nồng độ % các chất trong Y?
c. Tính V Cl2 (dktc) để phản ứng hết với hỗn hợp X?
Hòa tan hỗn hợp A gồm Fe, FeO, Fe2O3, Fe3O4, Fe(OH)2, Fe(OH)3, FeCO3 trong dung dịch HCl dư thu được 2,688 lít (đktc) hỗn hợp khí có tỉ khối so với He bằng 5,75 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn lượng hỗn hợp rắn A như trên trong dung dịch HNO3 dư thu được dung dịch X chứa 96,8 gam một muối và 4,48 lít (đktc) gồm 2 khí, trong đó có một khí hóa nâu trong không khí. Giá trị của m là A. 29,660 B. 59,320 C. 27,175 D. 54,350
Đọc tiếp
Hòa tan hỗn hợp A gồm Fe, FeO, Fe2O3, Fe3O4, Fe(OH)2, Fe(OH)3, FeCO3 trong dung dịch HCl dư thu được 2,688 lít (đktc) hỗn hợp khí có tỉ khối so với He bằng 5,75 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn lượng hỗn hợp rắn A như trên trong dung dịch HNO3 dư thu được dung dịch X chứa 96,8 gam một muối và 4,48 lít (đktc) gồm 2 khí, trong đó có một khí hóa nâu trong không khí. Giá trị của m là
A. 29,660
B. 59,320
C. 27,175
D. 54,350
Đáp án : D
+) A + HCl : 2 khí là H2 và CO2 => nH2 = nCO2 = 0,06 mol
=> nFe = nFeCO3 = 0,06 mol
+) A + HNO3 -> 1 muối là Fe(NO3)3 có n = 0,4 mol
Hỗn hợp khí gồm CO2 và khí hóa nâu ngoài không khí là NO
=> nCO2 + nNO = 0,2 mol => nNO = 0,14 mol
Bảo toàn e : 3nFe + nFe2+(oxit,hidroxit) + nFeCO3 = 3nNO
=> nFe2+(oxit,hidroxit) = 0,18 mol
Bảo toàn Fe : nFe2+(oxit,hidroxit) + nFe3+(oxit,hidroxit) + nFe + nFeCO3 = 0,4 mol
=> nFe3+(oxit,hidroxit) = 0,1 mol
+) A + HCl -> muối gồm FeCl2 và FeCl3
=> nFeCl3 = nFe3+(oxit,hidroxit) = 0,1 mol
Và nFeCl2 = nFe2+(oxit,hidroxit) + nFe + nFeCO3 = 0,3 mol
=> m = 54,35g
Đúng 0
Bình luận (0)
Bài 1: Viết PTHH thực hiện chuyển đổi hóa học sau:Al2O3 AlCl3 Al(OH)3 Al2O3 AlFe2O3 FeCl3 Fe(OH)3 Fe2O3 Fe Bài 2: Bằng phương pháp hóa học hãy nhận biết các kim loại sau: Al, Fe, Ag.Bài 3: Hòa tan 8,08g hỗn hợp 2 kim loại Fe, Cu phản ứng với dung dịch HCl 3,65%,sau phảnứng thu được 0,672 lít H2 ở đktcA. Viết PTHH.B. Tính% khối lượng mỗi kim loại trong hỗn hợp ban đầu ?C. Tính khối lượng dung dịch HCl 3,65% đã tham gia phản ứng?
Đọc tiếp
Bài 1: Viết PTHH thực hiện chuyển đổi hóa học sau:
Al2O3![]() AlCl3
AlCl3 ![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3![]() Al
Al
Fe2O3![]() FeCl3
FeCl3 ![]() Fe(OH)3
Fe(OH)3![]() Fe2O3
Fe2O3![]() Fe
Fe
Bài 2: Bằng phương pháp hóa học hãy nhận biết các kim loại sau: Al, Fe, Ag.
Bài 3: Hòa tan 8,08g hỗn hợp 2 kim loại Fe, Cu phản ứng với dung dịch HCl 3,65%,sau phảnứng thu được 0,672 lít H2 ở đktc
A. Viết PTHH.
B. Tính% khối lượng mỗi kim loại trong hỗn hợp ban đầu ?
C. Tính khối lượng dung dịch HCl 3,65% đã tham gia phản ứng?
\(1.a.Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3+3NaCl\\ 2Al\left(OH\right)_3-^{t^o}\rightarrow Al_2O_3+3H_2O\\ b.Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\\ 2Fe\left(OH\right)_3-^{t^o}\rightarrow Fe_2O_3+3H_2O\\ Fe_2O_3+3CO\rightarrow2Fe+3CO_2\)
Đúng 1
Bình luận (0)
2. Cho các mẫu thử vào dung dịch NaOH dư
+ Tan, có khí thoát ra: Al
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
+ Không hiện tượng: Fe, Ag
Cho 2 mẫu thử không hiện tượng trên vào dung dịch HCl
+ Tan, có khí thoát ra: Fe
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
+ Không hiện tượng : Ag
Đúng 1
Bình luận (0)
\(3.a.Fe+2HCl\rightarrow FeCl_2+H_2\\ b.n_{Fe}=n_{H_2}=0,03\left(mol\right)\\ \Rightarrow\%m_{Fe}=\dfrac{0,03.56}{8,08}.100=20,79\%;\%m_{Cu}=79,01\%\\ c.n_{HCl}=2n_{H_2}=0,06\left(mol\right)\\ \Rightarrow m_{HCl}=\dfrac{0,06.36,5}{3,65\%}=60\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 11,1 gam hỗn hợp gồm Fe và kim loại X hóa trị không đổi bằng dung dịch HCl, thu được 6,72 lít khí
H
2
. Mặt khác, hòa tan hoàn toàn 11,1 gam hỗn hợp trên bằng dung dịch
HNO
3
loãng (dư), thu được 5,6 lít khí NO (sản phẩm khử duy nhất). Biết các thể tích khí đều đo ở điều kiện tiêu chuẩn. Kim loại X là A. Zn B. Al C. Cr D. Mg
Đọc tiếp
Hòa tan hoàn toàn 11,1 gam hỗn hợp gồm Fe và kim loại X hóa trị không đổi bằng dung dịch HCl, thu được 6,72 lít khí H 2 . Mặt khác, hòa tan hoàn toàn 11,1 gam hỗn hợp trên bằng dung dịch HNO 3 loãng (dư), thu được 5,6 lít khí NO (sản phẩm khử duy nhất). Biết các thể tích khí đều đo ở điều kiện tiêu chuẩn. Kim loại X là
A. Zn
B. Al
C. Cr
D. Mg
Hòa tan hoàn toàn hỗn hợp M gồm Fe, FeCO3, Fe2O3, Fe(OH)2, Fe(OH)3 trong dung dịch HCl dư thu được 0,672 lít hỗn hợp khí E có tỉ khối so với He bằng 7,5 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn hỗn hợp M trong dung dịch HNO3 dư, thu được dung dịch chứa 33,88 gam muối và 1,12 lit hỗn hợp khí T gồm NO và CO2. Biết các thể tích khí đo ở đktc và NO là sản phẩm khử duy nhất của NO3-. Giá trị của m là A. 20,265. B. 15,375. C. 9,970. D. 11,035.
Đọc tiếp
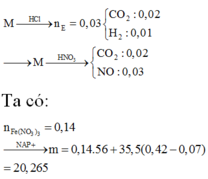
Hòa tan hoàn toàn hỗn hợp M gồm Fe, FeCO3, Fe2O3, Fe(OH)2, Fe(OH)3 trong dung dịch HCl dư thu được 0,672 lít hỗn hợp khí E có tỉ khối so với He bằng 7,5 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn hỗn hợp M trong dung dịch HNO3 dư, thu được dung dịch chứa 33,88 gam muối và 1,12 lit hỗn hợp khí T gồm NO và CO2. Biết các thể tích khí đo ở đktc và NO là sản phẩm khử duy nhất của NO3-. Giá trị của m là
A. 20,265.
B. 15,375.
C. 9,970.
D. 11,035.
Hòa tan hoàn toàn hỗn hợp M gồm Fe, FeCO3, Fe2O3, Fe(OH)2, Fe(OH)3 trong dung dịch HCl dư thu được 0,672 lít hỗn hợp khí E có tỉ khối so với He bằng 7,5 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn hỗn hợp M trong dung dịch HNO3 dư, thu được dung dịch chứa 33,88 gam muối và 1,12 lit hỗn hợp khí T gồm NO và CO2. Biết các thể tích khí đo ở đktc và NO là sản phẩm khử duy nhất của NO3-. Giá trị của m là A. 20,265 B. 15,375 C. 9,970 D. 11,035
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp M gồm Fe, FeCO3, Fe2O3, Fe(OH)2, Fe(OH)3 trong dung dịch HCl dư thu được 0,672 lít hỗn hợp khí E có tỉ khối so với He bằng 7,5 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn hỗn hợp M trong dung dịch HNO3 dư, thu được dung dịch chứa 33,88 gam muối và 1,12 lit hỗn hợp khí T gồm NO và CO2. Biết các thể tích khí đo ở đktc và NO là sản phẩm khử duy nhất của NO3-. Giá trị của m là
A. 20,265
B. 15,375
C. 9,970
D. 11,035
Hòa tan hoàn toàn 23,2 gam hỗn hợp (X) gồm Fe và FeS trong dung dịch HCl (dư). Sau khi phản ứng hoàn toàn thu được 6,72 lít hỗn hợp khí (A) gồm H2 và H2S đo ở đktc.
a) Viết phản ứng hóa học xảy ra.
b) Tính % khối lượng Fe và FeS trong (X)
c) Tính % thể tích mỗi khí trong (A)
Gọi số mol của Fe và FeS lần lượt là x và y
a) \(Fe+2HCl->FeCl_2+H_2\)
x.........................................x
\(FeS+2HCl->FeCl_2+H_2S\)
y............................................y
b) ta có n A = x+y = 6,72:22,4=0,3 mol
ta lại có m X = 56x+ 88y = 23,2 g
=> x=0,1 mol y=0,2 mol
=> m Fe = 0,1. 56 =5,6 g
% Fe = \(\dfrac{5,6}{23,2}.100\sim24,14\%\)
=> %FeS = \(100\%-24,14\%\sim75,86\%\)
c) V H2 = 0,1.22,4=2,24 lít
=> % H2 = \(\dfrac{2,24}{6,72}.100\sim33,34\%\)
% H2S = 100%-33,34%∼66,67%
Đúng 0
Bình luận (7)