tính khối lượng bằng gam của 6.1023 Al2O3, biết C = 1,9926.1023g.

Những câu hỏi liên quan
Bài 7: a) Tính khối lượng của 0,5 mol sắt.b) Cho biết khối lượng của 6.1023 phân tử của mỗi chất sau: CO2; Al2O3; C6H12O6; H2SO4.Bài 8: a) Trong 112 gam canxi có bao nhiêu mol canxi?b) Tính khối lượng của 0,5 mol axit clohidric (HCl).c) Trong 49 gam axit sunfuric có bao nhiêu mol H2SO4.
Đọc tiếp
Bài 7: a) Tính khối lượng của 0,5 mol sắt.
b) Cho biết khối lượng của 6.1023 phân tử của mỗi chất sau: CO2; Al2O3; C6H12O6; H2SO4.
Bài 8: a) Trong 112 gam canxi có bao nhiêu mol canxi?
b) Tính khối lượng của 0,5 mol axit clohidric (HCl).
c) Trong 49 gam axit sunfuric có bao nhiêu mol H2SO4.
Bài 7:
\(a.m_{Fe}=0,5.56=28\left(g\right)\\ b.n_{p.tử}=\dfrac{6.10^{23}}{6.10^{23}}=1\left(mol\right)\\ m_{CO_2}=44.1=44\left(g\right)\\ m_{Al_2O_3}=1.102=102\left(g\right)\\ m_{C_6H_{12}O_6}=180.1=180\left(g\right)\\ m_{H_2SO_4}=98.1=98\left(g\right)\)
Bài 8:
\(a.n_{Ca}=\dfrac{112}{40}=2,8\left(mol\right)\\ b.m_{HCl}=36,5.0,5=18,25\left(g\right)\\ c.n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
Đúng 3
Bình luận (4)
Tính khối lượng Nitơ có trong:
a) 8,8 gam N2O. b) 6.1023 phân tử NH4NO3. c) 6,72 lít khí NO ( đktc).
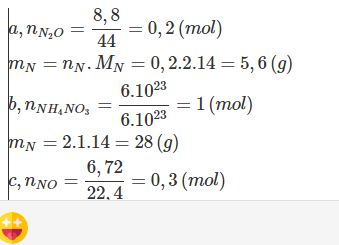
=> mN=nN.14=0,3.14=4,2(g)
Nãy lỗi mạng quá
Đúng 0
Bình luận (0)
\(a.n_{N_2O}=\dfrac{8,8}{44}=0,2\left(mol\right)\\ \Rightarrow n_N=2n_{N_2O}=0,4\left(mol\right)\\ \Rightarrow m_N=0,4.14=5,6\left(g\right)\\ b.n_N=2n_{NH_4NO_3}=\dfrac{2.6.10^{23}}{6.10^{23}}=2\left(mol\right)\\ \Rightarrow m_N=2.14=28\left(g\right)\\ c.n_N=n_{NO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ \Rightarrow m_N=0,3.14=4,2\left(g\right)\)
Đúng 0
Bình luận (0)
Biết khối lượng tính bằng gam của 1 nguyên tử C bằng 1,9926.10-23. Khối lượng tính bằng gam của nguyên tử canxi là bao nhiêu?
\(m_{Ca}=\dfrac{40}{12}.1,9926.10^{-23}=6,642.10^{-23}\left(g\right)\)
Đúng 4
Bình luận (0)
Trường hợp nào sau đây chưa khối lượng nguyên tử hidro lớn nhất
a) 6 . 10 23 phân tử H 2
b) 3 . 10 23 phân tử H 2 O
c) 0,6 gam C H 4
d) 1,498 gam N H 4 C l
Có một hỗn hợp A gồm Al2O3, CaCO3, MgCO3 trong đó khối lượng của Al2O3 bằng 1/8 tổng khối lượng của hai muối Cacbonat
1) Tính % khối lượng Al2O3 trong A
2) Nung A đến hỗn hợp không đổi, thì chất rắn còn lại chỉ bằng 1/10 khối lượng của A. Tính % khối lượng của CaCO3 trong A.
Hòa tan m gam Al2O3 bằng một lượng vừa đủ 100ml dung dịch H2So4,8M
A) tìm giá trị của m
B ) tính khối lượng muối tạo thành
C) nếu không dùng H2So4 mà dùng dung dịch KOH cùng nồng độ mol thì thể tích dung dịch KOH cần hòa tan m gam Al2O3 là bao nhiu?
a) $n_{H_2SO_4} = 0,1.4,8 = 0,48(mol)$
$Al_2O_3 + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2O$
$n_{Al_2O_3} = \dfrac{1}{3}n_{H_2SO_4} =0,16(mol)$
$m = 0,16.102 = 16,32(gam)$
b)
$n_{Al_2(SO_4)_3} = n_{Al_2O_3} = 0,16(mol)$
$m_{muối} = 0,16.342 = 54,72(gam)$
c)
$Al_2O_3 + 2KOH \to 2KAlO_2 + H_2O$
$n_{KOH} = 2n_{Al_2O_3} = 0,32(mol)$
$V_{dd\ KOH} = \dfrac{0,32}{4,8} = 0,067(lít)$
Đúng 3
Bình luận (0)
Ta có: \(n_{H_2SO_4}=0,1.4,8=0,48\left(mol\right)\)
PT: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
___0,16_____0,48______0,16 (mol)
a, m = mAl2O3 = 0,16.102 = 16,32 (g)
b, mAl2(SO4)3 = 0,16.342 = 54,72 (g)
c, \(Al_2O_3+2KOH\rightarrow2KAlO_2+H_2O\)
____0,16____0,32 (mol)
\(\Rightarrow V_{ddKOH}=\dfrac{0,32}{4,8}=\dfrac{1}{15}\left(l\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Đốt cháy nhôm trong không khí thu được nhôm oxit Al2O3. Tính khối lượng nhôm oxit tạo thành biết khối lượng nhôm và oxi phản ứng lần lượt là 10,8 gam và 9,6 gam.
Theo ĐLBTKL thì
m Al + m O2 = m Al2O3
10,8 + 9,6 = a
=> a = 20,4 g
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 10,2 gam Al2O3 vào 200 gam dung dịch H2SO4 loãng vừa đủ. a/. Tính khối lượng muối thu được sau phản ứng ? b/. Tính nồng độ phần trăm của dung dịch H2SO4 cần dùng? c/. Tính nồng độ phần trăm của dung dịch muối tạo thành? (khối lượng dung dịch sau phản ứng khối lượng các chất ban đầu) (Biết Al27, O16, H1, S32)
Đọc tiếp
Hoà tan hoàn toàn 10,2 gam Al2O3 vào 200 gam dung dịch H2SO4 loãng vừa đủ.
a/. Tính khối lượng muối thu được sau phản ứng ?
b/. Tính nồng độ phần trăm của dung dịch H2SO4 cần dùng?
c/. Tính nồng độ phần trăm của dung dịch muối tạo thành?
(khối lượng dung dịch sau phản ứng = khối lượng các chất ban đầu)
(Biết Al=27, O=16, H=1, S=32)
Biết giá trị khối lượng tính bằng gam của nguyên tử cacbon là 1,9926.10-23 (g). Hãy tính xem một đơn vị cacbon tương ứng bao nhiêu gam? Khối lượng tính bằng gam của nguyên tử nhôm là A, B, C hay D?
a. Ta có : C = 12 đvC = 1,9926.10-23 (g)
=> 1 đvC = (1,9926.10-23) : 12 ≈ 1,66.10-24 (g).
b. Khối lượng tính bằng gam của nguyên tử nhôm là :
mAl = 27 đvC = 27. 1,66.10-24 = 4,482.10-23 (g)
Đúng 2
Bình luận (6)






















