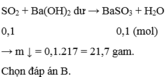
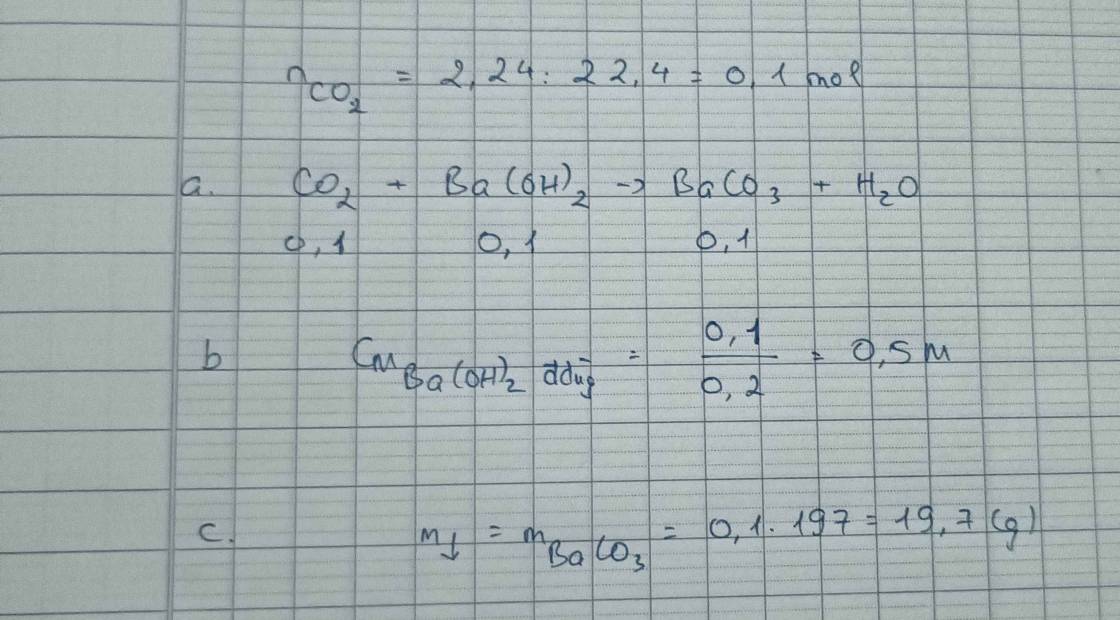Bài tập:Cho 2,24 lít (đktc)tác dụng với dung dịch Ba(OH)\(_2\)dư.Tính khối lượng chất kết tạo thành

Những câu hỏi liên quan
Cho 2,24 lít C O 2 (đktc) tác dụng với dung dịch Ba( O H ) 2 dư. Khối lượng chất kết tủa thu được là :
A. 19,7 g
B. 19,5 g
C. 19,3 g
D. 19 g
Chọn A
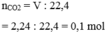
Vì Ba( O H ) 2 dư do đó chỉ xảy ra phản ứng tạo kết tủa
PTHH:
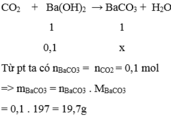
Đúng 0
Bình luận (0)
3/ Cho 1,12 lít khí CO2 (đktc) tác dụng vừa đủ với 100ml dung dịch KOH tạo thành muối và nước. Tìm nồng độ mol của dung dịch KOH tạo ra.4/ Cho 2,24 lít khí CO2 (đktc) tác dụng vừa đủ với 100ml dung dịch Ba(OH)2 tạo thành muối và nước. Khối lượng muối kết tủa được tạo ra là bao nhiêu gam?5/ Nhiệt phân hoàn toàn 19,6 gam Cu(OH)2 thu được chất rắn màu đen, dùng khí H2 (dư) khử chất rắn màu đen ở nhiệt độ cao. Vậy khối chất rắn sau khi nung là bao nhiêu gam?6/ Thể tích dung dịch H2SO4 2M. Khi cho 50...
Đọc tiếp
3/ Cho 1,12 lít khí CO2 (đktc) tác dụng vừa đủ với 100ml dung dịch KOH tạo thành muối và nước. Tìm nồng độ mol của dung dịch KOH tạo ra.
4/ Cho 2,24 lít khí CO2 (đktc) tác dụng vừa đủ với 100ml dung dịch Ba(OH)2 tạo thành muối và nước. Khối lượng muối kết tủa được tạo ra là bao nhiêu gam?
5/ Nhiệt phân hoàn toàn 19,6 gam Cu(OH)2 thu được chất rắn màu đen, dùng khí H2 (dư) khử chất rắn màu đen ở nhiệt độ cao. Vậy khối chất rắn sau khi nung là bao nhiêu gam?
6/ Thể tích dung dịch H2SO4 2M. Khi cho 500ml dung dịch NaOH 1M tác dụng với dung dịch H2SO4 2M tạo thành muối trung hoà và nước.
7/ Cho 200 gam dung dịch KOH 5,6% vào dung dịch CuCl2 dư, sau phản ứng thu được lượng chất kết tủa Cu(OH)2 là bao nhiêu gam?
8/ Khi cho 100ml dung dịch H2SO4 2M tác dụng với 100ml dung dịch Ba(NO3)2. Tìm nồng độ mol của dung dịch Ba(NO3)2
9/ Súc miệng bằng dung dịch nước muối 0,9% có tác dụng bảo vệ niêm mạc và sát khuẩn. Số gam NaCl cần lấy để pha 300 gam dung dịch nước muối 0,9% là bao nhiêu.
Cho 2,24 lít khí CO2(đktc) tác dụng vừa hết với 200 ml dung dịch BA(OH)2 tạo ra muối trung hoà và nước.Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng và khối lượng chất kết tủa thu được
Giải chi tiết giúp mik với ạ
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH CO2 + Ba(OH)2 --> BaCO3 + H2O
CO2 phản ứng với Ba(OH)2 tạo muối trung hòa
nBa(OH)2 = nCO2=0,1 mol
=> \(CM_{Ba\left(OH\right)_2}=\dfrac{0,1}{0,2}=0,5M\)
nBaCO3 = nCO2=0,1mol
=> \(m_{BaCO_3}=0,2.197=19,7\left(g\right)\)
Đúng 5
Bình luận (2)
Câu 4: Cho 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200ml dung dịch Ba(OH)2, sản phẩm chỉ tạo muối trung hòa và nước.
a) Viết PTHH.
b) Tính khối lượng chất kết tủa thu được
c) Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng
\(a.n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\\ 0,1...........0,1.............0,1..........0,1\left(mol\right)\\ b.m_{kt}=m_{BaCO_3}=0,1.197=19,7\left(g\right)\\ c.C_{MddBa\left(OH\right)_2}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Đúng 1
Bình luận (0)
: Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2a/ Viết phương trình hóa học.b/ Tính nồng độ mol/lít của dung dịch Ba(OH)2 đã dùng.c/ Tính khối lượng chất kết tủa thu được
Đọc tiếp
: Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2
a/ Viết phương trình hóa học.
b/ Tính nồng độ mol/lít của dung dịch Ba(OH)2 đã dùng.
c/ Tính khối lượng chất kết tủa thu được
biết 4,48 lít khí \(CO_2\)(ĐKTC)tác dụng vừa hết với 200ml dd \(Ba\left(OH\right)_2\) sản phẩm là \(BaCO_3\) VÀ \(H_2O\)
a)viết pthh
b)tính nồng độ mol của dung dịch\(Ba\left(OH\right)_2\) ĐÃ DÙNG
c)tính khối lượng chất kết tủa thu đc
ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(a.PTHH:CO_2+Ba\left(OH\right)_2--->BaCO_3\downarrow+H_2O\)
b. Theo PT: \(n_{Ba\left(OH\right)_2}=n_{BaCO_3}=n_{CO_2}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,2}{\dfrac{200}{1000}}=1M\)
c. Ta có: \(m_{BaCO_3}=0,2.197=39,4\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 2,24 lít C O 2 (đktc) tác dụng với dung dịch C a ( O H ) 2 dư. Khối lượng chất kết tủa thu được là
A. 10 g
B. 19,7 g
C. 5 g
D. 20 g
Biết 2,24 lít khí cacbonic(đktc) tác dụng vừa hết với 200ml dung dịch Ba(OH)2 sản phẩm là baricacbonat và nước
a) Viết PTPƯ
b) Tính nồng độ mol của dung dịch barihiđroxit đã dùng.
c) Tính khối lượng chất kết tủa.
Số mol của khí cacbonic ở dktc
nCO2= \(\dfrac{V_{CO2}}{22,4}=\dfrac{4,48}{22,4}=0,1\left(mol\right)\)
a) Pt : CO2 + Ba(OH)2 → BaCO3 + H2O\(|\)
1 1 1 1
0,1 0,1 0,1
Số mol của dung dịch bari hidroxit
nBa(OH)2 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
200ml = 0,2l
Nồng độ mol của dung dịch bari hidroxit đã dùng
CMBa(OH)2 = \(\dfrac{n}{V}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
c) số mol của bari cacbonat
nBaCO3 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Khối lượng của bari cacbonat
mBaCO3 = nBaCO3 . MBaCO3
= 0,1. 197
= 19,7 (g)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Dẫn 2,24 lít S O 2 (đktc) vào lượng dư dung dịch B a ( O H ) 2 . Khối lượng kết tủa tạo thành sau phản ứng là
A. 29,9 gam.
B. 21,7 gam.
C. 20,8 gam.
D. 26,2 gam.