Hoà tan 2O,7g hỗn hợp gồm 3 kim loại Cu,Al,Zn vào dung dịch H2SO4 . Sau fản ứng thu được 5g chất rắn không tan và 7,84l khí ở ĐKtc
Tính khối lượng của mỗi kim loại trong hỗn hợp đầu

Những câu hỏi liên quan
Hoà tan 5,64g Cu(NO3)2 và l,7g AgNO3 vào H2O thu dung dịch X. Cho l,57g hỗn hợp Y gồm bột Zn và Al vào X rồi khuấy đều. Sau khi phản ứng hoàn toàn thu chất rắn E và dung dịch D chỉ chứa 2 muối. Ngâm E trong dung dịch H2SO4 loãng không có khí giải phóng. Tính khối lượng của mỗi kim loại trong hỗn hợp Y. A. Zn: 0,65g, Al: 0,92g B. Zn: 0,975g, Al: 0,595g C. Zn: 0,6g, Al: 0,97g D. Đáp án khác
Đọc tiếp
Hoà tan 5,64g Cu(NO3)2 và l,7g AgNO3 vào H2O thu dung dịch X. Cho l,57g hỗn hợp Y gồm bột Zn và Al vào X rồi khuấy đều. Sau khi phản ứng hoàn toàn thu chất rắn E và dung dịch D chỉ chứa 2 muối. Ngâm E trong dung dịch H2SO4 loãng không có khí giải phóng. Tính khối lượng của mỗi kim loại trong hỗn hợp Y.
A. Zn: 0,65g, Al: 0,92g
B. Zn: 0,975g, Al: 0,595g
C. Zn: 0,6g, Al: 0,97g
D. Đáp án khác
Đáp án D
Vì D chỉ chứa 2 muối nên D chứa Al(NO3)3 và Zn(NO3)2.
Mà ngâm E trong dung dịch H2SO4 loãng không giải phóng khí nên E chứa Cu và Ag.
Do đó các chất đều phản ứng vừa đủ.
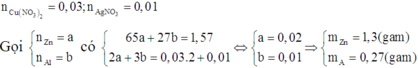
Đúng 0
Bình luận (0)
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là: A. 13,8;7,6;11,8 B. 11,8;9,6;11,8 C. 12,8;9,6;10,8 D. kết quả khác
Đọc tiếp
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là:
A. 13,8;7,6;11,8
B. 11,8;9,6;11,8
C. 12,8;9,6;10,8
D. kết quả khác
Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)
Đúng 0
Bình luận (0)
Ngâm 21,6g hỗn hợp 3 kim loại Zn ,Fe,Cu trong dung dịch H2SO4 Phản ứng thu được 3g chất rắn không tan và 6,72 lít khí đktc
Xác định % Khối lượng của mỗi chất trong hỗn hợp
phương trình bn tự ghi nha:
đặt số mol 3 KL Zn, Fe, Cu lần lượt là a, b, c (mol), ta có pt theo đề bài:
65a+56b+64c=21.6 (1)
c=3/64 (2)
a+b=6.72/22.4 (3)
Từ (1)(2)(3)==> a=0.2(mol), b=0.1(mol), c=3/64(mol)
==>%Zn=0.2x65x100/21.6=60.185%
%Fe=0.1x56x100/21.6=25.925%
%Cu=100%-(60.185%+25.925%)=13.89%
Đúng 1
Bình luận (6)
cho 21,6g hỗn hợp Zn Fe Cu phản ứng vừa đủ với mg dung dịch H2SO4 25% .sau phản ứng thu được 6,72l khí ở dktc và 3g chất rắn không tan .
A, tính % khối lượng mỗi kim loại trong hỗn hợp đầu
B, Tính m
C, Tính C% của chất rắn trong dung dịch sau phản ứng
a, \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
mhh Zn và Fe = 21,6-3 = 18,6 (g)
PTHH: Zn + H2SO4 → ZnSO4 + H2
Mol: x x
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}65x+56y=18,6\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\%m_{Zn}=\dfrac{0,2.65.100\%}{21,6}=60,19\%\)
\(\%m_{Fe}=\dfrac{0,1.56.100\%}{21,6}=25,93\%\)
\(\%m_{Cu}=100-60,19-25,93=13,88\%\)
b,
PTHH: Zn + H2SO4 → ZnSO4 + H2
Mol: 0,2 0,2 0,2
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,1 0,1 0,1
\(m_{H_2SO_4}=\left(0,1+0,2\right).98=29,4\left(g\right)\Rightarrow m_{ddH_2SO_4}=\dfrac{29,4.100\%}{25\%}=117,6\left(g\right)\)
c,mdd sau pư = 21,6+117,6- (0,1+0,2).2 = 138,6 (g)
\(C\%_{ddZnSO_4}=\dfrac{0,2.161.100\%}{138,6}=23,23\%\)
\(C\%_{ddFeSO_4}=\dfrac{0,1.152.100\%}{138,6}=10,97\%\)
Đúng 2
Bình luận (1)
Hoà tan hoàn toàn 15.1 gam hỗn hợp 3 kim loại gồm Al,Zn,Cu vào dung dịch Hcl 20%( vừa đủ ) thấy thoát ra 8,96L khí H2 đktc và 1 lượng chất rắn không tan, nung chất rắn trong không khí đến khối lượng không đổi, cân nặng được 4 gam A. Viết pthh B. Tính khối lượng các chất trong hỗn hợp ban đầu C. Tính khối lượng dung dịch Hcl đã dùng
\(n_{CuO}=n_{Cu}=\dfrac{4}{80}=0,05mol\\ n_{H_2}=0,4mol\\ n_{Al}=a;n_{Zn}=b\\ 27a+65b=15,1-0,05\cdot64\\ BTe^-:3a+2b=2\cdot0,4\\ a=0,2;b=0,1\\ m_{ddHCl}=\dfrac{\left(0,6+0,2\right)\cdot36,5}{0,2}=146g\)
Đúng 3
Bình luận (0)
Cho một lượng hỗn hợp gồm Ag và Zn tác dụng với lượng dư dung dịch axit H2SO4, thu được 5,6 lit khí H2 (đktc). Sau phản ứng thấy còn 6,25g một chất rắn không tan. Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp.
Chất không tan là Ag.
=> mAg= 6,25(g)
nH2=0,25(mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
-> nZn=nH2= 0,25(mol)
=>mZn= 0,25 . 65=16,25(g)
=>
Đúng 0
Bình luận (1)
2Ag+ 2H2SO4→ Ag2SO4+ 2H2O+ SO2
(mol) 0,04 0,02 Zn+ H2SO4→ ZnSO4+ H2
(mol) 0,25 0,25 \(n_{H_2}=\dfrac{V}{22,4}=\) \(\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
6,25g một chất rắn không tan là: Ag2SO4
→ \(n_{Ag_2SO_4}=\dfrac{m}{M}=\dfrac{6,25}{312}=0,02\left(mol\right)\)
=> mAg=n.M=0,04.108=4,32(g)
mZn=n.M= 0,25.65=16,25(g)
→ mhh kim loại=mAg+mZn=4,32+16,25=20,57(g)
=> %mAg=\(\dfrac{4,32}{20,57}.100\%=21\%\)
%mZn= 100%- 21%= 79%
Đúng 1
Bình luận (0)
2Ag+2H2SO4→Ag2SO4+2H2O+SO2
(mol) 0,04 0,02
Zn+H2SO4→ZnSO4+H2
(mol) 0,25 0,25
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
6,25g một chất rắn không tan đó là: Ag2SO4
→ \(n_{Ag_2SO_4}=\dfrac{m}{M}=\dfrac{6,25}{312}=0,02\left(mol\right)\)
mAg=n.M=0,04.108=4,32(g)
mZn=n.M=0,25.65=16,25(g)
mhh kim loại= mAg+ mZn=4,32+16,25= 20,57(g)
=> %mAg=\(\dfrac{4,32}{20,57}.100\%=21\%\)
%mZn= 100%-21%= 79%
Đúng 0
Bình luận (0)
Cho một lượng hỗn hợp gồm Zn và Cu tác dụng với lượng dư dung dịch axit HCL , thu được 4,48 lít khí H2 (đktc) . Sau phản ứng thấy còn 19,5 gam một chất rắn không tan. Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp.
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl -->ZnCl2 + H2
____0,2<----------------------0,2
=> mZn = 0,2.65 = 13 (g)
mCu = mrắn không tan = 19,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{13}{13+19,5}.100\%=40\%\\\%Cu=\dfrac{19,5}{13+19,5}.100\%=60\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
`n_(H_2)=4,48/22,4=0,2 (mol)`
Ta có PTHH: `Zn+2HCl --> ZnCl_2 +H_2`
Theo PT: `1`--------------------------------`1`
Theo đề: `0,2`------------------------------`0,2`
`m_(Zn)=0,2.65=13(g)`
Vì `Cu` không phản ứng với `HCl` nên `m_(chất rắn không tan)=m_(Cu)=19,5(gam)`
`%Zn=13/(13+19,5) .100%=40%`
`%Cu=100%-40%=60%`
Đúng 0
Bình luận (0)
Câu 1: Cho 10,5 gam hỗn hợp hai kim loại Cu, Zn vào dung dịch H₂SO₄ loãng dư, người ta thu được 2,24 lít khí (đktc). Tính khối lượng chất rắn còn lại trong dung dịch sau phản ứng.
Câu 2: Hòa tan 12 gam hỗn hợp gồm Al, Ag vào dung dịch H₂SO₄ loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H₂ (đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp.
Câu 3: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al₂O₃ trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí H₂. Tính khối lượng mu...
Đọc tiếp
Câu 1: Cho 10,5 gam hỗn hợp hai kim loại Cu, Zn vào dung dịch H₂SO₄ loãng dư, người ta thu được 2,24 lít khí (đktc). Tính khối lượng chất rắn còn lại trong dung dịch sau phản ứng. Câu 2: Hòa tan 12 gam hỗn hợp gồm Al, Ag vào dung dịch H₂SO₄ loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H₂ (đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp. Câu 3: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al₂O₃ trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí H₂. Tính khối lượng muối AlCl₃ thu được.
Câu 2:
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ n_{Al}=\dfrac{2.0,6}{3}=0,4\left(mol\right)\\ \%m_{Al}=\dfrac{0,4.27}{12}.100\%=90\%\Rightarrow\%m_{Ag}=100\%-90\%=10\%\)
Đúng 3
Bình luận (0)
Câu 3:
\(n_{H_2}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ n_{Al}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ n_{Al_2O_3}=\dfrac{25,8-0,2.27}{102}=0,2\left(mol\right)\\ n_{AlCl_3}=n_{Al}+2n_{Al_2O_3}=0,2+2.0,2=0,6\left(mol\right)\\ m_{AlCl_3}=133,5.0,6=80,1\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 1:
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{Zn}=n_{H_2}=0,1\left(mol\right)\\ m_{Zn}=0,1.65=6,5\left(g\right)\\ m_{rắn}=m_{hhCu,Zn}-m_{Zn}=10,5-6,5=4\left(g\right)\)
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 17,6 gam hỗn hợp Fe và Cu vào dung dịch axit H2SO4 đặc nóng, dư. Sau phảnứng thu được 8,96 lit khí SO2 (đo ở đktc) và dung dịch A.a) Tính % khối lượng của mỗi kim loại trong hỗn hợp ban đầu?b) Nếu cho lượng khí SO2 thu được ở trên vào 500 ml dd NaOH 1M. Tính nồng độ mol chất trong ddthu được sau phản ứng? Biết rằng thể tích của dung dịch thay đổi không đáng kể.c) Cho 500 ml dd BaCl2 1M vào dd A. Sau phản ứng thu được m gan kết tủA. Tính m. Biết rằng lượngaxít dư so với phản ứng...
Đọc tiếp
Hoà tan hoàn toàn 17,6 gam hỗn hợp Fe và Cu vào dung dịch axit H2SO4 đặc nóng, dư. Sau phản
ứng thu được 8,96 lit khí SO2 (đo ở đktc) và dung dịch A.
a) Tính % khối lượng của mỗi kim loại trong hỗn hợp ban đầu?
b) Nếu cho lượng khí SO2 thu được ở trên vào 500 ml dd NaOH 1M. Tính nồng độ mol chất trong dd
thu được sau phản ứng? Biết rằng thể tích của dung dịch thay đổi không đáng kể.
c) Cho 500 ml dd BaCl2 1M vào dd A. Sau phản ứng thu được m gan kết tủA. Tính m. Biết rằng lượng
axít dư so với phản ứng là 10%. mọi người giải câu c) dùm em nha các câu trên em làm đc rồi

























