Tinh thể ngậm nước Fe2(SO4)3.x H2O. Tìm x biết khối lượng nước chiếm 28.83%

Những câu hỏi liên quan
Trong tinh thể ngậm nước của muối sunfat KL hoá trịII, nước kết tinh chiếm 45,324% khối lượng tinh thể chứa 11,51% lưu huỳnh. Xác định công thức của tinh thể
Biết thành phần % khối lượng P trong tinh thể Na2HPO4.nH2O là 8,659%. Tinh thể muối ngậm nước đó có số phân tử H2O là A. 9 B. 10 C. 11 D. 12
Đọc tiếp
Biết thành phần % khối lượng P trong tinh thể Na2HPO4.nH2O là 8,659%. Tinh thể muối ngậm nước đó có số phân tử H2O là
A. 9
B. 10
C. 11
D. 12
Đáp án D
Thành phần % P trong tinh thể là ![]()
Đúng 0
Bình luận (0)
Biết thành phần % khối lượng của P trong tinh thể Na2HPO4.nH2O là 8,659%. Tinh thể muối ngậm nước đó có số phân tử H2O là A. 12 B. 9 C. 11 D. 13
Đọc tiếp
Biết thành phần % khối lượng của P trong tinh thể Na2HPO4.nH2O là 8,659%. Tinh thể muối ngậm nước đó có số phân tử H2O là
A. 12
B. 9
C. 11
D. 13
%mP = 31/ ( 142 + 18n) = 8,659%
=> n=12
=>A
Đúng 0
Bình luận (0)
1. Khối lượng của CuSO4 trong dd là 64g, khối lượng của tinh thể ngậm nước là 100g. Xác định CTHH muối ngậm nước
2. Tính khối lượng AgNO3 có thể tan trong 250 gam nước ở 25 độ C, biết độ tan của AgNO3 ở 25độ C là 222 gam
Xác định công thức của tinh thể BaCl2 ngậm nước . Biết thành phần % về khối lượng nước kết tinh trong tinh thể là 14,75%
Gọi công thức tinh thể cần tìm là: BaCl2.nH2O. 208 + 18n
mH2O = n.18=18n (g) %H2O =\(\dfrac{18n}{208+18n}\).100 =14,75 => 1800n = 14,75.(208 + 18n) => n = 2 Vậy: Công thức của tinh thể là:BaCl2.2H2O
Đúng 0
Bình luận (0)
Gọi công thức tinh thể BaCl2 ngậm nước cần tìm là BaCl2.nH2O
Ta có : \(M_{BaCl_2.nH_2O}=208+18n\left(g\right)\)
\(\Rightarrow\%H_2O=\dfrac{18n}{208+18n}\cdot100\%=14,75\%\)
\(\Leftrightarrow1800n=14,75\left(208+18n\right)\)
\(\Rightarrow n=2\)
Vậy công thức tinh thể là BaCl2.2H2O
Đúng 0
Bình luận (0)
Gọi CT tinh thể cần tìm là: BaCl2.nH2O
Ta có: MBaCl2.nH2O=208 + 18n (g/mol)
=> \(\%H_2O=\dfrac{18n.100\%}{208+18n}=14,75\left(\%\right)\)
<=> 1800n=14,75(208+18n)
<=> 1800n=3068+265,5n
<=> 1534,5n=3068
=> n\(\approx2\)
Vậy CT của tinh thể là : BaCl2.2H2O
Đúng 0
Bình luận (0)
Thành phần khối lượng của photpho trong Na2HPO4 ngậm nước là 11,56%. Trong 1 phân tử tinh thể ngâm nước đó có số phân tử H2O là:
A. 0
B. 1
C. 7
D. 12
Thêm 131,9 g Fe2(SO4)3 vào dung dịch D; khuấy đều thấy tách ra 28,1g tinh thể X. Biết độ tan của Fe2(SO4)3 tại nhiệt độ thí nghiệm là 1g/1ml H2O. Xác định công thức của X.
Một muối sunfat của kim loại hóa trị II ngậm nước có phân tử khối 278 gam và khối lượng nước kết tinh chiếm 45,324%. Tìm công thức hóa học của muối trên.
Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
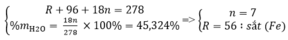
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O
Đúng 0
Bình luận (0)
một tinh thể ngậm nước có công thức là M(NO3)3.nH2O, trong đó % khối lượng oxi trong tinh thể là 71,29%, % khối lượng hidro là 4,46%
a) tìm công thức tinh thể
b) tìm thể tích khí NH3 để chứa được lượng nitơ bằng lượng nitơ trong 8,08 gam tinh thể trên











