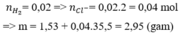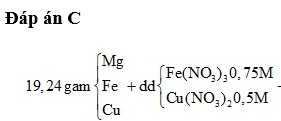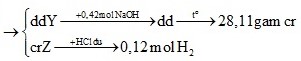Cho 1,53g hỗn hợp bột Mg, Zn và Fe với dung dịch HCl dư thấy thoát ra 4,48ml khí (đktc). Cô cạn hỗn hợp sau phản ứng thì thu được chất rắn có khối lượng là.

Những câu hỏi liên quan
Cho 1,53 gam hỗn hợp Ba, Mg, Fe và Zn vào dung dịch HCl dư thấy thoát ra 448 ml khí (đktc). Cô cạn hỗn hợp sau phản ứng thì thu được chất rắn có khối lượng là
A. 2,24 gam
B. 2,95 gam
C. 1,85 gam
D. 3,90 gam
Cho 1,5 gam hỗn hợp Mg Fe Al vào dung dịch HCl dư thấy thoát ra 0.336 lít khí ở điều kiện tiêu chuẩn .Cô cạn dung dịch sau phản ứng thì thu được chất rắn có khối lượng
\(n_{H_2}=\dfrac{0,336}{22,4}=0,015mol\)
\(\Rightarrow n_{HCl}=2n_{H_2}=2\cdot0,015=0,03mol\)
\(\Rightarrow n_{Cl^-}=0,03mol\Rightarrow m_{Cl^-}=1,065g\)
\(m_{CRắn}=m_{kl}+m_{Cl^-}=1,065+1,5=2,565g\)
Đúng 2
Bình luận (0)
Cho 12,1 gam hỗn hợp kim loại gồm Fe và Zn tan hết trong dung dịch HCl (vừa đủ) thấy thoát ra 4,48 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được chất rắn có khối lượng là
A. 24,6 gam.
B. 26,3 gam.
C. 19,2 gam.
D. 22,8 gam.
12,1 gam (Fe, Zn) + HCl (vừa đủ) → muối FeCl 2 , ZnCl 2 + H 2

Đáp án là C
Đúng 0
Bình luận (0)
Cho 12,1 gam hỗn hợp kim loại gồm Fe và Zn tan hết trong dung dịch HCl (vừa đủ) thấy thoát ra 4,48 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được chất rắn có khối lượng là A. 24,6 gam B. 26,3 gam C. 19,2 gam D. 22,8 gam
Đọc tiếp
Cho 12,1 gam hỗn hợp kim loại gồm Fe và Zn tan hết trong dung dịch HCl (vừa đủ) thấy thoát ra 4,48 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được chất rắn có khối lượng là
A. 24,6 gam
B. 26,3 gam
C. 19,2 gam
D. 22,8 gam
Chọn đáp án B
mMuối = 12,1 + 0,2.2.35,5 = 26,3 gam
Đúng 0
Bình luận (0)
Cho 1,53g hỗn hợp Mg, Fe, Zn vào dd HCl dư thấy thoát ra 448ml khí (đktc). Cô cạn hỗn hợp sau phản ứng thì thu được chất rắn có khối lượng là
nH2=0,44822,4=0,02mol
BTNTH:nHClpư=2nH2=0,04mol
BTKL:mKL+mHClpư=mmuối+mH2
=>1,53+0,04.36,5=mmuối+0,02.2
=>mmuối=2,95gam
Chất rắn sau khi cô cạn là muối có khối lượng 2,95 gam.
Nung 10,2g hỗn hợp Al, Mg, Na trong khí Oxi dư. Sau phản ứng kết thúc thu được 17g hỗn hợp chất rắn . Mặt khác cho hỗn hợp các kim loại trên tác dụng với dung dịch HCl dư thì thấy thoát ra V lít khí và dung dịch A. Cô cạn A thì thu được mg muối Clorua khan. Tính V và m ?
Gọi số mol Al, Mg, Na là a, b,c (mol)
- Xét TN1:
\(n_{O_2}=\dfrac{17-10,2}{32}=0,2125\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
a-->0,75a
2Mg + O2 --to--> 2MgO
b--->0,5b
4Na + O2 --to--> 2Na2O
c--->0,25c
=> 0,75a + 0,5b + 0,25c = 0,2125
- Xét TN2:
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a------------->a----->1,5a
Mg + 2HCl --> MgCl2 + H2
b------------->b------>b
2Na + 2HCl --> 2NaCl + H2
c-------------->c---->0,5c
nH2 = 1,5a + b + 0,5c = 0,2125.2 = 0,425 (mol)
=> V = 0,425.22,4 = 9,52 (l)
Có: \(n_{HCl}=2.n_{H_2}=0,425.2=0,85\left(mol\right)\)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> 10,2 + 0,85.36,5 = m + 0,425.2
=> m = 40,375 (g)
Đúng 1
Bình luận (0)
Nung 2,48 gam hỗn hợp X gồm Na, Mg, Al trong khí oxi dư, sau khi kết thúc phản ứng thu được 4,08 gam hỗn hợp chất rắn Y. Mặt khác, cho 4,96 gam hỗn hợp X trên tác dụng với dung dịch HCl dư thì thấy thoát ra V lít khí (ở đktc) và dung dịch A. Cô cạn dung dịch A thu được m gam muối clorua khan.
a. Viết các phương trình hóa học xảy ra.
b. Tính V, m?
a)
$4Na + O_2 \xrightarrow{t^o} 2Na_2O$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$2Na + 2HCl \to 2NaCl + H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
b)
Bảo toàn khối lượng : $m_{O_2} = 4,08 - 2,48 = 1,6(gam)$
$n_{O_2} = \dfrac{1,6}{32} = 0,05(mol)$
Đốt 2,48 gam X cần 0,05 mol $O_2$
Suy ra, đốt 4,96 gam X cần 0,1 mol $O_2$
Mà : \(\dfrac{1}{4}n_{Na}+\dfrac{1}{2}n_{Mg}+\dfrac{3}{4}n_{Al}=n_{O_2}=0,1\)
Theo PTHH :
\(n_{H_2}=\dfrac{1}{2}n_{Na}+n_{Mg}+\dfrac{3}{2}n_{Al}=2\left(\dfrac{1}{4}n_{Na}+\dfrac{1}{2}n_{Mg}+\dfrac{3}{4}n_{Al}\right)=2.0,1=0,2\)$V = 0,2.22,4 = 4,48(lít)$
$n_{HCl} = 2n_{H_2} = 0,4(mol)$
Bảo toàn khối lượng : $m = 4,96 + 0,4.36,5 - 0,2.2 = 19,16(gam)$
Đúng 2
Bình luận (0)
Cho 19,24 gam hỗn hợp gồm Mg, Fe, Cu vào dung dịch chứa
F
e
N
O
3
3
0,75M và
C
u
N
O
3
3
0,5M. Sau khi kết thúc phản ứng thu được dung dịch Y có chứa 2 muối và 20,56 gam chất rắn Z. Cho 350 ml dung d...
Đọc tiếp
Cho 19,24 gam hỗn hợp gồm Mg, Fe, Cu vào dung dịch chứa F e N O 3 3 0,75M và C u N O 3 3 0,5M. Sau khi kết thúc phản ứng thu được dung dịch Y có chứa 2 muối và 20,56 gam chất rắn Z. Cho 350 ml dung dịch NaOH 1,2M vào dung dịch Y, lọc bỏ kết tủa, cô cạn dung dịch nước lọc, lấy phần rắn đem nung đến khối lượng không đổi thu được 28,11 gam chất rắn khan. Cho dung dịch HCl dư vào rắn Z thấy thoát ra 2,688 lít khí H 2 (đktc). Phần trăm khối lượng của Mg có trong hỗn hợp X gần nhất với
A. 14,1%
B. 13,5%
C. 13,1%
D. 13,3%
Hòa tan hoàn toàn 13.6g hỗn hợp X gồm Mg và Fe vào lượng dư dung dịch HCl 2M sau phản ứng thấy thoát ra 6.72l H2 (đktc) và dung dịch Y
a. Tính % khối lượng mỗi chất trong hỗn hợp X
b. Tính thể tích dung dịch HCl đã phản ứng
c. Cô cạn dung dịch Y thu được m gam muối khan. Tính giá trị m
Mọi người giúp mình với ạ.
Xem chi tiết
\(Đặt:\)
\(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
\(m_{hh}=24x+56y=13.6\left(g\right)\\ n_{H_2}=x+y=0.3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0.1\\y=0.2\end{matrix}\right.\)
\(\%Mg=\dfrac{0.1\cdot24}{13.6}\cdot100\%=17.64\%\\ \%Fe=100-17.64=82.36\%\)
\(n_{HCl}=2n_{H_2}=2\cdot0.3=0.6\left(mol\right)\)
\(V_{HCl}=\dfrac{0.6}{2}=0.3\left(l\right)\)
\(m_Y=m_{MgCl_2}+m_{FeCl_2}=0.1\cdot95+0.2\cdot127=34.9\left(g\right)\)
Đúng 1
Bình luận (0)