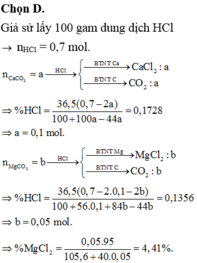Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 29,2%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 20,74%. Thêm vào X một lượng bột BaCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn là 8,52%. Xác định nồng độ phần trăm các muối CaCl2 và BaCl2 trong dung dịch Y.

Những câu hỏi liên quan
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại 24,2%. Thêm vào X một lượng bột MgCO3, khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ dung dịch HCl bằng 21,10%. Nồng độ % của dung dịch CaCl2 và MgCl2 lần lượt là: A. 11,35% và 3,54% B. 11,35% và 4,54% C. 10,35% và 3,04% D. 10,35% và 3,54%
Đọc tiếp
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại 24,2%. Thêm vào X một lượng bột MgCO3, khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ dung dịch HCl bằng 21,10%. Nồng độ % của dung dịch CaCl2 và MgCl2 lần lượt là:
A. 11,35% và 3,54%
B. 11,35% và 4,54%
C. 10,35% và 3,04%
D. 10,35% và 3,54%
Đáp án D
Giả sử có 100 gam dung dịch HCl 32,85% thì khối lượng HCl là 32,85 gam.
nHCl= 32 , 85 36 , 5 = 0,90 mol
- Gọi số mol của CaCO3 là x (mol). Phản ứng:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 (1)
x 2x x x
Từ (1) và đề ra: nHCldư = (0,90 - 2x) mol
Khối lượng dung dịch X sau phản ứng (1): 100 + 100x – 44x = (100 + 56x) gam
Theo đề ra: C%HCl = ( 0 , 90 - 2 x ) . 36 , 5 100 + 56 x . 100 % = 24,195% => x = 0,1 mol
Vậy sau p/ư (1) nHCl còn lại = 0,7mol
- Cho MgCO3 vào dung dịch X, có p/ư:
MgCO3 + 2HCl → MgCl2 + H2O + CO2 (2)
y 2y y y
Sau p/ư (2) nHCl dư = 0,7-2y
Khối lượng dung dịch Y là: (105,6 + 84y - 44y) gam hay (105,6 + 40y) gam
Từ (2) và đề ra: C%HCl trong Y = ( 0 , 7 - 2 y ) . 36 , 5 105 , 6 + 40 y . 100% = 21,11% => y = 0,04 mol
Dung dịch Y chứa 2 muối CaCl2, MgCl2 và HCl dư:
C%(CaCl2) = 0 , 1 . 111 107 , 2 . 100 % = 10 , 35 %
C%(MgCl2) = 0 , 04 . 95 107 , 2 . 100 % = 3 , 54 %
Đúng 0
Bình luận (0)
Cho một lượng tinh bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 24,20%. Thêm vào X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 21,10%. Nồng độ phần trăm MgCl2 trong dung dịch Y là: A. 12,35% B. 3,54% C. 10,35% D. 8,54%
Đọc tiếp
Cho một lượng tinh bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 24,20%. Thêm vào X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 21,10%. Nồng độ phần trăm MgCl2 trong dung dịch Y là:
A. 12,35%
B. 3,54%
C. 10,35%
D. 8,54%
Đáp án B
Chọn 1 mol HCl ban đầu. Gọi n C a C O 3 = x
Có phản ứng: C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O (1)
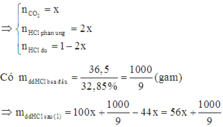
Do đó nồng độ phần trăm của HCl sau phản ứng (1) là:
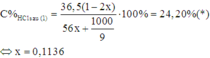
Do đó sau phản ứng (1) dung dịch X có mx = 117,47; nHCl dư = 0,7728
Gọi n M g C O 3 = y . Có phản ứng:
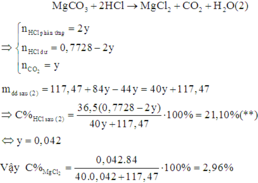
Do trong quá trình tính toán, ta có nhiều bước làm tròn nên dẫn đến sai số.
Khi đó ta sẽ chọn đáp án gần với kết quả tính được nhất.
Đúng 0
Bình luận (0)
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 25,55%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 17,28%. Thêm vào dung dịch X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 13,56%. Nồng độ phần trăm của MgCl2 trong dung dịch Y gần nhất với: A. 5,2%. B. 4,2%. C. 5,0%. D. 4,5%.
Đọc tiếp
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 25,55%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 17,28%. Thêm vào dung dịch X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 13,56%. Nồng độ phần trăm của MgCl2 trong dung dịch Y gần nhất với:
A. 5,2%.
B. 4,2%.
C. 5,0%.
D. 4,5%.
Cho một lượng bột CaCO3 tác dùng hoàn toàn vói dd HCl 32,85% sau phản ứng thu được dd X, trong đó nông độ HCl còn lại là 24,2%. Thêm vào X một lượng bột MgCO3 vào va khuấy đều để phản ứng xảy ra hoàn toàn, thu được dd Y, trong đó nồng độ HCl còn lại là 21,1%. Xác định nồng độ % các muối CaCl2, MgCl2 trong dd Y
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng, thu được dung dịch X trong đó nồng độ HCl còn lại là 24,195%. Thêm vào X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn, thu được dung dịch Y trong đó nồng độ HCl còn lại là 21,11%. Tính nồng độ % của các muối có trong dung dịch Y
cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau khi phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 24,20%.Thêm X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 21,10%. Nồng độ phần trăm MgCl2 trong dung dịch Y là:
Hòa tan hoàn toàn một lượng bột BaCO3 bằng dd HCl 7,3% sau phản ứng thu được dung dịch Acó nồng độ HCl 2,2,8%. Tính C% của dung dịch muối thu được trong A
Coi $m_{dd\ HCl} = 100(gam) \Rightarrow n_{HCl} = \dfrac{100.7,3\%}{36,5} = 0,2(mol)$
Gọi $n_{BaCO_3} = a(mol)$
BaCO3 + 2HCl → BaCl2 + CO2 + H2O
a..................2a............a..............a........................(mol)
Sau phản ứng :
$m_{dd} = 197a + 100 - a.44 = 153a + 100(gam)$
$n_{HCl\ dư} = 0,2 - 2a(mol)$
Suy ra :
$C\%_{HCl} = \dfrac{(0,2-2a).36,5}{153a + 100}.100\% = 2,28\%$
$\Rightarrow a = 0,066$
$C\%_{BaCl_2} = \dfrac{0,066.208}{0,066.153 + 100}.100\% = 12,47\%$
Đúng 5
Bình luận (0)
b. Hòa tan hoàn toàn một lượng bột BaCO3 bằng dd HCl 7,3% sau phản ứng thu được dung dịch Acó nồng độ HCl 2,28%. Tính C% của dung dịch muối thu được trong A
\(GS:m_{dd_{HCl}}=100\left(g\right)\)
\(m_{HCl}=100\cdot7.3\%=7.3\left(g\right)\)
\(n_{BaCO_3}=a\left(mol\right)\)
\(BaCO_3+2HCl\rightarrow BaCl_2+CO_2+H_2O\)
\(a..........2a.........a......a\)
\(m_{\text{dung dịch sau phản ứng}}=197a+100-44a=153a+100\left(g\right)\)\(\)
\(m_{HCl}=7.3-73a\left(g\right)\)
\(C\%_{HCl\left(dư\right)}=\dfrac{7.3-73a}{153a+100}\cdot100\%=2.28\%\)
\(\Rightarrow a=0.065\)
\(C\%_{BaCl_2}=\dfrac{0.065\cdot208}{153\cdot0.065+100}\cdot100\%=12.3\%\)
Đúng 1
Bình luận (0)
Chia 47,1g hỗn hợp bột X gồm Zn, Fe, Mg thành 3 phần bằng nhau. Cho phần 1 vào 500ml dung dịch HCl nồng độ a mol/l, làm khô hỗn hợp sau phản ứng thu được 33,45g chất rắn khan. Cho phần 2 tác dụng với 450ml dung dịch HCl nồng độ 2a mol/l, làm khô hỗn hợp sau phản ứng thu được 40,55g chất rắn khan. Phần 3 tác dụng với lượng dư dung dịch AgNO3 thu được 86,4g chất rắn. Biết các phản ứng đều xảy ra hoàn toàn, các quá trình làm khô hỗn hợp không xảy ra phản ứng hóa học. giá trị của a và phần trăm số m...
Đọc tiếp
Chia 47,1g hỗn hợp bột X gồm Zn, Fe, Mg thành 3 phần bằng nhau. Cho phần 1 vào 500ml dung dịch HCl nồng độ a mol/l, làm khô hỗn hợp sau phản ứng thu được 33,45g chất rắn khan. Cho phần 2 tác dụng với 450ml dung dịch HCl nồng độ 2a mol/l, làm khô hỗn hợp sau phản ứng thu được 40,55g chất rắn khan. Phần 3 tác dụng với lượng dư dung dịch AgNO3 thu được 86,4g chất rắn. Biết các phản ứng đều xảy ra hoàn toàn, các quá trình làm khô hỗn hợp không xảy ra phản ứng hóa học. giá trị của a và phần trăm số mol của Mg có trong hỗn hợp X lần lượt là :
A. 0,5 và 22,93%
B. 1,0 và 42,86%
C. 0,5 và 42,96%
D. 1,0 và 22,93%
Đáp án : B
Xét P1 và P2 : khi số mol HCl tăng thì khối lượng rắn tăng => ở P1 HCl thiếu
=> mrắn – mP1 = mCl pứ => nCl pứ = 0,5 mol = nHCl = 0,5a
=> a = 1 M
Gọi số mol Zn , Mg , Fe trong mỗi phần lần lượt là x , y , z
+) P2 : mrắn – mP2 = mCl pứ => nCl pứ = 0,7 mol < nHCl => kim loại phản ứng hết
=> 2x + 2y + 2z = 0,7 mol
+) P3 : nAg = 2nZn + 2nMg + nFe => 2x + 2y + 3z = 0,8 mol
,mmỗi P = 65x + 24y + 56z = 15,7g
=> x = z = 0,1 ; y = 0,15 mol
=> %nMg = 42,86%
Đúng 0
Bình luận (0)