Cho dung dịch NaOH 1M tác dụng vừa đủ với 200 ml dung dịch HCl 2 M thu được dung dịch X.
a) Tính thể tích dung dịch NaOH đã dùng.
b) Tính khối lượng muối tạo thành trong X.
Cho 16g bột CuO tác dụng vừa đủ với dung dịch HCl thu được 89g dung dịch muối
a) Tính nồng độ dung dịch HCl đã dùng
b) Tiếp tục cho từ từ dung dịch NaOH 1M vào dung dịch muối cho tới khi thu được kết tủa tối đa thì ngừng lại
Tính khối lượng chất kết tủa thu được
Tính thể tích dung dịch NaOh đã dùng
câu a là nồng độ mol hay nồng độ phần trăm
1 Cho 10,6gam Na2CO3 tác dụng vừa đủ với dung dịch CH3COOH 0,5M a/ Tính thể tích dung dịch CH3COOH cần dùng? b/ Tính khối lượng muối tạo thành? 2 Trung hòa 100 ml dung dịch CH3COOH 0,3M bằng dung dịch NaOH 1,5M. a) Tính thể tích dung dịch NaOH đã dùng ? b) Tính khối lượng muối thu được sau phản ứng ? c) Tính nồng độ mol của chất tan có trong dung dịch sau phản ứng ( biết thể tích thay đổi không đáng kể) ? Biết C= 12; O= 16; H = 1 ; Na=23 3/ Đốt cháy hoàn toàn 2,3 g rượu etylic nguyên chất a) Viết phương trình hóa học xảy ra. b) Tính thể tích khí CO2 sinh ra ở điều kiện tiêu chuẩn? c) Tính thể tích không khí cần dùng biết oxi chiếm 20% thể tích không khí? Biết C= 12; O= 16; H = 1
Cho 0,1 mol axit α-aminopropionic tác dụng vừa đủ với dung dịch HCl, thu được dung dịch X. Cho X tác dụng với 200 ml dung dịch NaOH 1M, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 11,10
B. 16,95
C. 11,70
D. 18,75
Đáp án B
Số mol NaOH phản ứng vừa đủ với HCl và 0,1 mol axit α-aminopropionic
CH3-CH(NH2)-COOH + NaOH → CH3-CH(NH2)COONa + H2O
0,1---------------------------0,1-----------------0,1
HCl + NaOH → NaCl + H2O
0,1-------0,1-------0,1
Vậy m = 0,1 x 111 + 0,1 x 58,5 = 16,95 gam → Chọn B.
Cho 300 ml dung dịch HCL 1M tác dụng với 200 ml dung dịch NaOH 0,5M. a) Viết phương trình hóa học xảy ra. b) Tính và so sánh số mol của hai dung dịch HCL và NaOH đã cho ở giả thiết. c) Tính khối lượng muối Nacl tạo thành.
a: \(HCl+NaOH\rightarrow NaCl+H_2O\)
\(n_{HCl}=0.3\cdot1=0.3\left(mol\right)\)
\(n_{NaOH}=0.2\cdot0.5=0.1\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
Lập tỉ lệ : \(\dfrac{0.3}{1}>\dfrac{0.1}{1}\Rightarrow HCldư\)
\(m_{NaCl}=0.1\cdot58.5=5.85\left(g\right)\)
Cho bột sắt (dư) vào 10 (ml) dung dịch CuSO4 1M. Kết thúc phản ứng thu được chất rắn A và dung dịch B
a) Tính khối lượng đồng thu được sau phản ứng
b) Đem dung dịch B tác dụng vừa đủ với dung dịch NaOH 1M. Tính thể tích dung dich NaOH đã dùng
nCuSO4=0,01 mol
Fe+CuSO4=> FeSO4+Cu
0,01 mol =>0,01 mol
mCu=0,01.64=0,64gam
FeSO4+2NaOH=>Fe(OH)2 +Na2SO4
0,01 mol=>0,02 mol
Vdd NaOH=0,02/1=0,02 lit
Cho 20,15 gam hỗn hợp X gồm CH2NH2COOH và CH3CHNH2COOH tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là:
A. 55,83% và 44,17%.
B. 58,53% và 41,47%.
C. 53,58% và 46,42%.
D. 52,59% và 47,41%
Quy hỗn hợp Y thành X (x mol) và HC1 (0,2 mol)
![]()
Gọi a, b lần lượt là số mol CH2NH2COOH và CH3CHNH2COOH
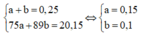
Từ đó tính được phần trăm khối lượng của mỗi chất.
Đáp án A
Cho 200ml dung dịch NaOH tác dụng với dung dịch HCl 0,5 M a) tính khối lượng muối thu được sau phản ứng b) tính thể tích của dung dịch HCl đã dùng
Cho 69 6 gam MnO2 tác dụng với dung dịch HCl đặc thu được khí A.
a)Tính thể tích khí A
b) Cho khí A tác dụng vừa đủ với dung dịch NaOH 1M được dung dịch B. Tính thể tích dung dịch NaOH cần dùng và nồng độ mol các chất trong dung dịch B
\(a)n_{MnO_2}=\dfrac{69,6}{87}=0,8mol\\ MnO_2+4HCl\xrightarrow[nhẹ]{đun}MnCl_2+Cl_2+H_2O\)
0,8 3,2 0,8 0,8 0,8
\(V_A=V_{Cl_2}=0,8.22,4=17,92l\\ b)Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\)
0,8 1,6 0,8 0,8
\(V_{ddNaOH}=\dfrac{1,6}{1}=1,6l\\ C_{M_{NaCl}}=\dfrac{0,8}{1,6}=0,5M\\ C_{M_{NaClO}}=\dfrac{0,8}{1,6}=0,5M\)
Cho 20,15 g hỗn hợp X gồm (NH2CH2 COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là
A.58,53%và41,47%.
B.55,83%và44,17%.
C.53,58%và46,42%.
D.52,59%và47,41%.