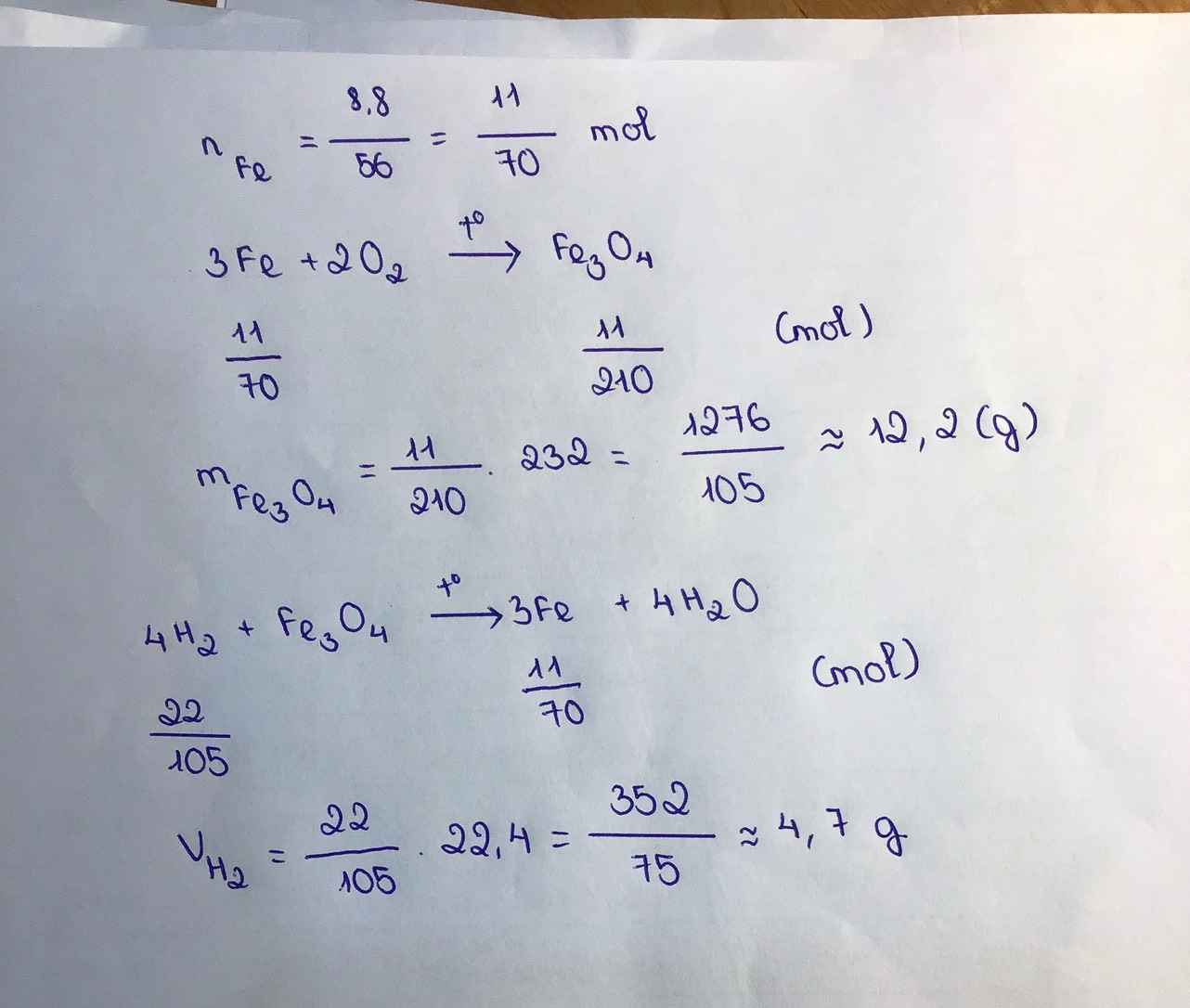Đốt cháy hoàn toàn 1,6 gam sắt ở nhiệt độ cao. Khối lượng sắt oxit thu được là: *

Những câu hỏi liên quan
Đốt cháy hoàn toàn 3,36 gam sắt Fe ở nhiệt độ cao thu được oxit sắt từ Fe3O4.
a/ Tính khối lượng oxit sắt từ thu được sau phản ứng.
b/ Tính thề tích khí oxi cần dùng (đktc).
a) \(n_{Fe}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,06->0,04------->0,02
=> mFe3O4 = 0,02.232 = 4,64 (g)
b) VO2 = 0,04.22,4 = 0,896 (l)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 8,8 gam sắt trong lọ chứa khí oxi
a) Viết PTHH xảy ra.
b) Tính khối lượng oxit sắt từ thu được.
c) Tính thể tích khí Hidro (đktc) cần dùng để khử hoàn toàn lượng oxit sắt từ trên ở nhiệt độ cao.
a) nFe= 8,4/56 = 0,15(mol)
PTHH: 3 Fe + 2 O2 -to-> Fe3O4
0,15_______0,1_____0,05(mol)
b) mFe3O4= 232. 0,05= 11,6(g)
Đúng 1
Bình luận (3)
Đốt cháy hết 5,04 gam sắt ở nhiệt độ cao. Khối lượng sắt từ oxit thu được là:
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{5,04}{56}=0,09mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,09 0,03 ( mol )
\(m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=0,03.232=6,96g\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 16,8g Fe trong bình chứa O2 dư thu được sắt từ oxit (Fe3O4)
A.Hãy viết phương trình phản ứng xảy ra
B.Tính khối lượng FeO4 thu được?
C.Khử hoàn toàn lượng sắt từ oxit trên bằng 44,8 lít khí H2 ở đktc thành sắt kim loại ở nhiệt độ cao,sau phản ứng chất nào dư và dư bao nhiêu gam?
nFe = 16,8 : 56 = 0,3 (mol)
pthh :3 Fe + 2O2 -t--> Fe3O4
0,3--------------> 0,1 (mol)
=> mFe3O4 =0,1 . 232 = 23,2(G)
nH2 = 44,8 : 22,4 = 2 (g)
pthh : Fe3O4 + H2 -t--> Fe + H2O
LTL : 0,1 / 1 < 2 /1
=> H2 du
nH2 (pu) = nFe3O4 = 0,1 (mol)
=> nH2 (d) = 2-0,1 = 1,9 (mol)
mH2 (d) = 1,9 . 2 = 3,8 (g)
Đúng 3
Bình luận (2)
Khi đốt cháy sắt trong oxi ở nhiệt độ cao, thu được oxit sắt từ. Để điều chế 4,64 gam oxit sắt từ thì khối lượng oxi đem dùng là *
1,28 gam.
3,24 gam.
4,56 gam.
2,25 gam.
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
3Fe + 2O2 \(\underrightarrow{t^o}\) Fe3O4
0,04 0,02 ( mol )
\(m_{O_2}=0,04.32=1,28\left(g\right)\)
=> Đáp án A
Đúng 1
Bình luận (0)
Khi đốt cháy sắt trong oxi ở nhiệt độ cao, thu được oxit sắt từ. Để điều chế 4,64 gam oxit sắt từ thì khối lượng oxi đem dùng là *
1,28 gam.
3,24 gam.
4,56 gam.
2,25 gam.
Đúng 0
Bình luận (0)
Khử hoàn toàn 16 gam bột oxit sắt bằng khí CO ở nhiệt độ cao. Sau phản ứng khối lượng khí thu được tăng thêm so với khối lượng khí ban đầu 4,8 gam. Công thức của oxit sắt là A.
F
e
2
O
3
. B. FeO. C.
F
e
O
2
. D.
F
e
3
O
4
.
Đọc tiếp
Khử hoàn toàn 16 gam bột oxit sắt bằng khí CO ở nhiệt độ cao. Sau phản ứng khối lượng khí thu được tăng thêm so với khối lượng khí ban đầu 4,8 gam. Công thức của oxit sắt là
A. F e 2 O 3 .
B. FeO.
C. F e O 2 .
D. F e 3 O 4 .
Đốt cháy hoàn toàn 6,72 gam bột sắt trong không khí. Giả sử sản phẩm thu được chỉ có sắt (II) oxit. Khối lượng oxit sắt thu được là
A. 1,344 g
B. 0,864 g
C. 8,64 g
D. 13,44 g
Đáp án C
2 F e + O 2 → 2 F e O 0 , 12 → 0 , 06 → 0 , 12 m o l m F e O = 0 , 12 . 72 = 8 , 64 g V O 2 = 0 , 06 . 22 , 4 = 1 , 344 l
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1.68 sắt ở nhiệt độ cao
a.Tính khối lượng oxit sắt từ thu được sau phản ứng
b.Tính thể tích oxi cần dùng ở đkc
c.Tính thể tích không khí cần thiết để có đủ lượng oxi trên,biết Vo2=20% Vkk
\(a.n_{Fe}=\dfrac{1,68}{56}=0,03mol\\ 3Fe+2O_2\xrightarrow[t^0]{}Fe_3O_4\)
0,03 0,02 0,01
\(m_{Fe_3O_4}=0,01.232=2,32g\\ b.V_{O_2}=0,02.24,79=0,4958l\\ c.V_{kk}=\dfrac{0,4958}{20\%}=2,479l\)
Đúng 4
Bình luận (0)
Tính khối lượng oxi cần dùng trong phòng thí nghiệm, khí đốt cháy sắt ở nhiệt độ cao thu thu được 4,64g oxit sắt từ (Fe3O4)
n Fe3O4=\(\dfrac{4,64}{232}=0,02mol\)
3Fe+2O2-to>Fe3O4
0,06----0,04---0,02
=>m O2=0,04.32=1,28g
Đúng 4
Bình luận (0)
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,06 0,02 ( mol )
\(m_{Fe}=n_{Fe}.M_{Fe}=0,06.56=3,36g\)
Đúng 1
Bình luận (3)
nFe3O4=4,64/232=0,02(mol)
PTHH: 3Fe+2O2 to⟶Fe3O4
0,06 mol ← 0,02 mol
mFe=56×0,06=3,36(g)
mO2=4,64–3,36=1,28(g)
Chúc em học giỏi
Đúng 1
Bình luận (1)